本试题 “碘盐的主要成分是NaCl,还添加有适量的KIO3。下列说法正确的是[ ]A.KIO3中阳离子的结构示意图为B.KIO3和NaCl都是离子化合物C.23Na37Cl中质子数和中子数之...” 主要考查您对原子核的组成及组成粒子间的关系
离子结构示意图
离子化合物
结构式
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原子核的组成及组成粒子间的关系
- 离子结构示意图
- 离子化合物
- 结构式
构成原子的三种微粒的比较:
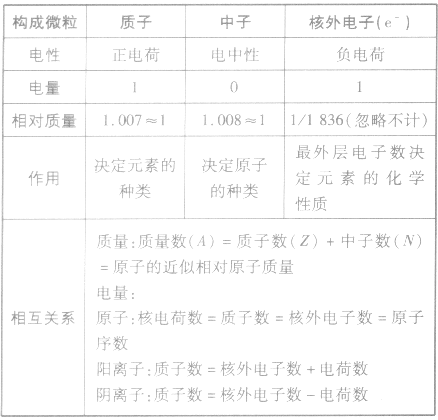
原子的构成:
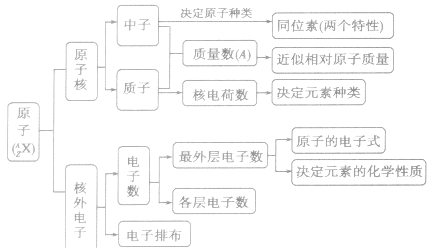
离子结构示意图的判断方法:
正离子的离子结构示意图中核内质子数大于核外电子数;
负离子的离子结构示意图中核内质子数小于核外电子数。
正离子的离子结构示意图中核内质子数大于核外电子数;
负离子的离子结构示意图中核内质子数小于核外电子数。
原子是否满足最外层8电子结构的判断方法:
1.离子化合物
(1)阳离子:看“主族元素原子的次外层电子数+ 原子的最外层电子数一化合价数”是否等于8,若为8,则该原子满足最外层8电子结构,否则不满足。
(2)阴离子:看“其原子的最外层电子数+化合价的绝对值”是否等于8,若为8,则该原子满足最外层8 电子结构,否则不满足。
2.共价化合物计算“各原子的最外层电子数+化合价的绝对值” 是否等于8,若为8,则该原子满足最外层8电子结构,否则不满足。另外,还有一些不满足8电子结构的特殊粒子,请大家记住:
(1)主族元素形成的化合物中:
a.H、Li、Be、B元素原子不满足最外层8电子结构.
b.非最高价离子(如 Pb2+、Bi3+等)也不满足最外层8电子结构。
(2)过渡金属元素形成的离子最外层电子数一般大于8.
定义:
含有离子键的化合物称为离子化合物,离子化合物中肯定存在离子键,也可以存在共价键。
含有离子键的化合物称为离子化合物,离子化合物中肯定存在离子键,也可以存在共价键。
结构式:
表示分子的结合或排列顺序的式子;如: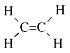
表示分子的结合或排列顺序的式子;如:
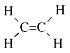
有机物分子中原子共直线、共平面问题的判断:
1、分子空间结构的基本类型:
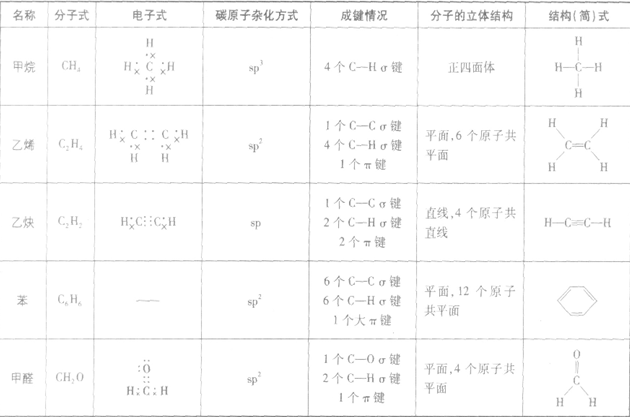
2、分子中原子共线、共面情况的判断方法:
以上述分子结构为原型和思维起点,把复杂的有机物分子分解成几个部分,借助单键可以旋转、双键和三键不能旋转这一知识来分析所分解的各个部分,再予以综合,便能得出分子中在同一平面或同一直线上的原子数目。例如:分子中只要有碳原子形成4个单键,则所有原子小可能都在一个平面上, 中最多有6个原子(5个C原子、1个H原子)在同一条直线上,最多有15个原子(除一CH3上的2个氢原子外)在同一平面上。
中最多有6个原子(5个C原子、1个H原子)在同一条直线上,最多有15个原子(除一CH3上的2个氢原子外)在同一平面上。
发现相似题
与“碘盐的主要成分是NaCl,还添加有适量的KIO3。下列说法正确的...”考查相似的试题有:
- 下列各项表达中正确的是[ ]A.Na2O2的电子式为B.106 g的乙醇和丙醇混合液完全燃烧生成的CO2为112 L(标准状况)C.在氮原子...
- 下列叙述错误的是[ ]A.13C和14C属于同一种元素,它们互为同位素B.1H和2H是不同的核素,它们的质子数相等C.14C和14N的质量...
- 2011年3月11日13时46分日本发生里氏9.0级大地震.地震导致的核泄露产生的放射性污染的主要成份是碘131和铯137,下列有关它们...
- “神舟七号”的燃料是氢化锂三兄弟--LiH、LiD、LiT.其中Li的质量数为7,对这三种物质的下列说法正确的是( )A.质子数之比为1...
- (1)某三价非金属的阴离子,核内有n 个中子,质量数为A ,则其该阴离子核外电子总数为 。(2)已知H2(g)、C2H4(g)和C2H5OH(l)的...
- 下列各组原子序数所表示的两种元素,能形成AB2型离子化合物的是[ ]A.6 和8B.11 和13C.11 和16D.12 和17
- 维生素k4是核酸的组成成分,在体内参与RNA和DNA合成。可用来治疗肿瘤病人因化疗或放疗等引起的白细胞减少。下列有关维生素k4...
- 金银花是治疗和预防甲型H1N1的常见中草药,有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构式见右图,下...
- 有机物A的结构简式为:则A的同分异构体中带苯环的化合物共有( )A.3种B.4种C.5种D.6种
- 分子式为C3H4Cl2链状有机物的同分异构体共有(不考虑顺反异构)A.4种B.5种C.6种D.7种