本试题 “下列各项表述中正确的是( )A.由AlO2-与CO32-在溶液中可以共存,推测:AlO2-与HCO3-在溶液中可以共存B.足量的氢氧化钙溶液中滴加少量的碳酸氢镁:Ca2++2OH...” 主要考查您对离子方程式
盐类水解判断溶液酸碱性或比较溶液pH值的大小
苯酚
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 离子方程式
- 盐类水解判断溶液酸碱性或比较溶液pH值的大小
- 苯酚
用实际参加反应的离子符号表示离子反应的式子。
离子方程式书写规则:
①写:写出化学反应方程式
②拆:把易溶于水、易电离的物质写成离子形式,难容难电离的物质及气体等仍用化学式表示
③删:删去方程式两边不参加反应的离子
④查:检查离子方程式两边各元素的原子个数和电荷总数是否相等
离子方程式书写及正误的判断方法:
①判断反应是否在水溶液中进行
因为电解质在水溶液中可以电离为自由移动的离子,在这种条件下才能发生离子反应。
②判断反应能否发生。
如果反应不能发生,当然也就没有离子方程式可言。
③判断反应物、生成物是否正确。
④判断质量和电荷是否守恒。
离子方程式不仅要质量守恒,而且反应前后各离子所带电荷总数必须相等。
⑤判断氧化物、难溶物、气体、单质、难电离的弱酸、弱碱、水是否写成了分子形式,而易电离的物质是否写成离子形式。
⑥判断连接符号“=”和“
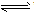 ”及状态符号“↑”和“↓”运用是否正确。
”及状态符号“↑”和“↓”运用是否正确。 强电解质的电离、不可逆反应、双水解反应用“=”;弱电解质电离、可逆反应、水解反应用“
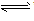 ”。复分解反应、水解反应生成的难溶物用“↓”,气体用“↑”;单水解反应生成的难溶物不用“↓”,气体不用“↑”。
”。复分解反应、水解反应生成的难溶物用“↓”,气体用“↑”;单水解反应生成的难溶物不用“↓”,气体不用“↑”。 ⑦判断微溶物的处理是否正确。
微溶物做反应物时,一般用离子形式,做生成物时一般用分子式。
⑧判断反应物的滴加顺序与方程式中生成物是否一致。
如:把碳酸钠溶液滴加到盐酸溶液中,和把盐酸滴加到碳酸钠溶液中反应产物是不同的。
⑨判断反应物的相对量与产物是否一致。
有些反应因反应物的量不同会生成不同的产物。如:CO2、SO2、H2S等气体与碱溶液反应时,若气体少量,则生成正盐;若气体过量,则生成酸式盐。
⑩判断电解质在写成离子形式时阴阳离子个数比是否合理。
如Ba(OH)2溶液和稀H2SO4反应的离子方程式往往错误写成:
 ,正确为:
,正确为: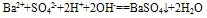
书写与量有关的离子方程式:
基本方法是:把物质的量少的物质的系数定为1,其他物质按最大量消耗。
1.因滴加顺序不同造成连续反应
- HCl与Na2CO3
向Na2CO3溶液中滴入盐酸溶液至过量,其离子反应分步写 (1)CO32-+H+==HCO3- (2)HCO3-+H+==CO2↑+H2O
若向盐酸溶液中滴入Na2CO3溶液至不再产生气体,其离子反应一步完成 CO32-+2H+==CO2↑+H2O
若向足量Na2CO3溶液中加入少量的盐酸溶液,其离子方程式为: CO32-+H+==HCO3-
- HCl与NaAlO2
向Na2CO3溶液中滴入盐酸溶液至过量,其离子反应分步写 (1)CO32-+H+==HCO3- (2)HCO3-+H+==CO2↑+H2O
若向盐酸溶液中滴入Na2CO3溶液至不再产生气体,其离子反应一步完成 CO32-+2H+==CO2↑+H2O
若向足量Na2CO3溶液中加入少量的盐酸溶液,其离子方程式为: CO32-+H+==HCO3-
- AlCl3与NaOH
向AlCl3溶液中滴入NaOH溶液至过量,其离子反应分步写 (1)Al3++3OH-==Al(OH)3↓ (2)Al(OH)3+OH-==AlO2-+2H2O
若向NaOH溶液中加入少量AlCl3溶液,其离子反应一步完成 Al3++4OH-==AlO2-+2H2O
若向足量Al2(SO4)3溶液中加入少量的NaOH溶液,其离子方程式为: Al3++3OH-==Al(OH)3↓
- AgNO3与NH3·H2O
向AgNO3溶液中滴入稀NH3·H2O至过量,其离子反应分步写(1) Ag++NH3·H2O==AgOH↓+NH4+ (2)AgOH+2NH3·H2O==Ag(NH3)2++OH-+2H2O
若向NH3·H2O溶液中加入少量AgNO3,其离子反应一步完成 Ag++3NH3·H2O==Ag(NH3)2++OH-+NH4++2H2O
若向足量AgNO3溶液中滴入少量NH3·H2O,其离子方程式为:Ag++NH3·H2O==AgOH↓+NH4+
- CO2与NaOH
向NaOH溶液中通人CO2气体至过量,其离子反应分步写 (1)2OH-+CO2==CO32-+H2O (2)CO32-+CO2+H2O==2HCO3-
若向足量NaOH溶液中通人少量CO2气体,其离子方程式为: 2OH-+CO2==CO32-+H2O
若向NaOH溶液中通人过量CO2气体,其离子反应一步完成 OH-+CO2==HCO3-
2.过量型:
向足量的Ca(HCO3)2溶液中逐渐滴入NaOH溶液 OH-+Ca2++HCO3-==H2O+CaCO3↓
向足量的NaOH溶液中逐渐滴入Ca(HCO3)2溶液 Ca2++2HCO3-+2OH-==2H2O+CaCO3↓+CO32-
Fe与HNO3 :铁过量时:Fe+4HNO3==Fe(NO3)3+NO↑+2H2O
铁不足时:3Fe+8HNO3==3Fe(NO3)2+2NO↑+4H2O
3.定量型:
因还原性I->Fe2+>Br-,所以在FeI2或者FeBr2中通入一定量的Cl2,发生不同的离子反应,依次为:
(1)2I-+Cl2==2Cl-+I2(2)2Fe2++Cl2==2Fe3++2Cl-(3)2Br-+Cl2==2Cl-+Br2
4.目标型
向明矾溶液逐滴滴加Ba(OH)2溶液至硫酸根离子刚好沉淀完全 Al3++SO42-+Ba2++4OH-==AlO2-+2BaSO4↓+2H2O
向明矾溶液逐滴滴加Ba(OH)2溶液至铝离子刚好沉淀完全 Al3+SO42-+Ba2++3OH-==Al(OH)3↓+2BaSO4↓
(1)盐水解的规律:
①谁弱谁水解,谁强显谁性,越弱越水解,都弱都水解,无弱不水解
②多元弱酸根、正酸根离子比酸式酸根离子水解程度大得多,故可只考虑第一步水解
(2)具体分析一下几种情况:
①强碱弱酸的正盐:弱酸的阴离子发生水解,水解显碱性;如:Na2CO3、NaAc等
②强酸弱碱的正盐:弱碱的阳离子发生水解,水解显酸性;如:NH4Cl、FeCl3、CuCl2等;
③强酸强碱的正盐,不发生水解;如:Na2SO4、NaCl、KNO3等;
④弱酸弱碱的正盐:弱酸的阴离子和弱碱的阳离子都发生水解,溶液的酸碱性取决于弱酸和弱碱的相对强弱,谁强显谁性;
⑤强酸的酸式盐只电离不水解,溶液显酸性,如:NaHSO4;而弱酸的酸式盐,既电离又水解,此时必须考虑其电离和水解程度的相对大小:若电离程度大于水解程度,则溶液显酸性,如:NaHSO3、NaH2PO4;若水解程度大于电离程度,则溶液显碱性,如:NaHCO3、NaHS、Na2HPO4等。
(3)几种盐溶液pH大小的比较强酸强碱盐pH=7、强碱弱酸盐pH>7、强酸弱碱盐pH<7
根据其相应的酸的酸性大小来比较,盐溶液对应的酸的酸性越强,其盐溶液的pH越小如:HClO酸性小于H2CO3,溶液pH NaClO>Na2CO3
酸式盐溶液酸碱性的判断:
酸式盐的水溶液显什么性,要看该盐的组成微粒。
1.强酸的酸式盐只电离,不水解,溶液一定显酸性。如 溶液:
溶液: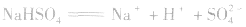
2.弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。
(1)若电离程度小于水解程度,溶液显碱性。例如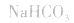 溶液中:
溶液中: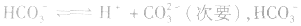
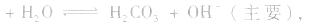
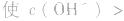
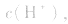 溶液显碱性。NaHS溶液、Na2HPO4溶液亦显碱性
溶液显碱性。NaHS溶液、Na2HPO4溶液亦显碱性
(2)若电离程度大于水解程度,溶液显酸性。例如 溶液中:
溶液中: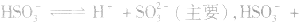
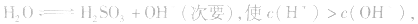 溶液显酸性
溶液显酸性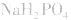 溶液亦显酸性。
溶液亦显酸性。
盐溶液蒸干后所得物质的判断:
1.考虑盐是否分解。如加热蒸干 溶液,因
溶液,因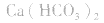 分解,所得固体应是
分解,所得固体应是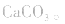
2.考虑氧化还原反应。如加热蒸干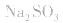 溶液,因
溶液,因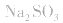 易被氧化,所得固体应是
易被氧化,所得固体应是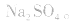
3.盐水解生成挥发性酸时,蒸干后一般得到弱碱,如蒸干 溶液,得
溶液,得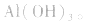 盐水解生成不挥发性酸时,蒸干后一般仍为原物质,如蒸干
盐水解生成不挥发性酸时,蒸干后一般仍为原物质,如蒸干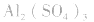 溶液,得
溶液,得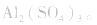
4.盐水解生成强碱时,蒸干后一般得到原物质,如蒸干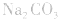 溶液,得到
溶液,得到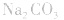 等。
等。
5.有时要多方面考虑,如加热蒸干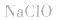 溶液时,既要考虑水解,又要考虑
溶液时,既要考虑水解,又要考虑 的分解,所得固体为
的分解,所得固体为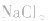
苯酚的结构:
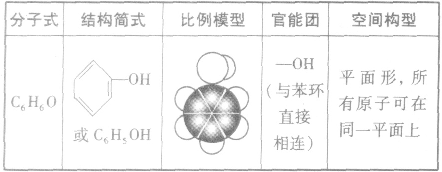
苯酚的性质:
1.物理性质纯净的苯酚是无色的晶体,露置在空气里会因被氧化而呈粉红色。苯酚具有特殊的气味,熔点为43℃。室温时,在水中的溶解度不大,当温度高于65℃时,则能与水以任意比互溶。苯酚易溶于乙醇、乙醚等有机溶剂,有毒,它的浓溶液对皮肤有强烈的腐蚀性。
2.苯酚的化学性质
苯酚的分子结构中既有苯环,又有羟基,它们相互影响。苯酚具有酸性,能与溴水、浓硝酸等发生取代反应,也能与氢气发生加成反应,苯酚还能与FeCl3溶液发生显色反应(显紫色)。
(1)苯酚的弱酸性
实验步骤:取苯酚浊液加氢氧化钠溶液,会变澄清。将得到的澄清液放人两支试管中,分别加入盐酸和通入二氧化碳气体。
实验现象:澄清液加入盐酸和通入二氧化碳气体后又会变浑浊。
实验结论:苯环对羟基的影响结果是使羟基的活性增强,在水溶液中能电离出H+。
反应方程式: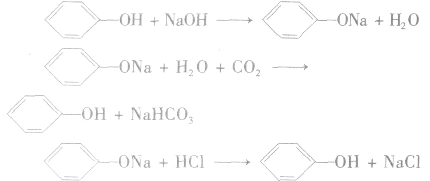
注意:苯酚具有酸性,但是苯酚的酸性极弱,它不能使酸碱指示剂显色,它与碳酸的电离程度的大小为: 因此,苯酚在与碳酸钠溶液反应时,只能生成碳酸氢钠和苯酚钠,而不能生成水和CO2。
因此,苯酚在与碳酸钠溶液反应时,只能生成碳酸氢钠和苯酚钠,而不能生成水和CO2。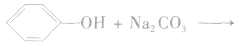
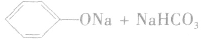
由于苯酚的酸性很弱,因此苯酚钠在水溶液中水解而使溶液显碱性:
相同浓度时,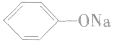 溶液的碱性比
溶液的碱性比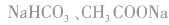 溶液的碱性强。
溶液的碱性强。
(2)苯环上的取代反应
①卤代反应
实验步骤:向少量稀苯酚中加入饱和溴水,观察实验现象。
实验现象:有白色沉淀生成。
实验结论:由于羟基对苯环的影响,使苯环上与羟基处在邻位和对位上的氢原子活性增强,容易被取代。
反应方程式: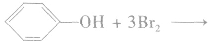
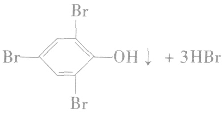
苯酚与溴的反应很灵敏,可用于苯酚的定性检验和定量测定。
注意:2,4,6一三溴苯酚不溶于水,但易溶于苯,若苯中溶有少量苯酚,加浓溴水不会产生白色沉淀,因而用溴水检验不出溶于苯中的苯酚,也不能用溴水来除去苯中混有的少量苯酚(应加NaOH溶液后分液)。
②硝化反应
苯需用混酸进行硝化,而苯酚很容易硝化,与浓硝酸反应即可生成三硝基苯酚。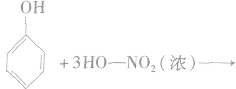
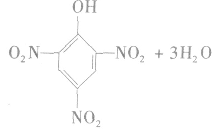
反应生成的2,4,6一三硝基苯酚,俗称苦味酸,可以用作炸药。
(3)苯酚的显色反应苯酚跟FeCl3溶液作用显示紫色,利用这一反应可以检验苯酚的存在。 
(4)氧化反应苯酚晶体在常温下易被空气中的氧气氧化,它也易燃烧,易被酸性KMnO4溶液氧化。
(5)加成反应
苯酚可在苯环上发生加成反应。如:

(6)苯酚与甲醛的缩聚反应
苯酚和甲醛在酸或碱的催化作用下发生反应生成酚醛树脂,反应方程式为: 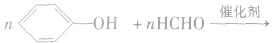
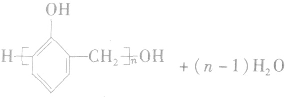
4.苯酚的主要用途
苯酚是一种重要的化工原料,广泛用于制造酚醛树脂、染料、医药、农药等。炼焦工业的废水中常含有酚类物质,这些物质是被控制的水污染物之一,在排放前必须经过处理。
苯酚有毒,但其稀溶液可直接用作防腐剂和消毒剂。
与“下列各项表述中正确的是( )A.由AlO2-与CO32-在溶液中可以...”考查相似的试题有:
- 下列离子方程式中,正确的是( )A.二氧化硫与氢氧化钠溶液反应:B.硫酸与氢氧化钡溶液反应:C.二氧化氮与水反应:D.氧化...
- 下列离子方程式不正确的是A.苯酚钠溶液与二氧化碳反应: 2C6H5O-+ CO2+ H2O = 2C6H5OH + CO32-B.在亚硫酸钡沉淀中加入稀...
- 写出下列反应式,并作简要回答:(1)写化学方程式:①呼吸面具中CO2与过氧化钠反应:______.②工业生产漂白粉:______.③加热...
- 已知HCO3-+OH-==CO32-+H2O,下列各组中两种物质在溶液中的反应,可用同一离子方程式表示的是[ ]A.Cu(OH)2+HCl;Cu(OH)2+CH3C...
- 下列表示对应化学反应的离子方程式正确的是A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2OB.用铜为电极...
- 下列离子方程式正确的是 A.等物质的量的Ba(OH)2与KAl(SO4)2·12H2O溶液混合:3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓...
- 下列离子方程式的书写正确的是( )A.铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑B.NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2...
- 下列反应的离子方程式正确的是电解 A.氢氧化铁溶于氢碘酸中:Fe(OH)3+ 3H+= Fe3++ 3H2OB.用惰性电极电解饱和食盐水:2Cl...
- 为配置NH4+的浓度与Cl-的浓度比为1:1的溶液,可在NH4Cl溶液中加入( )① 适量HCl ② 适量NaCl ③ 适量氨水 ④ 适量NaOHA.①②B...
- A~L是由6种短周期元素组成的物质,各物质之间有如下转化关系:已知:(a) C、E是气体单质,F是日常生活中的常用金属;(b)...