本试题 “某种施用于沙壤土的化肥主要成分由A、B、C、D四种短周期元素组成,它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素的单质在空气中的体积...” 主要考查您对铵盐
原子结构示意图
元素周期表
元素周期律
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 铵盐
- 原子结构示意图
- 元素周期表
- 元素周期律
定义:
铵盐是由铵根离子(NH4+)和酸根离子组成的化合物。铵盐都是晶体,都易溶于水。
铵盐的物理性质和化学性质:
(1)物理性质:铵盐是由铵离子(NH4+)和酸根阴离子组成的化合物,铵盐都是白色晶体,都易溶于水。
(2)铵盐的化学性质:
①受热分解:固态铵盐受热都易分解,根据组成铵盐的酸根阴离子对应的酸的性质的不同,铵盐分解时有以下三种情况:
A. 组成铵盐的酸根阴离子对应的酸是非氧化性的挥发性酸时,则加热时酸与氨气同时挥发,冷却时又重新化合生成铵盐。例如:
 (试管上端又有白色固体附着)。
(试管上端又有白色固体附着)。又如:
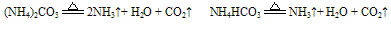
B. 组成铵盐的酸根阴离子对应的酸是难挥发性酸,加热时则只有氨气逸出,酸或酸式盐仍残留在容器中。如:
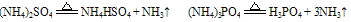
C. 组成铵盐的酸根阴离子对应的酸是氧化性酸,加热时则发生氧化还原反应,无氨气逸出。例如:
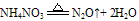
②跟碱反应--铵盐的通性。
固态铵盐+强碱(NaOH、KOH)
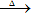 无色、有刺激性气味的气体
无色、有刺激性气味的气体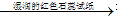 试纸变蓝色。例如:
试纸变蓝色。例如: 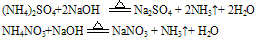
说明:a.若是铵盐溶液与烧碱溶液共热,则可用离子方程式表示为:

b.若反应物为稀溶液且不加热时,则无氨气逸出,用离子方程式表示为:
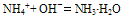
c.若反应物都是固体时,则只能用化学方程式表示。
(3)氮肥的存放和施用.铵盐可用作氮肥.由于铵盐受热易分解,因此在贮存时应密封包装并存放在阴凉通风处;施用氮肥时应埋在土下并及时灌水,以保证肥效。
定义:
圆圈和圆圈内的数字分别表示原子核和核内的质子数,弧线表示电子层,弧线上的数字表示该层的电子数。
表示原子结构的常用图示:
1.原子符号:
2.核外电子分层排布示意图:
3.原子结构示意图:
相对原子质量及近似相对原子质量:
1.几个概念的辨析
| 原子的真实质量 | 原子的真实质量也称绝对质量,是通过精密的实验测得的,原子的真实质量很小,使用极不方便,所以科学上,一般不直接使用原子的真实质量,而使用原子的相对质量—— 相对原子质量 |
| 核素的相对原子质量 | 核素的相对原子质量是指一个核素原子的质量与一个碳-12原子质量的l/12的比值 |
| 元素的相对原子质量 | 元素的相对原子质量是指某元素各种核素的相对原子质量与各核素原子所占的原子个数百分比(丰度)的乘积之和,也就是元素周期表中所给的相对原子质量的数值。一般情况下元素的相对原子质量不为整数 |
| 原子的质量数 | 原子的质量数是指某元素的一种核素原子的核中所含质子数和中子数之和,在实际使用中常代替相对原子质量,所以也叫做近似相对原子质量。需要注意的是元素无质量数 |
2.近似相对原子质量
1.核素的近似相对原子质量,就是核素的质量数。
2.元素的近似相对原子质量,就是按照该元素各种核素的质量数和各种核素原子所占的原子个数百分比算出的平均值。例如,氯元素的近似相对原子质量为:
元素周期表编排原则:
(1)把电子层数相同的各种元素按原子序数递增的顺序从左至右排成横行。
(2)把最外层电子数相同的元素按电子层数递增的顺序由上到下排列成纵行。
注意:①元素周期表是元素周期律的具体表现形式,它反映了元素之间相互联系的规律。
②历史上第一个元素周期表是1869年俄国化学家门捷列夫在前人探索的基础上排成的,他将元素按相对原子质量由小到大依次排列,并将化学性质相似的元素放在一个纵行。
元素周期表的结构:
(1)周期
①周期的含义在元素周期表中,把电子层数相同的元素,按原子序数递增的顺序从左到右排成横行,这样每个横行为一个周期。现在使用的元素周期表有7个横行,即7 个周期。
②周期的划分
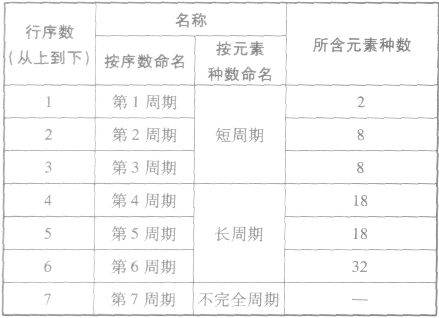
(2)族
①族的含义在周期表中,把不同横行(即周期)中最外层电子数相同的元素,按电子层数递增的顺序由上到下排成纵行,除第8、9、10三个纵行叫做第Ⅷ族外,其余15个纵行,每个纵行为一族。现在使用的元素周期表有18 个纵行,它们被划分为16个族。
②族的划分
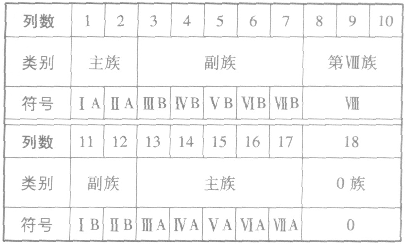
(3)元素周期表中主族元素金属性和非金属性的递变
定义:
元素的性质随原子序数的递增而呈现周期性变化的规律叫元素周期律。
实质:
元素性质随原子序数递增呈现周期性变化是元素原子的核外电子排布周期性变化的必然结果。
元素周期表中主族元素性质递变规律:

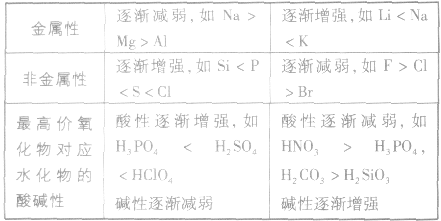
金属性强弱的判断依据:
1.单质跟水或酸反应置换出氢的难易程度(或反应的剧烈程度):反应越容易,说明其金属性越强。
2.最高价氧化物对应水化物的碱性强弱:碱性越强,说明其金属性越强,反之则越弱。
3.金属间的置换反应:依据氧化还原反应的规律,金属甲能从金属乙的盐溶液里置换出乙,说明甲的金属性比乙强。
4.金属活动性顺序按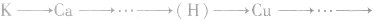 Au顺序,金属性逐渐减弱。
Au顺序,金属性逐渐减弱。
5.元素周期表中,同周期元素从左至右金属性逐渐减弱;同主族元素从上至下金属性逐渐增强。
6.原电池中的正负极:一般情况下,活泼金属作负极。
7.金属阳离子氧化性的强弱:阳离子的氧化性越强.对应金属的金属性就越弱。
非金属性强弱的判断依据:
1.同周期元素,从左到右,随核电荷数的增加,非金属性增强;同主族元素,从上到下,随着陔电荷数的增加,非金属性减弱。
2.最高价氧化物对应水化物的酸性强弱:酸性越强,其元素的非金属性也越强,反之则越弱。
3.气态氢化物的稳定性:稳定性越强,非金属性越强。
4.单质跟氢气化合的难易程度:越易与H2反应,说明其非金属性越强。
5.与盐溶液之间的置换反应:非金属元素甲的单质能从非金属乙的盐溶液中置换出乙,说明甲的非金属性比乙强。如 ,说明溴的非金属性比碘强。
,说明溴的非金属性比碘强。
6.相互化合后的价态:如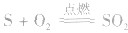 ,说明O 的非金属性强于S。
,说明O 的非金属性强于S。
7.其他:如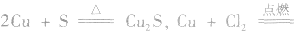 CuCl2,所以C1的非金属性强于S。
CuCl2,所以C1的非金属性强于S。
微粒半径大小的比较方法:
1.同周期元素的微粒
同周期元素的原子或最高价阳离子半径随核电荷数增大而减小(稀有气体元素除外),如半径:Na>Mg >Al,Na+>Mg2+‘>Al3+。
2.同主族元素的微粒
同主族元素的原子或离子半径随核电荷数增大而增大,如半径: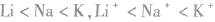
3.电子层结构相同的微粒电子层结构相同(核外电子排布相同)的微粒半径随核电荷数的增加而减小,如半径: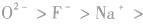
 (上一周期元素形成的阴离子与下一周期元素形成的最高价阳离子有此规律)。
(上一周期元素形成的阴离子与下一周期元素形成的最高价阳离子有此规律)。
4.同种元素形成的微粒同种元素原子形成的微粒半径大小为:阳离子< 中性原子<阴离子;价态越高的微粒半径越小,如半径: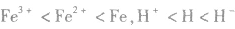 。
。
5.核外电子数和核电荷数都不同的微粒可通过一种参照物进行比较,如比较 的半径大小,可找出与A13+电子数相同,与S同主族的氧元素的阴离子
的半径大小,可找出与A13+电子数相同,与S同主族的氧元素的阴离子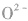 进行比较,半径:
进行比较,半径: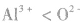 ,且
,且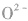
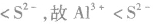
元素周期表中的几项重要规律相等规律:
| 规律 | 内容 |
| 相等规律 | ①周期数:电子层数 ②主族元素原子的最外层电子数=价电子数=主族序数=最高正化合价(F、 0除外) ③最低负价绝对值=8一主族序数(限 ⅣA族~ⅦA族非金属元素) |
| “位、构、性”规律 | |
| 递变规律 | 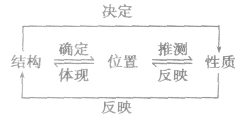 |
| 同周期从左到右,元素的金属性逐渐减弱,非金属性逐渐增强同主族从上到下,元素的金属性逐渐增强,非金属性逐渐减弱 | |
| 奇偶规律 | 在同一主族内,族序数和原子序数、核内质子数、核电荷数、核外电子数、最外层电子数(价电子数)、离子的电荷数、元素的主要正负化合价数等,若一个是偶数,其他的都是偶数,若一个是奇数,其他的都是奇数 |
| 相同电子层结构的规律 | 稀有气体元素的原子与同周期非金属元素的阴离子以及下一周期主族金属元素的阳离子具有相同的电子层结构 |
| 序差规律 | ①同主族相邻元素的原子序数之差与主族序数有关。IA~ⅡA族元素相差原子序数较小的元素所在周期包含的元素种数。ⅢA族~O族元素相差原子序数较大的元素所在周期包含的元素种数。如Na和K的原子序数相差8 (第三周期含8种元素),Cl和Br的原子序数相差18(第四周期含18种元素) ②同周期主族元素(长周期)的原子序数差:两元素分布在过渡元素同侧时,原子序数差=族序数差;两元素分布在过渡元素两侧时,第四或第五周期元素原子序数差=族序数差+10(如第四周期的Ca和Ca相差11),第六、七周期元素原子序数差=族序数差+24(如ⅡA 族的Ba和ⅢA族的Tl相差25) |
| 对角线相似规律 | 周期表中位于对角线位置的元素性质相似,尤以“和Mg、Be和Al最为典型 |
与“某种施用于沙壤土的化肥主要成分由A、B、C、D四种短周期元素...”考查相似的试题有:
- 下列化学用语使用正确的是( ) A.HCN分子的结构式:H-C≡N B.水分子的球棍模型: C.F-离子的结构示意图: D.二氧化碳的电...
- 下图是我们熟悉的元素周期表,请回答下列问题(1)在上面元素周期表中画出金属元素与非金属元素的分界线。(2)在上面元素周...
- 下表是元素周期表的一部分,按要求填空(1)写出下列元素的元素名称⑴ _____ ⑵ _____ ⑾ _______⑿______(2)在这些元素中,最...
- 下列有关化学用语表示正确的是( )A.乙醇的结构式:CH3CH2OHB.乙烯的比例模型C.中子数为20的氯原子: 3720CID.氨气的电...
- 下表列出了A-I九种元素在周期表中的位置(1)这九种元素中,金属性最强的元素是_____________(填元素符号,下同),化学性质...
- (4分)有X、Y两种元素,Y的第三个电子层上有2个电子,X的最外层电子数是其电子层数的3倍,请写出其原子结构示意图:X、 ;Y...
- 下列叙述中,能说明金属M的金属性比金属N的金属性强的是A.M原子的最外层电子数比N原子的最外层电子数少B.常温时,M单质能从...
- 下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题。(1)⑦表...
- 据报道,某些建筑材料会产生放射性同位素222 86Rn,从而对人体造成伤害,该同位素原子的中子数和质子数之差为 ( )A.86B.2...
- A、B两主族元素属于同一周期,它们的原子能以共价键结合成化学式为AB2型分子,A、B元素在周期表中的族序数可能为 ( )A.ⅠA...