本试题 “下列说法中正确的是( )A.不饱和溶液变为饱和溶液溶质质量分数一定变大B.饱和溶液一定为浓溶液,不饱和溶液一定为稀溶液C.物质的溶解能力只受温度影响D....” 主要考查您对溶解
饱和溶液,不饱和溶液
气体溶解度
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶解
- 饱和溶液,不饱和溶液
- 气体溶解度
溶解定义:
广义上说,超过两种以上物质混合而成为一个分子状态的均匀相的过程称为溶解。而狭义的溶解指的是一种液体对于固体/液体/或气体产生化学反应使其成为分子状态的均匀相的过程称为溶解。一种物质(溶质)分散于另一种物质(溶剂)中成为溶液的过程。如食盐或蔗糖溶解于水而成水溶液。溶液并不一定为液体,可以是固体、液体、气体。比如均匀的合金和空气都可以称为溶液。当两种物质互溶时,一般把质量大的物质称为溶剂(如有水在其中,一般习惯将水称为溶剂)。
溶解过程:
物质溶解于水,通常经过两个过程:一种是溶质分子(或离子)的扩散过程,这种过程为物理过程,需要吸收热量;另一种是溶质分子(或离子)和溶剂(水)分子作用,形成溶剂(水合)分子(或水合离子)的过程,这种过程是化学过程,放出热量。当放出的热量大于吸收的热量时,溶液温度就会升高,如浓硫酸、氢氧化钠等;当放出的热量小于吸收的热量时,溶液温度就会降低,如硝酸铵等;当放出的热量等于吸收的热量时,溶液温度不变,如盐、蔗糖。
固体、液体及气体溶解的对比分析:
(1)固体溶解
固体溶解时,常需要粉碎,加热,震荡,搅拌等方法加速溶解。

(2)液体溶解
一般液体溶解时,将液体加水搅拌均匀。
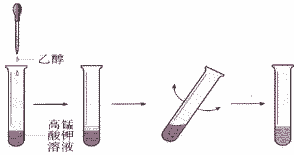
(3)气体溶解
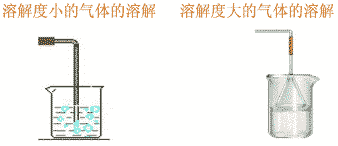
气体溶解时,对于溶解度小的气体要把导管插入水中,极易溶于水的气体,应在导管末端插一倒置的漏斗,漏斗边缘接触水。
溶解性应用:
1、是指物质在溶剂里溶解能力的大小。
2、溶解性是物理性质,溶解是物理变化。
3、溶解性是由20℃时某物质的溶解度决定的。(固体)
4、利用溶解性可有以下应用:
(1)判断气体收集方法
可溶(易溶)于水的气体不能用排水取气法。
如:CO2而H2,O2溶解性不好,可用排水取气法。
(2)判断混合物分离方法
两种物质在水中溶解性明显不同时,可用过滤法分离。
如:KNO3(易溶)与CaCO3(难溶)可用过滤法分离
而C与MnO2二者均不溶NaClKNO3均易溶,都不能用过滤法分离。
溶解度算法=溶质质量/溶剂质量(通常为水)
单位: g/100g水。
广义上说,超过两种以上物质混合而成为一个分子状态的均匀相的过程称为溶解。而狭义的溶解指的是一种液体对于固体/液体/或气体产生化学反应使其成为分子状态的均匀相的过程称为溶解。一种物质(溶质)分散于另一种物质(溶剂)中成为溶液的过程。如食盐或蔗糖溶解于水而成水溶液。溶液并不一定为液体,可以是固体、液体、气体。比如均匀的合金和空气都可以称为溶液。当两种物质互溶时,一般把质量大的物质称为溶剂(如有水在其中,一般习惯将水称为溶剂)。
溶解过程:
物质溶解于水,通常经过两个过程:一种是溶质分子(或离子)的扩散过程,这种过程为物理过程,需要吸收热量;另一种是溶质分子(或离子)和溶剂(水)分子作用,形成溶剂(水合)分子(或水合离子)的过程,这种过程是化学过程,放出热量。当放出的热量大于吸收的热量时,溶液温度就会升高,如浓硫酸、氢氧化钠等;当放出的热量小于吸收的热量时,溶液温度就会降低,如硝酸铵等;当放出的热量等于吸收的热量时,溶液温度不变,如盐、蔗糖。
固体、液体及气体溶解的对比分析:
(1)固体溶解
固体溶解时,常需要粉碎,加热,震荡,搅拌等方法加速溶解。

(2)液体溶解
一般液体溶解时,将液体加水搅拌均匀。

(3)气体溶解
气体溶解时,对于溶解度小的气体要把导管插入水中,极易溶于水的气体,应在导管末端插一倒置的漏斗,漏斗边缘接触水。

溶解性应用:
1、是指物质在溶剂里溶解能力的大小。
2、溶解性是物理性质,溶解是物理变化。
3、溶解性是由20℃时某物质的溶解度决定的。(固体)
| (20℃) | 难溶(不溶) | 微溶 | 可溶 | 易溶 |
| <0.01g | 0.01g~1g | 1 g~10g | >10g |
4、利用溶解性可有以下应用:
(1)判断气体收集方法
可溶(易溶)于水的气体不能用排水取气法。
如:CO2而H2,O2溶解性不好,可用排水取气法。
(2)判断混合物分离方法
两种物质在水中溶解性明显不同时,可用过滤法分离。
如:KNO3(易溶)与CaCO3(难溶)可用过滤法分离
而C与MnO2二者均不溶NaClKNO3均易溶,都不能用过滤法分离。
溶解度算法=溶质质量/溶剂质量(通常为水)
单位: g/100g水。
饱和溶液和不饱和溶液的概念:
①饱和溶液:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,
叫做这种溶质的饱和溶液
②不饱和溶液:在一定温度下,在一定量的溶剂里,还能再继续溶解某种溶质的溶液,
叫做这种溶质的不饱和溶液
饱和溶液与不饱和溶液的相互转化方法:
(1)对于大多数固体:在一定量的水中溶解的最大量随温度升高而增大
饱和溶液 不饱和溶液
不饱和溶液
(2)对于Ca(OH)2:在一定量的水中溶解的最大量随温度升高而减少
饱和石灰水 不饱和石灰水
不饱和石灰水
概念的理解:
(1)溶液的饱和与不饱和跟温度和溶质的量的多少有关系。因此在谈饱和溶液与不饱和溶液时,一定要强调“在一定温度下”和“一定量的溶剂里”,否则就无意义。
(2)一种溶质的饱和溶液仍然可以溶解其他溶质。如氯化钠的饱和溶液中仍可溶解蔗糖。
(3)有些物质能与水以任意比例互溶,不能形成饱和溶液,如:酒精没有饱和溶液。
饱和溶液和不饱和溶液的相互转化:
一般,对饱和溶液与不饱和溶液相互转化过程中溶液组成的分析:
①饱和溶液 不饱和溶液(或不饱和溶液
不饱和溶液(或不饱和溶液 饱和溶液。不发生结晶的前提下)
饱和溶液。不发生结晶的前提下)
溶液中溶质、溶剂、溶液的质量不变,溶质质量分数不变。
②不饱和溶液 饱和溶液
饱和溶液
溶液的溶剂质量不变,溶质、溶液、溶质质量分数均增大。
③不饱和溶液 饱和溶液(不发生结晶的前提下)
饱和溶液(不发生结晶的前提下)
溶质质量不变,溶剂、溶液质量变小,溶质质量分数变大。
④饱和溶液 不饱和溶液
不饱和溶液
溶剂、溶液质量增大,溶质质量不变,溶质质量分数变小
判断溶液是否饱和的方法:
①观察法:当溶液底部有剩余溶质存在,且溶质的量不再减少时,表明溶液已饱和。
②实验法:当溶液底部无剩余溶质存在时,可向该溶液中加入少量该溶质,搅拌后,若能溶解或溶解一部分,表明该溶液不饱和;若不能溶解,则表明该溶液已饱和。
浓溶液,稀溶液与饱和溶液,不饱和溶液的关系:
为粗略地表示溶液中溶质含量的多少,常把溶液分为浓溶液和稀溶液。在一定量的溶液里含溶质的量相对较多的是浓溶液,含溶质的量相对较少的是稀溶液。它们与饱和溶液、不饱和溶液的关系如下图所示:
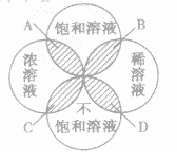 A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液
A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液
(1)溶液的饱和与不饱和与溶液的浓和稀没有必然关系。
(2)饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
(3)在一定温度下,同种溶剂、同种溶质的饱和溶液要比其不饱和溶液浓度大。
①饱和溶液:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,
叫做这种溶质的饱和溶液
②不饱和溶液:在一定温度下,在一定量的溶剂里,还能再继续溶解某种溶质的溶液,
叫做这种溶质的不饱和溶液
饱和溶液与不饱和溶液的相互转化方法:
(1)对于大多数固体:在一定量的水中溶解的最大量随温度升高而增大
饱和溶液
 不饱和溶液
不饱和溶液(2)对于Ca(OH)2:在一定量的水中溶解的最大量随温度升高而减少
饱和石灰水
 不饱和石灰水
不饱和石灰水概念的理解:
(1)溶液的饱和与不饱和跟温度和溶质的量的多少有关系。因此在谈饱和溶液与不饱和溶液时,一定要强调“在一定温度下”和“一定量的溶剂里”,否则就无意义。
(2)一种溶质的饱和溶液仍然可以溶解其他溶质。如氯化钠的饱和溶液中仍可溶解蔗糖。
(3)有些物质能与水以任意比例互溶,不能形成饱和溶液,如:酒精没有饱和溶液。
饱和溶液和不饱和溶液的相互转化:
一般,对饱和溶液与不饱和溶液相互转化过程中溶液组成的分析:
①饱和溶液
 不饱和溶液(或不饱和溶液
不饱和溶液(或不饱和溶液 饱和溶液。不发生结晶的前提下)
饱和溶液。不发生结晶的前提下)溶液中溶质、溶剂、溶液的质量不变,溶质质量分数不变。
②不饱和溶液
 饱和溶液
饱和溶液溶液的溶剂质量不变,溶质、溶液、溶质质量分数均增大。
③不饱和溶液
 饱和溶液(不发生结晶的前提下)
饱和溶液(不发生结晶的前提下)溶质质量不变,溶剂、溶液质量变小,溶质质量分数变大。
④饱和溶液
 不饱和溶液
不饱和溶液溶剂、溶液质量增大,溶质质量不变,溶质质量分数变小
判断溶液是否饱和的方法:
①观察法:当溶液底部有剩余溶质存在,且溶质的量不再减少时,表明溶液已饱和。
②实验法:当溶液底部无剩余溶质存在时,可向该溶液中加入少量该溶质,搅拌后,若能溶解或溶解一部分,表明该溶液不饱和;若不能溶解,则表明该溶液已饱和。
浓溶液,稀溶液与饱和溶液,不饱和溶液的关系:
为粗略地表示溶液中溶质含量的多少,常把溶液分为浓溶液和稀溶液。在一定量的溶液里含溶质的量相对较多的是浓溶液,含溶质的量相对较少的是稀溶液。它们与饱和溶液、不饱和溶液的关系如下图所示:
 A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液
A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液(1)溶液的饱和与不饱和与溶液的浓和稀没有必然关系。
(2)饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
(3)在一定温度下,同种溶剂、同种溶质的饱和溶液要比其不饱和溶液浓度大。
概念:
气体的溶解度是指在压强为101kPa和一定温度时,气体溶解在3体积水里达到饱和状态时的气体体积。如氮气在压强为101kPa和温度为0℃ 时,1体积水里最多能溶解0.024体积氮气,则在0℃ 时,氮气的溶解度为0.024。
影响气体溶解度的因素:
①压强:气体的溶解度随着压强的增大而增大,随若压强的减小而减小。
②温度:气体的溶解度随着温度的升高而减小,随着温度的降低而增大。
应用气体溶解度的知识来解释的现象:
①夏天打开汽水瓶盖时,压强减小,气体的溶解度减小,会有大量气泡冒出。
②喝汽水后会打隔,是因为汽水到胃中后,温度升高、气体的溶解度减小。
③养鱼池中放几个水泵,把水喷向空中,增大与氧气的接触面积,增加水中氧气的溶解量。
④不能用煮拂后的凉开水养鱼,因为温度升高,水巾溶解的氧气减少,因而凉开水中几乎不含氧气。
气体的溶解度是指在压强为101kPa和一定温度时,气体溶解在3体积水里达到饱和状态时的气体体积。如氮气在压强为101kPa和温度为0℃ 时,1体积水里最多能溶解0.024体积氮气,则在0℃ 时,氮气的溶解度为0.024。
影响气体溶解度的因素:
①压强:气体的溶解度随着压强的增大而增大,随若压强的减小而减小。
②温度:气体的溶解度随着温度的升高而减小,随着温度的降低而增大。
应用气体溶解度的知识来解释的现象:
①夏天打开汽水瓶盖时,压强减小,气体的溶解度减小,会有大量气泡冒出。
②喝汽水后会打隔,是因为汽水到胃中后,温度升高、气体的溶解度减小。
③养鱼池中放几个水泵,把水喷向空中,增大与氧气的接触面积,增加水中氧气的溶解量。
④不能用煮拂后的凉开水养鱼,因为温度升高,水巾溶解的氧气减少,因而凉开水中几乎不含氧气。
发现相似题
与“下列说法中正确的是( )A.不饱和溶液变为饱和溶液溶质质量...”考查相似的试题有:
- 用“不饱和”和“饱和”填空,20℃时,在盛10克水的烧杯中加入3克某物质,充分溶解后还有1克剩余,则所得溶液是该物质在20℃时的___...
- 下图是A、B、C三种物质的溶解曲线回答下列问题:(1)温度低于t1℃时,这三种物质的溶解度由大到小的顺序为_____________;(2)点...
- (1)如图为a、b两种物质的溶解度曲线.t℃时,a、b两种物质的饱和溶液中溶液质的质量分数的大小关系是______;(2)温度高于t...
- 如图所示是甲、乙、丙三种物质的溶解度曲线,当他们接近饱和时,可以分别通过加溶质、蒸发溶剂、升温等方法变为饱和溶液的是...
- 下列说法正确的是[ ]A.相同温度下,饱和溶液一定比不饱和溶液浓B.浓溶液一定是饱和溶液C.不饱和溶液降温一定会变成饱和溶...
- 有A、B、C、D四个烧杯中分别盛有质量相等的同种溶剂,在相同的温度下,向四个小烧杯中分别加入200g、150g、100g、50g某溶质,...
- (3分)如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:(1)P点的含义是 。(2)t1℃时30g a物质...
- 下图是a、b、c三种物质的溶解度曲线,下列有关说法正确的是A.t2℃时a、b、c的溶解度由大到小的顺序是a>b>cB.将a物质从溶液中...
- 下列说法不正确的是( )A.厨房洗涤剂清洁油污后形成溶液B.用硬水洗衣服不如用软水洗得干净C.硝酸铵溶于水制得的冰袋可用...
- 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )A.t1℃时,甲、乙两种物质的饱和溶液中溶质质量...