本试题 “2011年5月食品塑化剂事件引起社会的高度关注.常用塑化剂的学名“邻苯二甲酸而(2-乙基己)酯”,化学式为C24H38O4,它是一种无色透明的液体,有特殊气味,不溶...” 主要考查您对食品安全
有机化合物和无机化合物
物质组成元素的质量比
元素的定义
物理性质和化学性质的区别和应用
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 食品安全
- 有机化合物和无机化合物
- 物质组成元素的质量比
- 元素的定义
- 物理性质和化学性质的区别和应用
食品安全(food safety)指食品无毒、无害,符合应当有的营养要求,对人体健康不造成任何急性、亚急性或者慢性危害。
根据世界卫生组织的定义,食品安全是“食物中有毒、有害物质对人体健康影响的公共卫生问题”。
食品安全也是一门专门探讨在食品加工、存储、销售等过程中确保食品卫生及食用安全,降低疾病隐患,防范食物中毒的一个跨学科领域。
食品污染的类型食品安全问题越来越得到人们的重视,常见的食品污染有如下几类:
(1)微量元素中有一些有害元素,在人体内积累会影响身体健康,如铝、铅、汞;
(2)过量食用食品添加剂或使用非食品添加剂,如过量使用防腐剂、面粉增白剂、色素、香精,用工业用盐亚硝酸钠加工食品,添加苏丹红等;
(3)食品制作过程受到污染,如使用工业双氧水(漂白)、甲醛泡发水产品、用硫黄熏蒸食品等;
(4)食用变质原料或食用已被污染的原料制作的食品,如用霉变大米等加工食品。
安全购买食品的注意事项:
(1)注意看经营者是否有营、业执照,其主体资格是否合法。
(2)注意看食品包装标识是否齐全.注意食品外包装是否标明商品品称、配料表、净含量、厂名、厂址、电话、生产日期、保质期、产品标准号等内容。
(3)注意看食品的生产日期或失效日期,注意食品是否超过保质期。
(4)看产品标签,注意区分认证标志。
(5)看食品的色泽,不要被外观过于鲜艳、好看的食品迷惑。
(6)看散装食品经营者的卫生状况,注意有无健康证、卫生合格证等相关证照,有无防蝇、防尘设施.
(7)看食品价格,注意同类同种食品的市场比价,理性购买“打折”“低价”“促销”食品。
(8)购买肉制品、腌制品最好到规范的市场、“放心店”购买,慎购游商销售的食品。
(9)妥善保管好购物凭据及相关依据,以便发生消费争议时能够提供维权依据
食品添加剂的正确使用原则:
为了确保将食品添加剂正确地使用到食品中,一般来说,其使用应遵循以下原则:
(1)经食品毒理学霞全性评价证明,在其使用限量内长期使用对人安全无害。
(2)不影响食品自身的感官性状和理化指标,对营养成分无破坏作用。
(3)食品添加剂应有中华人民共和国卫生部颁布并批准执行的使用卫生标准和质量标准。
(4)食品添加剂在应用中应有明确的检验方法。
(5)使用食品添加剂不得以掩盖食品腐败变质或以掺杂、掺假、伪造为目的。
(6)不得经营和使用无卫生许可证、无产品检验合格及污染变质的食品添加剂。
(7)食品添加剂在达到一定使用目的后,能够经过加工、烹调或储存而被破坏或排除,不摄入人体则更为安全。
对人体有害的几种添加剂:
(1)吊白块吊白块是甲醛合次硫酸氢钠的俗称,化学式为 NaHSO2·CH2O·2H2O。为白色半透明小块,易溶于水,有漂白作用,是常用的工业漂白剂。但不能作食品漂白添加剂,不法分子用于食品增白,造成了很大的危害。吊白块水溶液在60℃以上就开始分解出有害物质,120℃下分解产生甲醛、二氧化硫和硫化氢等有毒气体。食用了用吊白块漂白过的白糖、粉丝、米线、面粉、腐竹后,可能对人体的某些酶有损害,从而造成中毒者肺、肝、肾器官的损害。
(2)苏丹红苏丹红是一种人工合成的红色染料,被广泛用于溶剂、油、蜡、汽油的增色,以及鞋、地板的增光。苏丹红的化学成分巾含有一种叫萘的化合物,该化合物具有偶氮结构,它具有致癌性,对人体的肝、肾器官具有明显的毒性。我国禁止将其使用于食品中。但不法食品生产企业违规在食品中加入苏丹红,如“苏丹红鸭蛋”。
(3)三聚氰胺 2008年9月,中国爆发三鹿婴幼儿奶粉事件,其原因是奶粉中含有三聚氰胺。三聚氰胺的化学式为C3H6N6,俗称蛋白精,是一种有机化合物,被用作化工原料。三聚氰胺对身体有害,不可用于食品加工和作食品添加剂。牛奶和奶粉中添加三聚氰胺,主要是因为它能冒充蛋白质,能提高奶粉中的含氮量。
(4)瘦肉精 “瘦肉精”学名盐酸克伦特罗,是一种平喘药,又称克喘素,本来是用来治疗人的哮喘病,有松弛支气管平滑肌的作用。该药可以增加蛋白质的合成,添加在猪饲料中可以使猪的肥肉明显减少,瘦肉增加,所以有人干脆就称它为“瘦肉精”。 “瘦肉精”进入猪体内后具有分散快、消除慢的特点,其化学性质稳定,加热到172℃时才能分解,一般的加热方法不能将其破坏。“瘦肉精”毒性较强,医学研究表明“瘦肉精”吸收快,人或动物服后15—20分钟即起作用,2—3小时血浆浓度达到峰值,作用维持时间长,一般用20微克就可以出现症状。人食用过量后会出现两手发抖、心慌、头晕、头痛、呕吐、腹泻等不良反应,严重的会危及生命,尤其对高血压、心脏病、甲亢、前列腺肥大等患者,其危害性更为严重。长期食用,有可能导致染色体畸变,会诱发恶性肿瘤。它是一种严重危害畜牧业健康发展和畜产品安全的“毒品”。猪在吃了“瘦肉精”后,其毒性主要积蓄在猪肝、猪肺等处。人在吃了烧熟的猪肝、猪肺后,会出现中毒症状。
有毒物质——甲醛:
甲醛的化学式为HCHO(或CH2O),是一种无色、有强烈刺激性气味的气体。易溶于水、乙醇。35%~ 40%的甲醛水溶液叫做福尔马林,具有防腐乐菌性能。可用来浸制标本,但不能用来作食品的防腐剂。甲醛是一种重要的化工原料,主要用于塑料工业、合成纤维及皮革工业、医药、染料等。甲醛具有毒性,能与蛋门质结合,使蛋白质发生变性。体表接触或吸人岛浓度甲醛,都会严重危害人体健康一在家庭生活中,装修房屋使用的黏合剂中含有甲醛。
根据世界卫生组织的定义,食品安全是“食物中有毒、有害物质对人体健康影响的公共卫生问题”。
食品安全也是一门专门探讨在食品加工、存储、销售等过程中确保食品卫生及食用安全,降低疾病隐患,防范食物中毒的一个跨学科领域。
食品污染的类型食品安全问题越来越得到人们的重视,常见的食品污染有如下几类:
(1)微量元素中有一些有害元素,在人体内积累会影响身体健康,如铝、铅、汞;
(2)过量食用食品添加剂或使用非食品添加剂,如过量使用防腐剂、面粉增白剂、色素、香精,用工业用盐亚硝酸钠加工食品,添加苏丹红等;
(3)食品制作过程受到污染,如使用工业双氧水(漂白)、甲醛泡发水产品、用硫黄熏蒸食品等;
(4)食用变质原料或食用已被污染的原料制作的食品,如用霉变大米等加工食品。
安全购买食品的注意事项:
(1)注意看经营者是否有营、业执照,其主体资格是否合法。
(2)注意看食品包装标识是否齐全.注意食品外包装是否标明商品品称、配料表、净含量、厂名、厂址、电话、生产日期、保质期、产品标准号等内容。
(3)注意看食品的生产日期或失效日期,注意食品是否超过保质期。
(4)看产品标签,注意区分认证标志。
(5)看食品的色泽,不要被外观过于鲜艳、好看的食品迷惑。
(6)看散装食品经营者的卫生状况,注意有无健康证、卫生合格证等相关证照,有无防蝇、防尘设施.
(7)看食品价格,注意同类同种食品的市场比价,理性购买“打折”“低价”“促销”食品。
(8)购买肉制品、腌制品最好到规范的市场、“放心店”购买,慎购游商销售的食品。
(9)妥善保管好购物凭据及相关依据,以便发生消费争议时能够提供维权依据
食品添加剂的正确使用原则:
为了确保将食品添加剂正确地使用到食品中,一般来说,其使用应遵循以下原则:
(1)经食品毒理学霞全性评价证明,在其使用限量内长期使用对人安全无害。
(2)不影响食品自身的感官性状和理化指标,对营养成分无破坏作用。
(3)食品添加剂应有中华人民共和国卫生部颁布并批准执行的使用卫生标准和质量标准。
(4)食品添加剂在应用中应有明确的检验方法。
(5)使用食品添加剂不得以掩盖食品腐败变质或以掺杂、掺假、伪造为目的。
(6)不得经营和使用无卫生许可证、无产品检验合格及污染变质的食品添加剂。
(7)食品添加剂在达到一定使用目的后,能够经过加工、烹调或储存而被破坏或排除,不摄入人体则更为安全。
对人体有害的几种添加剂:
(1)吊白块吊白块是甲醛合次硫酸氢钠的俗称,化学式为 NaHSO2·CH2O·2H2O。为白色半透明小块,易溶于水,有漂白作用,是常用的工业漂白剂。但不能作食品漂白添加剂,不法分子用于食品增白,造成了很大的危害。吊白块水溶液在60℃以上就开始分解出有害物质,120℃下分解产生甲醛、二氧化硫和硫化氢等有毒气体。食用了用吊白块漂白过的白糖、粉丝、米线、面粉、腐竹后,可能对人体的某些酶有损害,从而造成中毒者肺、肝、肾器官的损害。
(2)苏丹红苏丹红是一种人工合成的红色染料,被广泛用于溶剂、油、蜡、汽油的增色,以及鞋、地板的增光。苏丹红的化学成分巾含有一种叫萘的化合物,该化合物具有偶氮结构,它具有致癌性,对人体的肝、肾器官具有明显的毒性。我国禁止将其使用于食品中。但不法食品生产企业违规在食品中加入苏丹红,如“苏丹红鸭蛋”。
(3)三聚氰胺 2008年9月,中国爆发三鹿婴幼儿奶粉事件,其原因是奶粉中含有三聚氰胺。三聚氰胺的化学式为C3H6N6,俗称蛋白精,是一种有机化合物,被用作化工原料。三聚氰胺对身体有害,不可用于食品加工和作食品添加剂。牛奶和奶粉中添加三聚氰胺,主要是因为它能冒充蛋白质,能提高奶粉中的含氮量。
(4)瘦肉精 “瘦肉精”学名盐酸克伦特罗,是一种平喘药,又称克喘素,本来是用来治疗人的哮喘病,有松弛支气管平滑肌的作用。该药可以增加蛋白质的合成,添加在猪饲料中可以使猪的肥肉明显减少,瘦肉增加,所以有人干脆就称它为“瘦肉精”。 “瘦肉精”进入猪体内后具有分散快、消除慢的特点,其化学性质稳定,加热到172℃时才能分解,一般的加热方法不能将其破坏。“瘦肉精”毒性较强,医学研究表明“瘦肉精”吸收快,人或动物服后15—20分钟即起作用,2—3小时血浆浓度达到峰值,作用维持时间长,一般用20微克就可以出现症状。人食用过量后会出现两手发抖、心慌、头晕、头痛、呕吐、腹泻等不良反应,严重的会危及生命,尤其对高血压、心脏病、甲亢、前列腺肥大等患者,其危害性更为严重。长期食用,有可能导致染色体畸变,会诱发恶性肿瘤。它是一种严重危害畜牧业健康发展和畜产品安全的“毒品”。猪在吃了“瘦肉精”后,其毒性主要积蓄在猪肝、猪肺等处。人在吃了烧熟的猪肝、猪肺后,会出现中毒症状。
有毒物质——甲醛:
甲醛的化学式为HCHO(或CH2O),是一种无色、有强烈刺激性气味的气体。易溶于水、乙醇。35%~ 40%的甲醛水溶液叫做福尔马林,具有防腐乐菌性能。可用来浸制标本,但不能用来作食品的防腐剂。甲醛是一种重要的化工原料,主要用于塑料工业、合成纤维及皮革工业、医药、染料等。甲醛具有毒性,能与蛋门质结合,使蛋白质发生变性。体表接触或吸人岛浓度甲醛,都会严重危害人体健康一在家庭生活中,装修房屋使用的黏合剂中含有甲醛。
有机化合物:
(1)概念:通常人们将含有碳元素的化合物称为有机化合物,简称有机物,如甲烷、乙醇、葡萄糖、淀粉等。
(2)组成和结构:有机物都含碳元素,多数含有氢元素,可能还含有氧、氮、氯、硫、磷等元素。有机物中碳原子不仅可以和H,O,Cl,,N等原子直接结合,而且碳原子之间也可以互相连接成链状或环状。原子的排列方式不同,形成有机物的结构就不同,所表现出来的性质也不同。
(3)特点:大多数有机化合物都难溶于水,易溶于有机溶剂,大多数有机化合物受热易分解,且容易燃烧,燃烧产物有CO2和水;绝大多数有机化合物不易导电、熔点低。
(4)分类:
①有机物小分子:相对分了质量较小,如乙醇,甲烷、葡萄糖等。
②有机高分子化合物:简称有机高分子,其相对分子质量比较大,从几万到几十万,甚至高达几百万或更高,如淀粉、蛋白质等。
无机化合物:
(1)概念:无机化合物简称无机物,通常指不含碳元素的化合物,但少数含碳元素的化合物,如CO,CO2, H2CO3,CaCO3等,不具有有机化合物的特点,归在无机化合物中。
(2)分类:无机化合物根据元素组成及在水中离解成的粒子特点分为氧化物、酸、碱,盐。
有机化合物与无机化合物的主要区别:
概念的理解:
像NaCl、H2SO4和NaOH等不含碳元素的化合物称为无机化合物,而少数含碳元素的化合物,如CO,CO2和CaCO3等虽然含有碳元素,但具有无机化合物的特点,也把它们看作无机化合物。有机物一定含有碳元素,但含有碳元素的化合物不一定是有机物。含有碳元素但不属于有机物的化合物主要包括: 碳的氧化物、碳酸、碳酸盐和碳酸氢盐。
(1)概念:通常人们将含有碳元素的化合物称为有机化合物,简称有机物,如甲烷、乙醇、葡萄糖、淀粉等。
(2)组成和结构:有机物都含碳元素,多数含有氢元素,可能还含有氧、氮、氯、硫、磷等元素。有机物中碳原子不仅可以和H,O,Cl,,N等原子直接结合,而且碳原子之间也可以互相连接成链状或环状。原子的排列方式不同,形成有机物的结构就不同,所表现出来的性质也不同。
(3)特点:大多数有机化合物都难溶于水,易溶于有机溶剂,大多数有机化合物受热易分解,且容易燃烧,燃烧产物有CO2和水;绝大多数有机化合物不易导电、熔点低。
(4)分类:
①有机物小分子:相对分了质量较小,如乙醇,甲烷、葡萄糖等。
②有机高分子化合物:简称有机高分子,其相对分子质量比较大,从几万到几十万,甚至高达几百万或更高,如淀粉、蛋白质等。
无机化合物:
(1)概念:无机化合物简称无机物,通常指不含碳元素的化合物,但少数含碳元素的化合物,如CO,CO2, H2CO3,CaCO3等,不具有有机化合物的特点,归在无机化合物中。
(2)分类:无机化合物根据元素组成及在水中离解成的粒子特点分为氧化物、酸、碱,盐。
氧化物,酸,碱,盐的比较:
| 物质类别 | 概念 | 分类 |
| 氧化物 | 由两种元素组成,期中一种是氧元素 | 金属氧化物:由金属元素与氧元素组成,如MgO,Fe2O3等 非金属氧化物:由非金属元素与氧元素组成,如CO2、SO2、H2O等 |
| 酸 | 能离解成氢离子和酸根离子的化合物 | 含氧酸:如H2SO4、H2CO3、HNO3等无氧酸:如HCl,H2S等 |
| 碱 | 由金属离子和氢氧根离子构成的化合物 | 可溶性碱:如NaOH,Ca(OH)2等不溶性碱:如Mg(OH)2、 Fe(OH)3等 |
| 盐 | 由金属离子(或铵根离子)和酸根离子构成的化合物 | 正盐:如NaCl、NH4Cl、Na2CO3,仅由金属离子或钱根离子和酸根离子两部分组成酸式盐:如NaHCO3、NH4HCO3,由金属离子或铵根离子、酸式酸根离子构成碱式盐;如Cu2(OH)2CO3,由金属离子、酸根离子和氢氧根离子构成 |
有机化合物与无机化合物的主要区别:
| 有机化合物 | 无机化合物 | |
| 溶解性 | 多数不溶于水。易溶于有机溶剂 | 有些溶于水而不溶于有机溶剂 |
| 耐热性 | 多数不耐热。熔点较低,一般在400℃ 以下 | 多数耐热,难熔化,熔点一般比较高 |
| 可燃性 | 多数可以燃烧 | 多数不能燃烧 |
概念的理解:
像NaCl、H2SO4和NaOH等不含碳元素的化合物称为无机化合物,而少数含碳元素的化合物,如CO,CO2和CaCO3等虽然含有碳元素,但具有无机化合物的特点,也把它们看作无机化合物。有机物一定含有碳元素,但含有碳元素的化合物不一定是有机物。含有碳元素但不属于有机物的化合物主要包括: 碳的氧化物、碳酸、碳酸盐和碳酸氢盐。
定义:
化合物里各元素的质量比是原子个数与相对原子质量的乘积之比。即各元素原子的相对原子质量总和之比。计算的关键在于正确判断出各元素的原子总数。
公式:
各元素的质量比=各元素相对原子质量与相应原子个数的乘积之比。如化学式为AmBn的物质中,A、B两元素的质量比 =(A的相对原子质量×m):(B的相对原子质量×n)。
对概念公式的理解:
(1)元素是宏观概念,只讲种类,不讲个数。用元素符号表示时,7C素符号前后都不能写数字,如计算四氧化三铁(Fe3O4)中铁元素和氧元素的质量比时不能写成3Fe:4O
(2)在化学式中,原子个数比等于元素的质量除以其相对原子质量之比。如AmBn中A,B两元素的质量比为M:N,则化学式中A,B两元素的原子个数比m:n=
(3)当化学式中含有多种元素时,根据化学式可以计算出全部元素的质量比,也可以计算出其中某几种元素的质量比。
化学式中元素质量比的变式运算:
在AmBn中元素A,B的质量比等于各元素的相对原子质m与原子个数的乘积比,即A,B元素质量比= (A的相对原子质量×m):(B的相对原子质量×n),根据元素质量比的变形运算主要有:
(1)根据某化合物中元素的质最比求化学式根据化合物中元素的质量比(或元素的质量分数比)求化学式,其方法是通过元素的相对原子质量来推断化学式。通过组成元素质量比或元素的质量分数进行分式变换,转换成原子个数(比),推测化学式。
(2)根据某化合物中元素的质量比确定元素的化合价已知某化合物中元素的质量比确定某元素的化合价,可通过元素的质量比及元素的相对原子质量推断化学式中元素的原子个数之比,再根据化合物中正负化合价代数和为零的原则确定元素的化合价。
(3)根据元素的质量比确定元素的相对原子质量
化合物中元素的质量比等于相对原子质量与原子个数的乘积比,利用元素的质量比及化合物中各原子的个数即可求出元素的相对原子质量。相对原子质量之比等于元素的质量除以其原子个数所得的数值之比。
(4)物质的质量比与分子个数比之间的换算:
换算关系:物质的质量比 分子个数比、如SO3、SO2、O2三种物质的质量比为5:4:2,则SO3、SO2、O2的分子个数比为
分子个数比、如SO3、SO2、O2三种物质的质量比为5:4:2,则SO3、SO2、O2的分子个数比为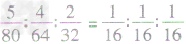 =1:1:1
=1:1:1
利用化学式变形求物质的质量比:
例:含有相同质量铁元素的Fe2O3和Fe3O4的质量比是多少?
解析:设含有相同质量铁元素的Fe2O3和Fe3O4的质量分别为x,y,为了使两者含铁元素的质量相等,可以将它们的化学式变形为铁原子数目相等的式子:
Fe2O3→Fe6O9 Fe3O4→Fe6O8
480 464
x y
x:y=480:464=30:29
答案:30:29
化合物里各元素的质量比是原子个数与相对原子质量的乘积之比。即各元素原子的相对原子质量总和之比。计算的关键在于正确判断出各元素的原子总数。
公式:
各元素的质量比=各元素相对原子质量与相应原子个数的乘积之比。如化学式为AmBn的物质中,A、B两元素的质量比 =(A的相对原子质量×m):(B的相对原子质量×n)。
对概念公式的理解:
(1)元素是宏观概念,只讲种类,不讲个数。用元素符号表示时,7C素符号前后都不能写数字,如计算四氧化三铁(Fe3O4)中铁元素和氧元素的质量比时不能写成3Fe:4O
(2)在化学式中,原子个数比等于元素的质量除以其相对原子质量之比。如AmBn中A,B两元素的质量比为M:N,则化学式中A,B两元素的原子个数比m:n=

(3)当化学式中含有多种元素时,根据化学式可以计算出全部元素的质量比,也可以计算出其中某几种元素的质量比。
化学式中元素质量比的变式运算:
在AmBn中元素A,B的质量比等于各元素的相对原子质m与原子个数的乘积比,即A,B元素质量比= (A的相对原子质量×m):(B的相对原子质量×n),根据元素质量比的变形运算主要有:
(1)根据某化合物中元素的质最比求化学式根据化合物中元素的质量比(或元素的质量分数比)求化学式,其方法是通过元素的相对原子质量来推断化学式。通过组成元素质量比或元素的质量分数进行分式变换,转换成原子个数(比),推测化学式。
(2)根据某化合物中元素的质量比确定元素的化合价已知某化合物中元素的质量比确定某元素的化合价,可通过元素的质量比及元素的相对原子质量推断化学式中元素的原子个数之比,再根据化合物中正负化合价代数和为零的原则确定元素的化合价。
(3)根据元素的质量比确定元素的相对原子质量
化合物中元素的质量比等于相对原子质量与原子个数的乘积比,利用元素的质量比及化合物中各原子的个数即可求出元素的相对原子质量。相对原子质量之比等于元素的质量除以其原子个数所得的数值之比。
(4)物质的质量比与分子个数比之间的换算:
换算关系:物质的质量比
 分子个数比、如SO3、SO2、O2三种物质的质量比为5:4:2,则SO3、SO2、O2的分子个数比为
分子个数比、如SO3、SO2、O2三种物质的质量比为5:4:2,则SO3、SO2、O2的分子个数比为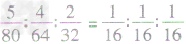 =1:1:1
=1:1:1利用化学式变形求物质的质量比:
例:含有相同质量铁元素的Fe2O3和Fe3O4的质量比是多少?
解析:设含有相同质量铁元素的Fe2O3和Fe3O4的质量分别为x,y,为了使两者含铁元素的质量相等,可以将它们的化学式变形为铁原子数目相等的式子:
Fe2O3→Fe6O9 Fe3O4→Fe6O8
480 464
x y
x:y=480:464=30:29
答案:30:29
概念:元素是具有相同核电荷数(即核内质子数)的一类原子的总称。
对元素概念的理解:
①元素是以核电荷数(即核内质子数)为标准对原子进行分类。只讲种类,不讲个数。
②质子数是划分元素种类的标准。质子数相同的原子和单核离子都属于同一种元素。如Na+与Na都属于钠元素,但Na+与NH4+不属于同一种元素。
③同种元素可以有不同的存在状态。如游离态和化合态。
④同种元素的离子因带电荷数不同,性质也不同。如Fe2+与Fe3+。
⑤同种元素的原子可以是不同种原子。如碳元素有三种不同中子数的碳原子:612C、613C、614C.
元素与原子的比较
元素、原子、分子与物质间的关系:
物质的组成可以从宏观和微观两个方面进行描述,其中元素是从宏观上对物质组成的描述,分子、原子是从微观上对物质构成的描述。其关系如下图;
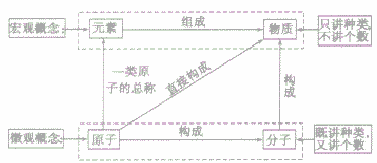
在讨论物质的组成和结构时,应注意规范地运用这些概念,现举例如下:
(1)由分子构成的物质,有三种说法(以二氧化碳为例):
①二氧化碳是由氧元素和碳元素组成的。
②二氧化碳是由二氧化碳分子构成的。
③每个二氧化碳分子是由2个氧原子和I个碳原子构成的。
(2)由原子(或离子)直接构成的物质(如汞、食盐),有两种说法:
①汞是由汞元素组成的;食盐是由钠元素和氯元素组成的。
②汞是由汞原子构成的;食盐是由钠离子和氯离子构成的。
同位素:
同位素指具有相同的质子数,但中子数不同的同一元素的不同原子,如氢有3种同位素,分别称为氕(H)、氘(D)、氚T),即原子核内质子数均为1,但中子数分别为0,1,2的氢原子。同位素有天然存在的,也有人工合成的。同一元素的同位素虽然中子数不同,但它们的化学性质基本相同。
对元素概念的理解:
①元素是以核电荷数(即核内质子数)为标准对原子进行分类。只讲种类,不讲个数。
②质子数是划分元素种类的标准。质子数相同的原子和单核离子都属于同一种元素。如Na+与Na都属于钠元素,但Na+与NH4+不属于同一种元素。
③同种元素可以有不同的存在状态。如游离态和化合态。
④同种元素的离子因带电荷数不同,性质也不同。如Fe2+与Fe3+。
⑤同种元素的原子可以是不同种原子。如碳元素有三种不同中子数的碳原子:612C、613C、614C.
元素与原子的比较
| 元素 | 原子 | |
| 概念 | 具有相同核电荷数〔即核内质子数)的一类原子的总称 | 化学变化中的最小粒子 |
| 区分 | 只讲种类,不讲个数 | 既讲种类,又讲个数 |
| 使用范围 | 用于描述物质的宏观组成 | 用于描述物质的微观构成 |
| 举例 | 水由氢元素和氧元素组成,或说水中含有氢元素和氧元素 | 每个水分子由两个氢原子和一个氧原子构成 |
| 联系 | 元素和原子是总体和个体的关系,原子是元素的个体,是构成并体现元素性质的最小微粒;元素是一类原子的总称一种元素可以包含几种原子 | |
元素、原子、分子与物质间的关系:
物质的组成可以从宏观和微观两个方面进行描述,其中元素是从宏观上对物质组成的描述,分子、原子是从微观上对物质构成的描述。其关系如下图;

在讨论物质的组成和结构时,应注意规范地运用这些概念,现举例如下:
(1)由分子构成的物质,有三种说法(以二氧化碳为例):
①二氧化碳是由氧元素和碳元素组成的。
②二氧化碳是由二氧化碳分子构成的。
③每个二氧化碳分子是由2个氧原子和I个碳原子构成的。
(2)由原子(或离子)直接构成的物质(如汞、食盐),有两种说法:
①汞是由汞元素组成的;食盐是由钠元素和氯元素组成的。
②汞是由汞原子构成的;食盐是由钠离子和氯离子构成的。
同位素:
同位素指具有相同的质子数,但中子数不同的同一元素的不同原子,如氢有3种同位素,分别称为氕(H)、氘(D)、氚T),即原子核内质子数均为1,但中子数分别为0,1,2的氢原子。同位素有天然存在的,也有人工合成的。同一元素的同位素虽然中子数不同,但它们的化学性质基本相同。
物理性质:
1. 概念: 不需要发生化学变化就直接表现出来的性质。
2. 实例:在通常状态下,氧气是一种无色,无味的气体。
3. 物质的物理性质:如颜色,状态,气味,熔点,沸点,硬度等。
化学性质:
1. 概念:物质在化学变化中表现出来的性质,如铁在潮湿的空气中生成铁锈,铜能在潮湿的空气中生成铜绿。化学性质只能通过化学变化表现出来。
物质的性质和用途的关系:
若在使用物质的过程中,物质本身没有变化,则是利用了物质的物理变化,物质本身发生了变化,变成了其他物质,则是利用了物质的化学性质。物质的性质与用途的关系:物质的性质是决定物质用途的主要因素,物质的用途体现物质的性质。
物质的性质与物质的变化的区别和联系
| 物质的性质 | 物质的变化 | |
| 区别 | 物质的性质是指物质的特有属性,不同的物质其属性不同,是变化的内因 | 物质的变化是一个过程,是有序的,动态的,性质的具体体现 |
| 联系 | 物质的性质决定了它能发生的变化,而变化又是性质的具体表现 | |
判断是“性质”还是“变化”:
判断某种叙述是指物质的“性质”还是“变化”时,首先要准确把握它们的区别和联系,若叙述中有“能”,“难”,“易”,“会”,“就”等词语,往往指性质,若叙述中有“已经”,“了”,“在”等词语,往往指物质的变化。
有关描述物质的词语:
1. 物理性质:
(1)熔点
物质从固态变成液态叫熔化,物体开始熔化时的温度叫熔点。
(2)沸点
液体沸腾时的温度叫沸点。
(3)压强
物体在单位面积上所受到的压力叫压强。
(4)密度
物质在单位体积上的质量叫密度,符号为p。
(5)溶解性
一种物质溶解在另一种物质里的能力,称为这种物质的溶解性。溶解性跟溶质、溶剂的性质及温度等因素有关。
(6)潮解
物质在空气中吸收水分,表面潮湿并逐渐溶解的现象。如固体、NaOH,精盐在空气中易潮解。
(7)挥发性
物质由固态或液态变为气体或蒸气的过程二如浓盐酸具有挥发性,可挥发出氯化氢气体
(8)导电性
物体传导电流的能力叫导电性:固体导电靠的是白由移动的电子,溶液导电依靠的是自由移动的离子
(9)导热性
物体传导热量的能力叫导热性。一般导电性好的材料,其导热性也好。
(10)延展性
物体在外力作用下能延伸成细丝的性质叫延性;在外力作用下能碾成薄片的性质叫展性。二者合称为延展性,延展性一般是金属的物理性质之一。
2. 化学性质:
(1)助燃性物质在一定的条件下能进行燃烧的性质。如硫具有可燃性。
(2)助燃性物质能够支持燃烧的性质。如氧气具有助燃性
(3)氧化性在氧化还原反应中,能够提供氧元素的性质
(4)还原性在氧化还原反应中,能够夺取含氧化合物中氧元素的性质,初中化学常见的还原性物质(即还原剂)有 H2、CO、C。
(5)酸碱性酸碱性是指物质能够使酸碱指示剂变色的性质: 酸性溶液能使紫色石蕊变红,碱性溶液能使紫色石蕊变蓝。
(6)稳定性物质不易与其他物质发生化学反应或自身不易发生分解反应的性质,如稀有气体化学性质稳定。
(7)风化结晶水合物(如Na2CO3·10H2O)在干燥的环境中失去结晶水的性质。
发现相似题
与“2011年5月食品塑化剂事件引起社会的高度关注.常用塑化剂的学...”考查相似的试题有:
- 以下生活常识的认识正确的是( )A.绿颜色的食品均为“绿色食品”B.油污可被洗涤剂通过乳化作用除去C.白色物质造成的污染即...
- 下列关于生活和健康常识的说法不正确的是[ ]A.甲醛溶液可用于水产品保鲜B.用地沟油烹饪的食物危害人体健康C.水果和蔬菜含...
- 化学物质的不恰当使用有可能对人体健康造成危害,下列做法不会给健康带来不良影响的是( )A.食用甲醛溶液浸泡的水产品B.发...
- 某元素R的氧比物中,R元素与氧元素的质量比为7:8,R的相对原子质量为14,则R氧化物的化学式是( )A.ROB.RO2C.R2OD.R2O5
- 2009年2月20日6:20分左右江苏省盐城市许多市民在饮用自来水时闻到刺鼻的农药味。经检测,该市城西自来水厂的水源受到盐城市...
- 下列各物质的组成中,不含原子团的是( )A.FeCl3B.HNO3C.MgSO4D.NaOH
- 以下物质中,不含有原子团的是( )A.KClB.CaCO3C.Cu(OH)2D.Na2SO4
- 下列物质的性质中,属于化学性质的是( )A.酒精易挥发B.氯化钠易溶于水C.石墨能导电D.碳酸易分解
- 苏州博物馆用“真空充氮杀虫灭菌消毒机”来处理和保护文物.即将文物置于该机器内,三天后氮气浓度可达99.99%;再密闭三天左右...
- (3分)如下图所示,在高温条件下,框图A巾的粒子可以转化为框图B中的粒子。(1)反应前物质A属于 (填物质类别);(2)请在反应...