本试题 “某校研究性学习小组到实验室进行探究实验.他们准备用加热高锰酸钾的方法制取氧气并验证氧气的性质.(1)请指出图中所用仪器的名称:a______,b______,c___...” 主要考查您对常用仪器的名称和选用
氧气的制取和收集
氧气的性质
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 常用仪器的名称和选用
- 氧气的制取和收集
- 氧气的性质
常用的实验仪器:
试管、烧杯、蒸发皿、坩埚、酒精灯、漏斗、洗气瓶、干燥管、
托盘天平、量筒、容量瓶、滴定管、玻璃棒、量气装置等。
常用仪器对比分析:
试管、烧杯、蒸发皿、坩埚、酒精灯、漏斗、洗气瓶、干燥管、
托盘天平、量筒、容量瓶、滴定管、玻璃棒、量气装置等。
常用仪器对比分析:
|
常见的化学仪器 |
主要用途 | ||
|
分类 |
名称 |
图示 | |
| 用于加热仪器 | 试管 |  |
(1)用作少量试剂的反应容器,在常温或加热时使用 (2)作为小型气体发生器 (3)收集少量气体 |
| 蒸发皿 |  |
用于溶液的蒸发、浓缩 | |
| 燃烧匙 |  |
用于盛放可燃性固体物质进行燃烧实验 | |
| 烧杯 |  |
(1)溶解物质配制溶液 (2)较大量试剂反应容器 (3)常温或加热使用 | |
| 锥形瓶,烧瓶(圆底,平底) | 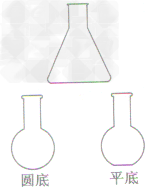 |
(1)用作较大量液体反应的容器和气体发生装置,在常温或加热时使用 (2)锥形瓶是蒸馏的接收容器 | |
| 酒精灯 |  |
用于加热 | |
| 盛放物质的仪器 | 集气瓶 |  |
(1)收集和储存少量气体 (2)进行物质和气体之间的反应 |
| 滴瓶,滴管 |  |
滴瓶用于盛放少量液体试剂 | |
| 细口瓶 |  |
储存液体药品 | |
| 广口瓶 | 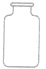 |
储存固体药品 | |
| 计量仪器 | 托盘天平 | 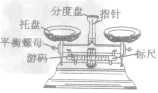 |
称量物质的质量(精确度为0.1g) |
| 量筒 |  |
量取一定体积的液体或间接测量气体的体积 | |
| 漏斗 | 普通漏斗 |  |
过滤,注入液体 |
| 长颈漏斗 |  |
用于注入液体 | |
| 分液漏斗 |  |
(1)注入液体 (2)分液漏斗用于分离两种密度不同且互不相溶的液体 | |
| 夹持仪器 | 铁架台 |  |
固定和放置各种仪器 |
| 试管夹 |  |
夹持试管进行简单的加热试验 | |
| 坩埚钳 |  |
夹持坩埚或夹持热的蒸发皿等 | |
| 辅助仪器 | 水槽 |  |
排水集气 |
| 药匙 |  |
取用固体药品(粉末状或小颗粒状) | |
| 玻璃棒 | 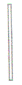 |
搅拌液体,引流,沾取液体 | |
| 石棉网 |  |
用于烧杯或烧瓶加热时垫在底部,使仪器受热均匀 | |
| 试管刷 |  |
用于刷洗试管等玻璃仪器 | |
| 温度计 |  |
用于测量温度 | |
氧气的制取是初中化学的重点,也是历年中考的热点。我们不仅要学好氧气制取的知识,而且要触类旁通,逐步掌握实验室制取气体的一般思路和方法。中考对制取氧气的考查主要集中在药品选用、实验装置、操作步骤等方面。
实验室制取收集氧气:
| 过氧化氢制氧气 | 高锰酸钾制氧气 | |
| 药品和反应原理 | 2H2O2 2H2O+O2↑ 2H2O+O2↑ |
2KMnO4 K2MnO4 + MnO2 + O2↑ K2MnO4 + MnO2 + O2↑ |
| 发生装置 | 固液常温型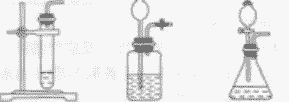 |
固体加热型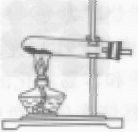 |
| 收集装置 | 氧气可用排水法收集,也可用向上排空气法收集 | |
| 整体装置图 | 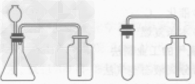 |
 |
| 操作步骤 | ①检查装置气密性 ②再锥形瓶中装入二氧化锰 ③塞好带有长颈漏斗和导管的橡皮塞(长颈漏斗的下端一定在液面以下,否则氧气会从长颈漏斗中跑出来) ④向长颈漏斗中加入过氧化氢溶液 ⑤收集氧气 |
①检查装置气密性 ②将药品平铺在试管底部,用带导管的单孔橡皮塞塞紧试管口(用高锰酸钾制取氧气,还要在管口放一小团棉花) ③将试管固定在铁架台上 ④点燃酒精灯,预热后加热试管 ⑤当导管口有连续均匀的气泡冒出时开始收集气体 ⑥收集完毕,先将导管移出水面 ⑦熄灭酒精灯。加热高锰酸钾(或氯酸钾和二氧化锰的混合物)制氧气,用排水法收集,其操作步骤可概括为:“查”“装”“定”“点”“收”“离”“熄”7个字。可用谐音记忆为“茶庄定点收利息”。 |
| 注意事项 | ①伸入试管或锥形瓶中的导管应刚刚露出橡皮塞即可,否则不利于气体的导出。 ②用排水法收集氧气时,导管应刚伸人集气瓶口即可,过长不利于水的排出,气体不易收集满。 ③用向上排空气法收集氧气时,导管要伸入集气瓶的底部,否则不利于空气的排出,收集的气体不纯。 ④用长颈漏斗时,长颈漏斗末端应在液面以下,否则氧气会从长颈漏斗中逸出。 |
①药品要平铺在试管底部,均匀受热。 ②试管口要略向下倾斜,防止药品中湿存的水分受热后变成水蒸气,遇冷凝结成水倒流回试管底部,使试管炸裂。 ③铁架台的铁夹要夹在试管的中上部(或距离试管口1/3处)。 ④试管内的导管稍伸出橡皮塞即可,这样便于气体导出。 ⑤集气瓶充满水后倒放入水槽中(瓶口要在水面下)。 ⑥加热时要先使试管均匀受热,然后酒精灯外焰要对准药品所在部位加热。 ⑦用排水法收集气体时,应注意当气泡连续均匀冒出时再收集,否则收集的气体中混有空气,当集气瓶口有大盆气泡冒出时,证明已集满。 ⑧停止加热时,应先把导管从水里撤出,再撤掉酒精灯。如果先熄灭酒精灯,试管内气体温度降低,压强减小,水槽中的水就会被倒吸入热的试管内,使试管炸裂。 ⑨用高锰酸钾制氧气时,试管口要放一小团棉花,防止加热时高锰酸钾小颗粒进人导管。 ⑩盛氧气的集气瓶应盖上玻璃片正放,因为在相同状况下氧气的密度大于空气的密度,正放可减少气体的逸散。 |
定义:
氧气,空气主要组分之一,比空气重,标准状况(0℃和大气压强101325帕)下密度为1.429克/升。无色、无臭、无味。在水中溶解度很小。压强为101kPa时,氧气在约-183摄氏度时变为淡蓝色液体,在约-218摄氏度时变成雪花状的淡蓝色固体。
氧气的性质:
1.氧气的物理性质:
(1)无色无味,标况下,氧气的密度为1.429g/L,密度比空气大,难溶于水,1L水中只能溶解约30ml的氧气。
(2)三态变化:氧气(无色气体) 液氮(淡蓝色液体)
液氮(淡蓝色液体) 固态氮(淡蓝色雪花状)
固态氮(淡蓝色雪花状)
(3)工业产生的氧气,一般加压贮存在蓝色的钢瓶中。
2.氧气的化学性质:
(1)化学性质较活泼,在一定条件下,可以和多种物质发生化学反应,同时放出热量;具有助燃性和氧化性,在化学反应中提供氧,是一种常用的氧化剂。
(2)助燃性,氧化性
①与金属的反应:
2Mg+O2 2MgO
2MgO
3Fe+2O2 Fe3O4
Fe3O4
②与非金属的反应:
C+O2 CO2(O2充分)
CO2(O2充分)
2C+O2 2CO(O2不充分)
2CO(O2不充分)
③与化合物的反应:
2CO+O2 2CO2
2CO2
CH4+2O2 CO2+2H2O
CO2+2H2O
C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
易错点:
(1)误认为氧气具有可燃性,可以做燃料
氧气可以帮助可燃物燃烧,具有助燃性,它本身不能燃烧,不能做可燃物。
(2)误认为氧气的化学性质非常活泼,能与所有物质发生反应
氧气是一种化学性质非常活泼的气体,在一定条件下能与许多物质发生化学反应,但不是与所有物质都能发生化学反应。
(3)误认为燃烧都需要氧气
燃烧有广义和狭义之分,通常所说的燃烧是指可燃物与氧气发生的一种发光,放热的剧烈的氧化反应。燃烧的条件之一是需要氧气。但有一些燃烧不需要氧气,如镁在二氧化碳中也能燃烧。
(4)误认为物质与氧气的反应叫氧化反应
氧化反应是物质与氧发生的反应,其中包括物质与氧气中的氧元素发生的反应,也包括物质与其他含氧物质中的氧元素发生的反应。如氢气与氧气反应生成水是氧化反应,氢气与氧化铜反应生成铜和水也是氧化反应。
(5)误认为氧气与液氧性质不行
物质的性质包括物理性质和化学性质,氧气与液氧物理性质不同,但化学性质是相同的,因为它们二者的分子构成相同,都是由氧分子构成的。
(6)误认为含氧的物质都能制取氧气。
制取氧气需要含氧的物质,但不是所有的含氧物质都能用来制取氧气。
氧气,空气主要组分之一,比空气重,标准状况(0℃和大气压强101325帕)下密度为1.429克/升。无色、无臭、无味。在水中溶解度很小。压强为101kPa时,氧气在约-183摄氏度时变为淡蓝色液体,在约-218摄氏度时变成雪花状的淡蓝色固体。
氧气的性质:
1.氧气的物理性质:
(1)无色无味,标况下,氧气的密度为1.429g/L,密度比空气大,难溶于水,1L水中只能溶解约30ml的氧气。
(2)三态变化:氧气(无色气体)
 液氮(淡蓝色液体)
液氮(淡蓝色液体) 固态氮(淡蓝色雪花状)
固态氮(淡蓝色雪花状)(3)工业产生的氧气,一般加压贮存在蓝色的钢瓶中。
2.氧气的化学性质:
(1)化学性质较活泼,在一定条件下,可以和多种物质发生化学反应,同时放出热量;具有助燃性和氧化性,在化学反应中提供氧,是一种常用的氧化剂。
(2)助燃性,氧化性
①与金属的反应:
2Mg+O2
 2MgO
2MgO3Fe+2O2
 Fe3O4
Fe3O4②与非金属的反应:
C+O2
 CO2(O2充分)
CO2(O2充分)2C+O2
 2CO(O2不充分)
2CO(O2不充分)③与化合物的反应:
2CO+O2
 2CO2
2CO2CH4+2O2
 CO2+2H2O
CO2+2H2OC2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O易错点:
(1)误认为氧气具有可燃性,可以做燃料
氧气可以帮助可燃物燃烧,具有助燃性,它本身不能燃烧,不能做可燃物。
(2)误认为氧气的化学性质非常活泼,能与所有物质发生反应
氧气是一种化学性质非常活泼的气体,在一定条件下能与许多物质发生化学反应,但不是与所有物质都能发生化学反应。
(3)误认为燃烧都需要氧气
燃烧有广义和狭义之分,通常所说的燃烧是指可燃物与氧气发生的一种发光,放热的剧烈的氧化反应。燃烧的条件之一是需要氧气。但有一些燃烧不需要氧气,如镁在二氧化碳中也能燃烧。
(4)误认为物质与氧气的反应叫氧化反应
氧化反应是物质与氧发生的反应,其中包括物质与氧气中的氧元素发生的反应,也包括物质与其他含氧物质中的氧元素发生的反应。如氢气与氧气反应生成水是氧化反应,氢气与氧化铜反应生成铜和水也是氧化反应。
(5)误认为氧气与液氧性质不行
物质的性质包括物理性质和化学性质,氧气与液氧物理性质不同,但化学性质是相同的,因为它们二者的分子构成相同,都是由氧分子构成的。
(6)误认为含氧的物质都能制取氧气。
制取氧气需要含氧的物质,但不是所有的含氧物质都能用来制取氧气。
发现相似题
与“某校研究性学习小组到实验室进行探究实验.他们准备用加热高...”考查相似的试题有:
- 下图是实验室中用于制取和收集气体的装置图,请回答以下问题:⑴写出上图中带标号仪器的名称:① ,② 。⑵用高锰酸钾制取氧气,...
- 使用和选择实验装置,一方面要知道仪器的名称、用途和使用时的注意事项;另一方面要知道各种仪器组装的方法,更要懂得为什么...
- 某校进行中考化学实验操作考查,有以下五个考题:①粗盐提纯;②酸的化学性质;③二氧化碳的制取、收集和验满;④氧气的制取、收...
- 下图是实验室中常见的化学仪器,你可能已使用过多次。(1)请按下列要求把上图仪器的名称填在指定位置上。①少量溶液相互反应时...
- (6分)通过一学期的学习,同学们一定对右图装置很熟悉,请回答有关问题:(1)写出标号仪器有名称:① ② (2)我们知道有两种...
- 根据下图所给实验装置回答下列问题:(1)图中仪器a的名称是_______;(2)用A装置在实验室制氢气,该反应的化学方程式为____...
- 实验室常用下列A、B装置来制取气体:(1)写出有标号仪器的名称:a________ ,b ________。(2)实验室用B装置制氧气的反应物是__...
- 以下描述的实验现象正确的是 ( )A.红磷在空气中燃烧产生大量白雾,放出热量B.硫在空气中燃烧产生明亮的蓝紫色火焰,放出...
- 实验室有如下图所示的仪器:(1)写出下列仪器的名称:⑥______,⑧______.(2)实验室用加热高锰酸钾的方法制取并用排水法收...
- 化学是一门以实验为基础的科学。下列有关实验现象的描述中正确的是A.红磷在氧气中燃烧发出耀眼的白光,并产生大量的白雾B....