本试题 “下列有关的叙述正确的是[ ]A.用苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出B.实验室可用NaOH溶液处理NO2和HCl废气C.酸碱滴定时,若加入待测液前...” 主要考查您对溶液
浊液
胶体
分液
酸碱中和滴定
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶液
- 浊液
- 胶体
- 分液
- 酸碱中和滴定
一种或几种物质分散到另一种物质中,形成均一、稳定的混合物,分散质粒子的直径d<10-9m
电中性原理:
溶液对外是不显电性的,所以,在电解质的溶液中,阳离子所带正电荷总数=阴离子所带负电荷总数。
如含K+、Al3+、H+、Cl-、SO42-的溶液中,必然存在c(K+)+3c(Al3+)+c(H+)=c(Cl-)+2c(SO42-)。
溶液的稀释定律:
- 稀释前后溶液中溶质的物质的量不变: c(浓溶液)V(浓溶液)=c(稀溶液)V(稀溶液)
- 稀释前后溶液中溶质的质量不变: ρ(浓溶液)V(浓溶液)w%(浓溶液)=ρ(稀溶液)V(稀溶液)w%(稀溶液)
容量瓶的使用:
1.容量瓶的使用及注意事项
(1)在使用前首先要检查是否漏水。
具体操作如下:
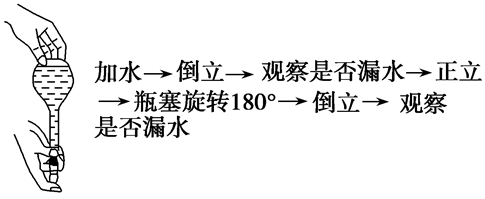
(2)检查合格后,用蒸馏水洗涤干净。
(3)四个“不能”
①不能将固体或浓溶液直接在容量瓶中溶解或稀释。
②不能作为反应容器或长期贮存溶液。
③容量瓶的容积是在瓶身所标温度下确定的,因而不能将过冷或过热的溶液转移到容量瓶中。
④只能配制容量瓶上规定容积的溶液,即不能配制任意体积的溶液。
2. 误差分析
分析依据 ,以配置NaOH溶液为例,在进行误差分析时,根据实验操作弄清是“m”还是“V”引起的误差,再具体分析,具体情况如下:
,以配置NaOH溶液为例,在进行误差分析时,根据实验操作弄清是“m”还是“V”引起的误差,再具体分析,具体情况如下:
| 能引起误差的一些操作 | 因变量 | c(mol/L) | |
| m | V | ||
| 砝码与物品颠倒(使用游码) | 减小 | —— | 偏低 |
| 称量时间过长 | 减小 | —— | |
| 用滤纸称NaOH | 减小 | —— | |
| 向容量瓶注液时少量溅出 | 减小 | —— | |
| 未洗涤烧杯和玻璃棒 | 减小 | —— | |
| 定容时,水多用滴管吸出 | 减小 | —— | |
| 定容摇匀后液面下降再加水 | —— | 增大 | |
| 定容时仰视刻度线 | —— | 增大 | |
| 砝码沾有其他物质或已生锈 | 增大 | —— | 偏高 |
| 未冷却至室温就注入容量瓶定容 | —— | 减小 | |
| 定容时俯视读数 | —— | 减小 | |
| 称量前小烧杯内有水 | —— | —— | 不变 |
| 定容后经振荡、摇匀,静置液面下降 | —— | —— | |
特别提醒:
(1)定容、摇匀后液面下降也不要补加蒸馏水,否则结果会偏低。
(2)定容时俯视、仰视对结果的影响。
①仰视刻度线(图1),导致溶液体积偏大。
②俯视刻度线(图2),导致溶液体积偏小。

为减小误差务必按:眼睛视线→刻度线→凹液面最低处的次序,做到“三点一线”。
一定物质的量浓度的溶液的配置:
1.主要仪器 (1)托盘天平:可精确至0.1g,称量前先调零,称量时物品放在左盘,砝码放在右盘。
(2)容量瓶:配制溶液的专用精确容器,瓶上标有温度、容积和刻度线。
(3)其他仪器:量筒、烧杯、玻璃棒、胶头滴管等。
2.配制过程
配制过程如下:

以配制480mL1mol·L-1NaCl溶液为例:
(1)所需容量瓶规格:500mL容量瓶。
(2)若用托盘天平应称量NaCl粉末29.3g。
(3)溶解过程中玻璃棒的作用为:搅拌加速溶解。
(4)移液
①移液前需要将溶液冷却至室温。
②移液中玻璃棒的作用为:引流。
③移液时需要进行的操作为:将烧杯中溶液注入容量瓶中,用少量蒸馏水洗涤烧杯内壁2~3次并将洗涤液也转入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀。
(5)定容
①当液面距瓶颈刻度线1~2cm时改用胶头滴管滴加蒸馏水。
②定容时要平视刻度线,直到凹液面最低点与刻度线相切。
(6)摇匀,转入试剂瓶保存
假如其他操作均准确无误,分析下列情况对配制浓度的影响。
①定容时俯视观察刻度线:偏高;
②移液时,对用于溶解NaCl的烧杯没有洗涤:偏低;
③定容后,将容量瓶振荡摇匀,静置后发现液面低于刻度线,又补水至刻度线:偏低。
溶液配制过程中的“四个数据”:
(1)选择容量瓶的规格时应该与所配溶液体积相等或稍大
数据
要求或解释
药品的质量
实验室中一般用托盘天平称量药品,而托盘天平只能称准0.1g,所以记录数据时只能保留小数点后一位数字。如题中NaOH的质量为10.0,不能写为10.00g
容量瓶的规格
(2)回答补充仪器的问题时应该注明容量瓶的规格,如应该回答“500ml容量瓶”,不能只回答“容量瓶”。
洗涤烧瓶2-3次
移液时洗涤烧瓶2-3次是为了确保溶质全部转移入容量瓶中,否则会导致溶液浓度偏低
液面离容量瓶颈刻度线下1-2cm
定容时,当液面离容量瓶颈刻度线下1-2cm时,应该改用胶头滴管滴加,否则溶液导致液体体积超过刻度线,导致溶液浓度偏低
浊液:
粒子直径大于100nm的分散系,若分散质为固体小颗粒的称为悬浊液,若分散质为小液滴的称为乳浊液。
悬浊液是固体的小颗粒分散在溶剂中所形成的混合物;
乳浊液是液体的小液滴分散在溶剂中所形成的混合物。
浊液的特性:
浊液里的固体小颗粒或小液滴都是由巨大数量的分子(或原子等)集合而成的。浊液静置后,其中的固体小颗粒或小液滴会逐渐下沉或上浮。所以浊液中物质的分散是不均一、不稳定的。
分散系比较:
| 分散系 | 溶液 | 胶体 | 悬浊液 | 乳浊液 |
| 分散质粒子大小 | <1nm | 1~100nm | >100nm | >100nm |
| 分散质粒子结构 | 分子、离子 | 少量分子的结合体或大分子 | 大量分子聚集成的固体小颗粒 | 大量分子聚集成的液体小液滴 |
| 特点 | 均一、透明、稳定 | 多数均一、透明、较稳定 | 不均一、不透明、久置沉淀 | 不均一、不透明、久置分层 |
| 能否透过滤纸 | 能 | 能 | 不能 | —— |
| 实例 | 食盐水、蔗糖溶液 | Fe(OH)3(胶体)、淀粉胶体 | 泥水、石灰乳 | 牛奶、油漆 |
胶体:分散质粒子直径在10-9m~10-7m之间的分散系胶粒直径的大小是胶体的本质特征
胶体可分为固溶胶、液溶胶、气溶胶
①常见的液溶胶:Fe(OH)3、AgI、牛奶、豆浆、粥等
②常见的气溶胶:雾、云、烟等;
③常见的固溶胶:有色玻璃、烟水晶等胶体的性质:
丁达尔效应:
①当光束通过氢氧化铁胶体时,可以看到一条光亮的通路,这条光亮的通路是由于胶体粒子对光线散射(光波偏离原来方向而分散传播)形成的,即为丁达尔效应。
②布朗运动:粒子在不停地、无秩序的运动
③电泳:胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂里定向移动。一般来讲:金属氢氧化物,金属氧化物的胶粒吸附阳离子,胶体微粒带正电荷;非金属氧化物,金属硫化物的胶体胶粒吸附阴离子,胶体微粒带负电荷。
④胶体聚沉:向胶体中加入少量电解质溶液时,由于加入的阳离子(或阴离子)中和了胶体粒子所带的电荷,使胶体粒子聚集成为较大的颗粒,从而形成沉淀从分散剂里析出。该过程不可逆。
胶体的特性:
(1)丁达尔效应当一束光通过胶体时,胶体内会出现一条光亮的通路,这是由胶体粒子对光线散射而形成的,利用丁达尔效应可区分胶体和浊液。
(2)介稳性:胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,但改变条件就有可能发生聚沉。
(3)聚沉:给胶体加热、加入电解质或加入带相反电荷的胶体颗粒等均能使胶体粒子聚集成较大颗粒,从而形成沉淀从分散剂里析出。聚沉常用来解释生活常识,如长江三角洲的形成、明矾净水等。
(4)电泳现象:在电场作用下,胶体粒子在分散剂中作定向移动。电泳现象说明胶体粒子带电。电泳常用来分离提纯胶体,如工业上静电除尘。
分散系比较:
| 分散系 | 溶液 | 胶体 | 悬浊液 | 乳浊液 |
| 分散质粒子大小 | <1nm | 1~100nm | >100nm | >100nm |
| 分散质粒子结构 | 分子、离子 | 少量分子的结合体或大分子 | 大量分子聚集成的固体小颗粒 | 大量分子聚集成的液体小液滴 |
| 特点 | 均一、透明、稳定 | 多数均一、透明、较稳定 | 不均一、不透明、久置沉淀 | 不均一、不透明、久置分层 |
| 能否透过滤纸 | 能 | 能 | 不能 | —— |
| 实例 | 食盐水、蔗糖溶液 | Fe(OH)3(胶体)、淀粉胶体 | 泥水、石灰乳 | 牛奶、油漆 |
胶体发生聚沉的条件:
因胶粒带电,故在一定条件下可以发生聚沉:
- 向胶体中滴加电解质
- 向胶体中加入带相反电荷胶粒的胶体
- 加热
常见的胶体的带电情况:
- 胶粒带正电荷的胶体有:金属氧化物、金属氢氧化物。例如Fe(OH)3、Al(OH)3等。
- 胶粒带负电荷的胶体有:非金属氧化物、金属硫化物、硅酸胶体、土壤胶体。
- 胶粒不带电的胶体有:淀粉胶体。
- 特殊的,AgI胶粒随着AgNO3和KI相对量不同,而带正电或负电。若KI过量,则AgI胶粒吸附较多I-而带负电;若AgNO3过量,则因吸附较多Ag+而带正电。
注意:胶体不带电,而胶粒可以带电。
Fe(OH)3胶体的制备:
操作步骤:将烧杯中的蒸馏水加热至沸腾,向沸水中滴加5~6滴饱和FeCl3溶液,继续煮沸至呈红褐色为止。
离子方程式:Fe3++3H2O=(加热)=Fe(OH)3(胶体)+3H+
点拨:(1)淀粉溶液、蛋白质溶液虽叫做溶液,但属于胶体。
(2)胶体可以是液体,也可以是固体、气体,如烟、云、雾、有色玻璃等。
分液:
| 名称 | 用途 | 装置 | 举例 | 注意事项 |
| 分液 | 分离两种不相混溶的液体(密度不同) | 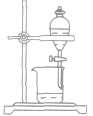 |
水、苯的分离 | 下层液体从下口放出,上层液体从上口倒出 |
酸碱中和滴定:
用已知物质的量浓度的酸(或碱)来测 定未知物质的量浓度的碱(或酸)的方法叫做酸碱中和滴定。
(1)原理:对于一元酸和一元碱发生的中和反应,C酸V酸=C碱V碱 或:C未知V未知=C标准V标准,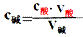
(2)仪器:a.酸式滴定管 b.碱式滴定管c.铁架台d.滴定管夹e.锥形瓶 f.烧杯g.胶头滴管等
(3)装置图: 
(4)操作步骤:
洗涤、检漏、水洗、润洗、装液、去泡、调液面记录、放待测液、加指示剂、滴定、记录、
计算、误差分析
(5)数据处理依据:
c(NaOH)=c(HCl)V(HCl)/V(NaOH)
(6)误差分析:
①仪器润洗不当:
a.盛标准液的滴定管用蒸馏水洗后未用标准液润洗;
b.盛待测液滴定(移液)管用蒸馏水洗后未用待测液润洗;
c.锥形瓶用蒸馏水洗后再用待测液润洗;
②读数方法有误:
a.滴定前仰视,滴定后俯视;
b.滴定前俯视,滴定后仰视;
c.天平或量筒的使用读数方法错误;
③操作出现问题:
a.盛标准液的滴定管漏液;
b.盛待测液的滴定管滴前尖嘴部分有气泡,终了无气泡
(或前无后有);
c.振荡锥形瓶时,不小心有待测液溅出;
d.滴定过程中,将标准液滴到锥形瓶外;
中和滴定中的误差分析:
中和滴定是一个要求较高的定量实验,每一个不当的或错误的操作都会引起误差。
对于一元酸与一元碱,由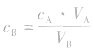 可知,
可知,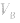 是准 确量取的体积,
是准 确量取的体积, 是标准溶液的浓度,它们均为定值,所以
是标准溶液的浓度,它们均为定值,所以 的大小取决于
的大小取决于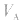 的大小,
的大小,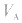 大则
大则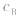 大,
大,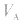 小则
小则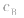 小。
小。
以标准酸溶液滴定末知浓度的碱溶液(酚酞作指示剂)为例,常见的不正确操作对实验结果的影响见下表: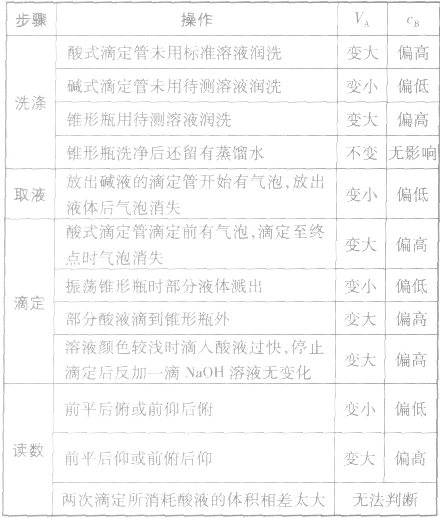
中和滴定应注意的问题:
1.中和滴定中指示剂的使用与选择
(1)用量不能太多,常用2~3滴,冈指示剂本身也是有机弱酸或有机弱碱,若用量太多,会使中和滴定中需要的酸或碱的量增多或减少。
(2)指示剂的选择:中和滴定时一般选用的指示剂有酚酞和甲基橙。石蕊试液由于颜色变化不明显,不易辨别,在滴定过程中不宜使用。
(3)酸、碱恰好完全反应时,终点溶液的pH应在指示剂的变色范围内,如强酸溶液滴定弱碱溶液应选用甲基橙作指示剂;强碱溶液滴定弱酸溶液应选用酚酞作指示剂。
(4)指示剂的变色:最好由浅到深,这样对比明显。如用强碱滴定强酸用酚酞作指示剂较好,当酚酞从无色变为粉红色(或浅红色)且半分钟内不褪色时即达到滴定终点。
2.欲减小实验误差的三点做法
(1)半分钟:振荡,半分钟内颜色不褪去,即为滴定终点。
(2)l一2min:滴定停止后,必须等待l~2min,让附着在滴定管内壁的溶液流下后,再进行读数。
(3)重复:同一实验,要做两到三次,两次滴定所用标准溶液的体积的差值不能超过0.02mL,再取平均值。
与“下列有关的叙述正确的是[ ]A.用苯萃取溴水中的溴,分液时有...”考查相似的试题有:
- 当光束通过下列分散系:①有尘埃的空气②稀硫酸③蒸馏水④墨水⑤稀豆浆,能观察到丁达尔效应的是A.①④⑤B.②③⑤C.①②⑤D.①②④
- 下列事实与胶体性质无关的是 ( )A.日常生活中看到的烟、云、雾B.向豆浆中加入石膏制得可口的豆腐C.FeCl3溶液呈现棕黄色...
- 下列关于胶体的叙述不正确的是[ ]A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9~10-7m之间B.光线透过胶体时,...
- 胶体区别于其他分散系的本质特征是( )A.是混合物B.有丁达尔效应C.属于介稳系统D.粒子大小在1nm~100nm之间
- 下列说法正确的是( )A.CuSO4•5H2O是一种混合物B.O3是由3个氧原子构成的化合物C.可用丁达尔现象区分溶液与胶体D.生石灰...
- 下列各组液体混合物,可以用分液漏斗分离的是( ) A.乙醇和水 B.溴乙烷和水 C.溴乙烷和氯仿 D.苯和溴苯
- 现有常温条件下的甲、乙、丙三种溶液。甲为0.1mol·L-1的NaOH溶液,乙为 0.1mol·L-1的HCl溶液,丙为0.1mol·L-1的CH3COOH溶...
- 向20mL NaOH溶液中逐滴加入0.1mol/L醋酸溶液,滴定曲线如图所示.下列判断正确的是( )A.在M点,两者恰好反应完全B.滴定前...
- 用标准的NaOH溶液滴定未知浓度的盐酸,若测定结果偏低,其原因可能是( )A.配制标准溶液的固体NaOH中混有杂质KOHB.滴定终...
- 用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:(1)准确称量8.2g含有少量中性易溶杂质的样品,配成500mL待测...