本试题 “阅读下列科普短文,然后回答问题.臭氧的化学式是O3,在通常状况下是淡蓝色、有鱼腥臭味的气体.臭氧不稳定,一旦受热极易转化成O2,并放出大量的热,臭氧的...” 主要考查您对空气的污染和防治
氧气的性质
氧化反应
化合反应
文字表达式
物理性质和化学性质的区别和应用
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 空气的污染和防治
- 氧气的性质
- 氧化反应
- 化合反应
- 文字表达式
- 物理性质和化学性质的区别和应用
空气污染:
即空气中含有一种或多种污染物,其存在的量、性质及时间会伤害到人类、植物及动物的生命,损害财物、或干扰舒适的生活环境,如臭味的存在。换言之,只要是某一种物质其存在的量,性质及时间足够对人类或其他生物、财物产生影响者,我们就可以称其为空气污染物;而其存在造成之现象,就是空气污染。换言之,某些物质在空气中不正常的增量就产生空气污染的情形。
空气污染治理:
1. 空气污染及来源
导致空气质量下降的污染物很多。目前量多且危害严重的空气污染物主要有二氧化硫(SO2)、氮氧化物 (NO2)、一氧化碳(CO)和可吸入颗粒物等。如下表所示:
2. 空气污染的危害
①酸雨:SO2、NOx等气体形成酸雨。
②臭氧层破坏:氟利昂的释放,加速臭氧分解。
③其他危害:空气污染严重危害了人体健康,影响了农作物生长,破坏了生态平衡。
3. 空气污染的防治
①改善燃料结构,尽量充分燃烧液体燃料和气体燃料。
②对化石燃料进行脱硫、脱氮处理,工厂的废气要经过处理再排放。
③开发新能源,如太阳能、风能、水能、地热能等。
④大力开展植树造林活动,提高环境的自我净化能力。
空气质量日报:
空气质量日报的主要内容:空气污染指数,首要污染物,空气质量级别,空气质量状况。
计入空气污染指数的项目:二氧化硫,一氧化碳,二氧化氮,可吸入颗粒物,臭氧等。
空气质量级别:
PM2.5
(1)什么是PM2.5:PM2.5是指大气中小于或等于2.5微米的颗粒物,也称为可入肺颗粒物。它的直径还不到人的头发丝粗细的1/20。虽然PM2.5只是地球大气成分中含量很少的组分,但对空气质量和能见度等有重要影响。
(2)PM2.5的性状:与较粗的大气颗粒物相比,PM2.5粒径小,富含大量的有毒,有害物质且能在大气中停留时间长,输送距离远,因而对人体健康和大气环境质量的影响更大。
(3)PM2.5的来源:主要来源是日常发电,工业生产,汽车尾气排放等过程中经过燃烧而排放的残留物,大多含有重金属的等有毒物质。一般而言,粒径2.5微米至10微米的粗颗粒物主要来自道路扬尘等,2.5微米以下的细颗粒物(PM2.5)则主要来自化石燃料的燃烧(机动车尾气,燃烧)、挥发性有机物等。
(4)2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM2.5监测指标。
室内空气污染:
指由于各种原因导致的室内空气中有害物质超标.进而影响人体健康的室内环境污染。有害物质包括甲醛、苯、氨、放射性物质等。
即空气中含有一种或多种污染物,其存在的量、性质及时间会伤害到人类、植物及动物的生命,损害财物、或干扰舒适的生活环境,如臭味的存在。换言之,只要是某一种物质其存在的量,性质及时间足够对人类或其他生物、财物产生影响者,我们就可以称其为空气污染物;而其存在造成之现象,就是空气污染。换言之,某些物质在空气中不正常的增量就产生空气污染的情形。
空气污染治理:
1. 空气污染及来源
导致空气质量下降的污染物很多。目前量多且危害严重的空气污染物主要有二氧化硫(SO2)、氮氧化物 (NO2)、一氧化碳(CO)和可吸入颗粒物等。如下表所示:
| 空气污染物 | 主要来源 |
| 二氧化硫 | 煤、石油等燃料的燃烧,生产硫酸等工厂排放的尾气 |
| 一氧化碳 | 化石燃料等不完全燃烧 |
| 氮氧化物 | 机动车辆等排放的废气 |
| 可吸入颗粒物 | 地面扬尘、燃煤排放的粉尘等 |
2. 空气污染的危害
①酸雨:SO2、NOx等气体形成酸雨。
②臭氧层破坏:氟利昂的释放,加速臭氧分解。
③其他危害:空气污染严重危害了人体健康,影响了农作物生长,破坏了生态平衡。
3. 空气污染的防治
①改善燃料结构,尽量充分燃烧液体燃料和气体燃料。
②对化石燃料进行脱硫、脱氮处理,工厂的废气要经过处理再排放。
③开发新能源,如太阳能、风能、水能、地热能等。
④大力开展植树造林活动,提高环境的自我净化能力。
空气质量日报:
空气质量日报的主要内容:空气污染指数,首要污染物,空气质量级别,空气质量状况。
计入空气污染指数的项目:二氧化硫,一氧化碳,二氧化氮,可吸入颗粒物,臭氧等。
空气质量级别:
| 污染指数 | 50以下 | 51-100 | 101-150 | 151-200 | 201-250 | 251-300 | 300以上 |
| 质量级别 | Ⅰ | Ⅱ | Ⅲ⑴ | Ⅲ⑵ | Ⅳ⑴ | Ⅳ⑵ | Ⅴ |
| 质量状况 | 优 | 良 | 轻微污染 | 轻度污染 | 中度污染 | 中度重污染 | 重度污染 |
PM2.5
(1)什么是PM2.5:PM2.5是指大气中小于或等于2.5微米的颗粒物,也称为可入肺颗粒物。它的直径还不到人的头发丝粗细的1/20。虽然PM2.5只是地球大气成分中含量很少的组分,但对空气质量和能见度等有重要影响。
(2)PM2.5的性状:与较粗的大气颗粒物相比,PM2.5粒径小,富含大量的有毒,有害物质且能在大气中停留时间长,输送距离远,因而对人体健康和大气环境质量的影响更大。
(3)PM2.5的来源:主要来源是日常发电,工业生产,汽车尾气排放等过程中经过燃烧而排放的残留物,大多含有重金属的等有毒物质。一般而言,粒径2.5微米至10微米的粗颗粒物主要来自道路扬尘等,2.5微米以下的细颗粒物(PM2.5)则主要来自化石燃料的燃烧(机动车尾气,燃烧)、挥发性有机物等。
(4)2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM2.5监测指标。
室内空气污染:
指由于各种原因导致的室内空气中有害物质超标.进而影响人体健康的室内环境污染。有害物质包括甲醛、苯、氨、放射性物质等。
定义:
氧气,空气主要组分之一,比空气重,标准状况(0℃和大气压强101325帕)下密度为1.429克/升。无色、无臭、无味。在水中溶解度很小。压强为101kPa时,氧气在约-183摄氏度时变为淡蓝色液体,在约-218摄氏度时变成雪花状的淡蓝色固体。
氧气的性质:
1.氧气的物理性质:
(1)无色无味,标况下,氧气的密度为1.429g/L,密度比空气大,难溶于水,1L水中只能溶解约30ml的氧气。
(2)三态变化:氧气(无色气体) 液氮(淡蓝色液体)
液氮(淡蓝色液体)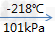 固态氮(淡蓝色雪花状)
固态氮(淡蓝色雪花状)
(3)工业产生的氧气,一般加压贮存在蓝色的钢瓶中。
2.氧气的化学性质:
(1)化学性质较活泼,在一定条件下,可以和多种物质发生化学反应,同时放出热量;具有助燃性和氧化性,在化学反应中提供氧,是一种常用的氧化剂。
(2)助燃性,氧化性
①与金属的反应:
2Mg+O2 2MgO
2MgO
3Fe+2O2 Fe3O4
Fe3O4
②与非金属的反应:
C+O2 CO2(O2充分)
CO2(O2充分)
2C+O2 2CO(O2不充分)
2CO(O2不充分)
③与化合物的反应:
2CO+O2 2CO2
2CO2
CH4+2O2 CO2+2H2O
CO2+2H2O
C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
易错点:
(1)误认为氧气具有可燃性,可以做燃料
氧气可以帮助可燃物燃烧,具有助燃性,它本身不能燃烧,不能做可燃物。
(2)误认为氧气的化学性质非常活泼,能与所有物质发生反应
氧气是一种化学性质非常活泼的气体,在一定条件下能与许多物质发生化学反应,但不是与所有物质都能发生化学反应。
(3)误认为燃烧都需要氧气
燃烧有广义和狭义之分,通常所说的燃烧是指可燃物与氧气发生的一种发光,放热的剧烈的氧化反应。燃烧的条件之一是需要氧气。但有一些燃烧不需要氧气,如镁在二氧化碳中也能燃烧。
(4)误认为物质与氧气的反应叫氧化反应
氧化反应是物质与氧发生的反应,其中包括物质与氧气中的氧元素发生的反应,也包括物质与其他含氧物质中的氧元素发生的反应。如氢气与氧气反应生成水是氧化反应,氢气与氧化铜反应生成铜和水也是氧化反应。
(5)误认为氧气与液氧性质不行
物质的性质包括物理性质和化学性质,氧气与液氧物理性质不同,但化学性质是相同的,因为它们二者的分子构成相同,都是由氧分子构成的。
(6)误认为含氧的物质都能制取氧气。
制取氧气需要含氧的物质,但不是所有的含氧物质都能用来制取氧气。
氧气,空气主要组分之一,比空气重,标准状况(0℃和大气压强101325帕)下密度为1.429克/升。无色、无臭、无味。在水中溶解度很小。压强为101kPa时,氧气在约-183摄氏度时变为淡蓝色液体,在约-218摄氏度时变成雪花状的淡蓝色固体。
氧气的性质:
1.氧气的物理性质:
(1)无色无味,标况下,氧气的密度为1.429g/L,密度比空气大,难溶于水,1L水中只能溶解约30ml的氧气。
(2)三态变化:氧气(无色气体)
 液氮(淡蓝色液体)
液氮(淡蓝色液体) 固态氮(淡蓝色雪花状)
固态氮(淡蓝色雪花状)(3)工业产生的氧气,一般加压贮存在蓝色的钢瓶中。
2.氧气的化学性质:
(1)化学性质较活泼,在一定条件下,可以和多种物质发生化学反应,同时放出热量;具有助燃性和氧化性,在化学反应中提供氧,是一种常用的氧化剂。
(2)助燃性,氧化性
①与金属的反应:
2Mg+O2
 2MgO
2MgO3Fe+2O2
 Fe3O4
Fe3O4②与非金属的反应:
C+O2
 CO2(O2充分)
CO2(O2充分)2C+O2
 2CO(O2不充分)
2CO(O2不充分)③与化合物的反应:
2CO+O2
 2CO2
2CO2CH4+2O2
 CO2+2H2O
CO2+2H2OC2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O易错点:
(1)误认为氧气具有可燃性,可以做燃料
氧气可以帮助可燃物燃烧,具有助燃性,它本身不能燃烧,不能做可燃物。
(2)误认为氧气的化学性质非常活泼,能与所有物质发生反应
氧气是一种化学性质非常活泼的气体,在一定条件下能与许多物质发生化学反应,但不是与所有物质都能发生化学反应。
(3)误认为燃烧都需要氧气
燃烧有广义和狭义之分,通常所说的燃烧是指可燃物与氧气发生的一种发光,放热的剧烈的氧化反应。燃烧的条件之一是需要氧气。但有一些燃烧不需要氧气,如镁在二氧化碳中也能燃烧。
(4)误认为物质与氧气的反应叫氧化反应
氧化反应是物质与氧发生的反应,其中包括物质与氧气中的氧元素发生的反应,也包括物质与其他含氧物质中的氧元素发生的反应。如氢气与氧气反应生成水是氧化反应,氢气与氧化铜反应生成铜和水也是氧化反应。
(5)误认为氧气与液氧性质不行
物质的性质包括物理性质和化学性质,氧气与液氧物理性质不同,但化学性质是相同的,因为它们二者的分子构成相同,都是由氧分子构成的。
(6)误认为含氧的物质都能制取氧气。
制取氧气需要含氧的物质,但不是所有的含氧物质都能用来制取氧气。
定义:
氧化反应:物质与氧发生的化学反应,如S+O2 SO2;H2+CuO
SO2;H2+CuO H2O+Cu.
H2O+Cu.
氧化反应与缓慢氧化:
氧化反应:物质与氧发生的化学反应,如S+O2
 SO2;H2+CuO
SO2;H2+CuO H2O+Cu.
H2O+Cu.氧化反应与缓慢氧化:
| 氧化反应 | 缓慢氧化 | |
| 概念 | 物质与氧(包括氧气)发生的化学反应 | 物质与氧气发生的缓慢的,不易察觉的氧化反应 |
| 举例 | 所有与氧气发生的反应 | 铁生锈,食物腐烂 |
| 联系 | 氧化反应包括剧烈氧化和缓慢氧化两种 | |
| 相同点 | ①都是氧化反应②都放出热量 | |
概念:指的是由两种或两种以上的物质生成一种新物质的反应。其中部分反应为氧化还原反应,部分为非氧化还原反应。 此外,化合反应一般释放出能量。
注意:不是所有的化合反应都是放热反应。
特征:多变一
表达式:a+b=ab
初中常见化合反应:
1.金属+氧气→金属氧化物
很多金属都能跟氧气直接化合。例如常见的金属铝接触空气,它的表面便能立即生成一层致密的氧化膜,可阻止内层铝继续被氧化。4Al+3O2=2Al2O3
2.非金属+氧气→非金属氧化物 经点燃,许多非金属都能在氧气里燃烧,如:C+O2 CO2
CO2
3.金属+非金属→无氧酸盐 许多金属能与非金属氯、硫等直接化合成无氧酸盐。如 2Na+Cl2 2NaCl
2NaCl
4.氢气+非金属→气态氢化物 因氢气性质比较稳定,反应一般需在点燃或加热条件下进行。如 2H2+O2 2H2O
2H2O
5.碱性氧化物+水→碱. 多数碱性氧化物不能跟水直接化合。判断某种碱性氧化物能否跟水直接化合,一般的方法是看对应碱的溶解性,对应的碱是可溶的或微溶的,则该碱性氧化物能与水直接化合。如: Na2O+H2O=2NaOH. 对应的碱是难溶的,则该碱性氧化物不能跟水直接化合。如CuO、Fe2O3都不能跟水直接化合。
6.酸性氧化物+水→含氧酸. 除SiO2外,大多数酸性氧化物能与水直接化合成含氧酸。如: CO2+H2O=H2CO3
7.碱性氧化物+酸性氧化物→含氧酸盐 Na2O+CO2=Na2CO3。大多数碱性氧化物和酸性氧化物可以进行这一反应。其碱性氧化物对应的碱碱性越强,酸性氧化物对应的酸酸性越强,反应越易进行。
8.氨+氯化氢→氯化铵 氨气易与氯化氢化合成氯化铵。如: NH3+HCl=NH4Cl
9.硫和氧气在点燃的情况下形成二氧化硫 S+O2 SO2
SO2
10.特殊化合反应
公式 A+B+…+N→X(有些化合反应属于燃烧反应)
例如:铁+氧气 四氧化三铁 3Fe+2O2
四氧化三铁 3Fe+2O2 Fe3O4
Fe3O4
注意:不是所有的化合反应都是放热反应。
特征:多变一
表达式:a+b=ab
初中常见化合反应:
1.金属+氧气→金属氧化物
很多金属都能跟氧气直接化合。例如常见的金属铝接触空气,它的表面便能立即生成一层致密的氧化膜,可阻止内层铝继续被氧化。4Al+3O2=2Al2O3
2.非金属+氧气→非金属氧化物 经点燃,许多非金属都能在氧气里燃烧,如:C+O2
 CO2
CO2 3.金属+非金属→无氧酸盐 许多金属能与非金属氯、硫等直接化合成无氧酸盐。如 2Na+Cl2
 2NaCl
2NaCl 4.氢气+非金属→气态氢化物 因氢气性质比较稳定,反应一般需在点燃或加热条件下进行。如 2H2+O2
 2H2O
2H2O 5.碱性氧化物+水→碱. 多数碱性氧化物不能跟水直接化合。判断某种碱性氧化物能否跟水直接化合,一般的方法是看对应碱的溶解性,对应的碱是可溶的或微溶的,则该碱性氧化物能与水直接化合。如: Na2O+H2O=2NaOH. 对应的碱是难溶的,则该碱性氧化物不能跟水直接化合。如CuO、Fe2O3都不能跟水直接化合。
6.酸性氧化物+水→含氧酸. 除SiO2外,大多数酸性氧化物能与水直接化合成含氧酸。如: CO2+H2O=H2CO3
7.碱性氧化物+酸性氧化物→含氧酸盐 Na2O+CO2=Na2CO3。大多数碱性氧化物和酸性氧化物可以进行这一反应。其碱性氧化物对应的碱碱性越强,酸性氧化物对应的酸酸性越强,反应越易进行。
8.氨+氯化氢→氯化铵 氨气易与氯化氢化合成氯化铵。如: NH3+HCl=NH4Cl
9.硫和氧气在点燃的情况下形成二氧化硫 S+O2
 SO2
SO210.特殊化合反应
公式 A+B+…+N→X(有些化合反应属于燃烧反应)
例如:铁+氧气
 四氧化三铁 3Fe+2O2
四氧化三铁 3Fe+2O2 Fe3O4
Fe3O4概念:用文字表示化学反应的式子
文字表达式的书写步骤:
(1)写:根据反应事实写出反应物和生成物
(2)注:注明反应条件:[点燃,加热,光照,通电等]
文字表达式的书写步骤:
(1)写:根据反应事实写出反应物和生成物
(2)注:注明反应条件:[点燃,加热,光照,通电等]
物理性质:
1. 概念: 不需要发生化学变化就直接表现出来的性质。
2. 实例:在通常状态下,氧气是一种无色,无味的气体。
3. 物质的物理性质:如颜色,状态,气味,熔点,沸点,硬度等。
化学性质:
1. 概念:物质在化学变化中表现出来的性质,如铁在潮湿的空气中生成铁锈,铜能在潮湿的空气中生成铜绿。化学性质只能通过化学变化表现出来。
物质的性质和用途的关系:
若在使用物质的过程中,物质本身没有变化,则是利用了物质的物理变化,物质本身发生了变化,变成了其他物质,则是利用了物质的化学性质。物质的性质与用途的关系:物质的性质是决定物质用途的主要因素,物质的用途体现物质的性质。
物质的性质与物质的变化的区别和联系
| 物质的性质 | 物质的变化 | |
| 区别 | 物质的性质是指物质的特有属性,不同的物质其属性不同,是变化的内因 | 物质的变化是一个过程,是有序的,动态的,性质的具体体现 |
| 联系 | 物质的性质决定了它能发生的变化,而变化又是性质的具体表现 | |
判断是“性质”还是“变化”:
判断某种叙述是指物质的“性质”还是“变化”时,首先要准确把握它们的区别和联系,若叙述中有“能”,“难”,“易”,“会”,“就”等词语,往往指性质,若叙述中有“已经”,“了”,“在”等词语,往往指物质的变化。
有关描述物质的词语:
1. 物理性质:
(1)熔点
物质从固态变成液态叫熔化,物体开始熔化时的温度叫熔点。
(2)沸点
液体沸腾时的温度叫沸点。
(3)压强
物体在单位面积上所受到的压力叫压强。
(4)密度
物质在单位体积上的质量叫密度,符号为p。
(5)溶解性
一种物质溶解在另一种物质里的能力,称为这种物质的溶解性。溶解性跟溶质、溶剂的性质及温度等因素有关。
(6)潮解
物质在空气中吸收水分,表面潮湿并逐渐溶解的现象。如固体、NaOH,精盐在空气中易潮解。
(7)挥发性
物质由固态或液态变为气体或蒸气的过程二如浓盐酸具有挥发性,可挥发出氯化氢气体
(8)导电性
物体传导电流的能力叫导电性:固体导电靠的是白由移动的电子,溶液导电依靠的是自由移动的离子
(9)导热性
物体传导热量的能力叫导热性。一般导电性好的材料,其导热性也好。
(10)延展性
物体在外力作用下能延伸成细丝的性质叫延性;在外力作用下能碾成薄片的性质叫展性。二者合称为延展性,延展性一般是金属的物理性质之一。
2. 化学性质:
(1)助燃性物质在一定的条件下能进行燃烧的性质。如硫具有可燃性。
(2)助燃性物质能够支持燃烧的性质。如氧气具有助燃性
(3)氧化性在氧化还原反应中,能够提供氧元素的性质
(4)还原性在氧化还原反应中,能够夺取含氧化合物中氧元素的性质,初中化学常见的还原性物质(即还原剂)有 H2、CO、C。
(5)酸碱性酸碱性是指物质能够使酸碱指示剂变色的性质: 酸性溶液能使紫色石蕊变红,碱性溶液能使紫色石蕊变蓝。
(6)稳定性物质不易与其他物质发生化学反应或自身不易发生分解反应的性质,如稀有气体化学性质稳定。
(7)风化结晶水合物(如Na2CO3·10H2O)在干燥的环境中失去结晶水的性质。
发现相似题
与“阅读下列科普短文,然后回答问题.臭氧的化学式是O3,在通常...”考查相似的试题有:
- 近年来,福州市作出了限放烟花爆竹规定,其原因主要是燃放烟花爆竹会( )A.污染水源B.产生温室效应C.污染土壤D.污染空气...
- 正确写出下列反应的化学方程式(1)用H2做“零污染汽车”燃料的化合反应:______.(2)水参加的分解反应:______.(3)剧烈燃...
- (1)用数字和化学符号填空:①2个钙离子:______; ②氧分子:______;(2)用化学方程式填空:①实验室制取二氧化碳气体:____...
- 某些化学反应在一定条件下才能发生,请你利用所提供的物质,写出符合下列反应条件的化学方程式:O2,H2O,H2O2,KMnO4,Fe(...
- A、B、C三个集气瓶中只盛有氧气、空气、二氧化碳中的某一种气体,分别将集气瓶按照下图方式倒扣住蜡烛和白磷.(1)若A瓶中是...
- 根据题中信息,写出有关的化学方程式.(1)查获的大麻(化学式是C21H30O2)等毒品常在空气中焚烧销毁.______.(2)一些豆...
- (1)2008年5月16日,奥运火炬在英雄城南昌传递.“祥云”火炬中的燃料含有C3H8,它燃烧的化学方程式是______.(2)某化工厂产...
- 电子消毒橱是饮食行业中常用的设备,其中的臭氧(O3)发生器在消毒过程中,将空气中的氧气转化为臭氧.下列有关说法中正确的...
- 过氧乙酸(CH3C000H)与双氧水(H202)是常见的医用消毒剂.过氧乙酸易分解,分解产物是醋酸和氧气,过氧乙酸具有很强的消毒...
- 善于梳理化学知识,是学好化学的一种方法.下面是某同学用连线的方式对某一主题内容进行归纳的情况,其中有错误的一组是( )...