本试题 “某化学反应2A(g)B(g)+D(g)在四种不同条件下进行,反应器均为相同恒容密闭容器,B、D起始浓度为0.反应物A的浓度(mol•L-1间(min)的变化情况如下表:...” 主要考查您对勒夏特列原理
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 勒夏特列原理
原理内容:
如果改变影响平衡的一个条件(如浓度、压强、温度),平衡将向着能够减弱这种改变的方向移动。勒夏特列原理又叫平衡移动原理。
适用范围:
平衡移动原理适用于化学平衡、溶解平衡、电离平衡、水解平衡等动态平衡。
注意事项:
(1)平衡向“减弱”外界条件变化的方向移动,但不能“抵消”外界条件的变化。
(2)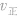 增大并不意味着平衡一定向正反应方向移动,只有
增大并不意味着平衡一定向正反应方向移动,只有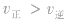 时才可以肯定平衡向正反应方向移动。
时才可以肯定平衡向正反应方向移动。
(3)当平衡向正反应方向移动时,反应物的转化率并不一定提高,生成物的体积分数也并不一定增大(因为反应物或反应混合物的总量增大了),增大一种反应物的浓度会提高另一种反应物的转化率。
(4)存在平衡且平衡发生移动时才能应用平衡移动原理。
分析思路:
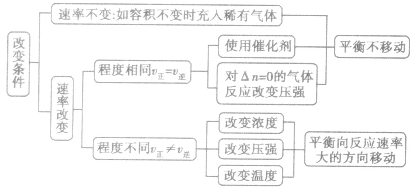
如果改变影响平衡的一个条件(如浓度、压强、温度),平衡将向着能够减弱这种改变的方向移动。勒夏特列原理又叫平衡移动原理。
适用范围:
平衡移动原理适用于化学平衡、溶解平衡、电离平衡、水解平衡等动态平衡。
注意事项:
(1)平衡向“减弱”外界条件变化的方向移动,但不能“抵消”外界条件的变化。
(2)
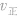 增大并不意味着平衡一定向正反应方向移动,只有
增大并不意味着平衡一定向正反应方向移动,只有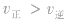 时才可以肯定平衡向正反应方向移动。
时才可以肯定平衡向正反应方向移动。 (3)当平衡向正反应方向移动时,反应物的转化率并不一定提高,生成物的体积分数也并不一定增大(因为反应物或反应混合物的总量增大了),增大一种反应物的浓度会提高另一种反应物的转化率。
(4)存在平衡且平衡发生移动时才能应用平衡移动原理。
分析思路:

发现相似题
与“某化学反应2A(g)B(g)+D(g)在四种不同条件下进行,反应...”考查相似的试题有:
- 红矾钠(重铬酸钠:Na2Cr2O7-2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作助剂,在化学工业和制药工业中...
- 甲图是NO2(g)+CO(g)CO2(g)+NO(g)反应过程能量变化示意图.一定条件下,在固定容积的密闭容器中该反应达到平衡状态....
- 在密闭容器中,反应X2(g)+Y2(g)⇌2XY(g);△H<0,达到甲平衡.在仅改变某一条件后,达到乙平衡,图中对此过程的分析正确...
- 下列事实不能用勒夏特列原理解释的是[ ]A.黄绿色的氯水光照后颜色变浅B.在硫酸亚铁溶液中,加入铁粉以防止氧化变质C.生产...
- 在容积不变的密闭容器中存在如下反应:2A(g)+B(g)⇌3C(g);△H<0某研究小组研究了其他条件不变时,改变某一条件对上述反...
- 冰醋酸CH3COOH沸点较高(117.9℃),且能形成二聚物(CH3COOH)2,其反应式为2CH3COOH(g)⇌(CH3COOH)2(g) (正反应为放热...
- 一定条件下,某反应的化学方程式为:CO2+NO⇌NO2+CO,下列说法正确的是( )A.升高温度,正反应速率增大,逆反应速率减少B....
- 合成氨对工、农业生产和国防都有重要意义。已知:25℃时,N2(g)+3H2(g)2NH3(g);△H
- 下列事实不能用勒夏特列原理解释的是[ ]A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率B.合成氨工厂通常采...
- 下列各组物质的变化,不能用勒夏特列原理解释的是[ ]A.新制的氯水在光照条件下颜色变浅B.NO2和N2O4的混合体系,增大压强(压...