本试题 “下列说法中不正确的是( )①溶液都是无色透明、均一、稳定的混合物.②同种溶质的饱和溶液一定比它的不饱和溶液浓.③糖水是溶液,盐水是溶液,混合在一起,既...” 主要考查您对溶解
溶液的定义、组成及特征
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶解
- 溶液的定义、组成及特征
溶解定义:
广义上说,超过两种以上物质混合而成为一个分子状态的均匀相的过程称为溶解。而狭义的溶解指的是一种液体对于固体/液体/或气体产生化学反应使其成为分子状态的均匀相的过程称为溶解。一种物质(溶质)分散于另一种物质(溶剂)中成为溶液的过程。如食盐或蔗糖溶解于水而成水溶液。溶液并不一定为液体,可以是固体、液体、气体。比如均匀的合金和空气都可以称为溶液。当两种物质互溶时,一般把质量大的物质称为溶剂(如有水在其中,一般习惯将水称为溶剂)。
溶解过程:
物质溶解于水,通常经过两个过程:一种是溶质分子(或离子)的扩散过程,这种过程为物理过程,需要吸收热量;另一种是溶质分子(或离子)和溶剂(水)分子作用,形成溶剂(水合)分子(或水合离子)的过程,这种过程是化学过程,放出热量。当放出的热量大于吸收的热量时,溶液温度就会升高,如浓硫酸、氢氧化钠等;当放出的热量小于吸收的热量时,溶液温度就会降低,如硝酸铵等;当放出的热量等于吸收的热量时,溶液温度不变,如盐、蔗糖。
固体、液体及气体溶解的对比分析:
(1)固体溶解
固体溶解时,常需要粉碎,加热,震荡,搅拌等方法加速溶解。

(2)液体溶解
一般液体溶解时,将液体加水搅拌均匀。
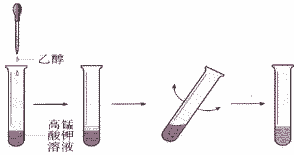
(3)气体溶解
气体溶解时,对于溶解度小的气体要把导管插入水中,极易溶于水的气体,应在导管末端插一倒置的漏斗,漏斗边缘接触水。
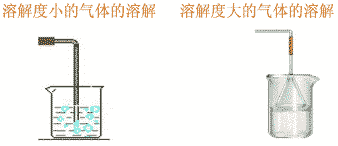
溶解性应用:
1、是指物质在溶剂里溶解能力的大小。
2、溶解性是物理性质,溶解是物理变化。
3、溶解性是由20℃时某物质的溶解度决定的。(固体)
4、利用溶解性可有以下应用:
(1)判断气体收集方法
可溶(易溶)于水的气体不能用排水取气法。
如:CO2而H2,O2溶解性不好,可用排水取气法。
(2)判断混合物分离方法
两种物质在水中溶解性明显不同时,可用过滤法分离。
如:KNO3(易溶)与CaCO3(难溶)可用过滤法分离
而C与MnO2二者均不溶NaClKNO3均易溶,都不能用过滤法分离。
溶解度算法=溶质质量/溶剂质量(通常为水)
单位: g/100g水。
广义上说,超过两种以上物质混合而成为一个分子状态的均匀相的过程称为溶解。而狭义的溶解指的是一种液体对于固体/液体/或气体产生化学反应使其成为分子状态的均匀相的过程称为溶解。一种物质(溶质)分散于另一种物质(溶剂)中成为溶液的过程。如食盐或蔗糖溶解于水而成水溶液。溶液并不一定为液体,可以是固体、液体、气体。比如均匀的合金和空气都可以称为溶液。当两种物质互溶时,一般把质量大的物质称为溶剂(如有水在其中,一般习惯将水称为溶剂)。
溶解过程:
物质溶解于水,通常经过两个过程:一种是溶质分子(或离子)的扩散过程,这种过程为物理过程,需要吸收热量;另一种是溶质分子(或离子)和溶剂(水)分子作用,形成溶剂(水合)分子(或水合离子)的过程,这种过程是化学过程,放出热量。当放出的热量大于吸收的热量时,溶液温度就会升高,如浓硫酸、氢氧化钠等;当放出的热量小于吸收的热量时,溶液温度就会降低,如硝酸铵等;当放出的热量等于吸收的热量时,溶液温度不变,如盐、蔗糖。
固体、液体及气体溶解的对比分析:
(1)固体溶解
固体溶解时,常需要粉碎,加热,震荡,搅拌等方法加速溶解。

(2)液体溶解
一般液体溶解时,将液体加水搅拌均匀。

(3)气体溶解
气体溶解时,对于溶解度小的气体要把导管插入水中,极易溶于水的气体,应在导管末端插一倒置的漏斗,漏斗边缘接触水。

溶解性应用:
1、是指物质在溶剂里溶解能力的大小。
2、溶解性是物理性质,溶解是物理变化。
3、溶解性是由20℃时某物质的溶解度决定的。(固体)
| (20℃) | 难溶(不溶) | 微溶 | 可溶 | 易溶 |
| <0.01g | 0.01g~1g | 1 g~10g | >10g |
4、利用溶解性可有以下应用:
(1)判断气体收集方法
可溶(易溶)于水的气体不能用排水取气法。
如:CO2而H2,O2溶解性不好,可用排水取气法。
(2)判断混合物分离方法
两种物质在水中溶解性明显不同时,可用过滤法分离。
如:KNO3(易溶)与CaCO3(难溶)可用过滤法分离
而C与MnO2二者均不溶NaClKNO3均易溶,都不能用过滤法分离。
溶解度算法=溶质质量/溶剂质量(通常为水)
单位: g/100g水。
溶液的概念:
一种或几种物质分散到另一种物质中,形成均一的,稳定的混合物,叫做溶液
溶液的组成:
(1)溶液由溶剂和溶质组成溶质:被溶解的物质溶剂:
溶液质量=溶剂质量+溶质质量
溶液的体积≠溶质的体积+溶剂的体积
(2)溶质可以是固体(氯化钠、硝酸钾等)、液体(酒精、硫酸等)或气体(氯化氢、二氧化碳等),一种溶液中的溶质可以是一种或多种物质。水是最常用的溶剂,汽油、洒精等也可以作为溶剂,如汽油能够溶解油脂,洒精能够溶解碘等。
溶液的特征:
均一性:溶液中各部分的性质都一样;
稳定性:外界条件不变时,溶液长时间放置不会分层,也不会析出固体溶质
对溶液概念的理解:
溶液是一种或儿种物质分散到另一种物质里.形成的均一、稳定的混合物。应从以下几个方面理解:
(1)溶液属于混合物;
(2)溶液的特征是均一、稳定;
(3)溶液中的溶质可以同时有多种;
(4)溶液并不一定都是无色的,如CuSO4溶液为蓝色;
(5)均一、稳定的液体并不一定郡是溶液,如水;
(6)溶液不一定都是液态的,如空气。
溶液与液体
(1)溶液并不仅局限于液态,只要是分散质高度分散(以单个分子、原子或离子状态存在)的体系均称为溶液。如锡、铅的合金焊锡,有色玻璃等称为固态溶液。气态的混合物可称为气态溶液,如空气。我们通常指的溶液是最熟悉的液态溶液,如糖水、盐水等。
(2)液体是指物质的形态之一。如通常状况下水是液体,液体不一定是溶液。
3. 溶液中溶质、溶剂的判断
(1)根据名称。溶液的名称一般为溶质的名称后加溶剂,即溶质在前,溶剂在后。如食盐水中食盐是溶质,水是溶剂,碘酒中碘是溶质,酒精是溶剂。
(2)若是固体或气体与液体相互溶解成为溶液。一般习惯将固体或气体看作溶质,液体看作溶剂。
(3)若是由两种液体组成的溶液,一般习惯上把量最多的看作溶剂,量少的看作溶质。
(4)其他物质溶解于水形成溶液时。无论,水量的多少,水都是溶剂。
(5)一般水溶液中不指明溶剂,如硫酸铜溶液,就是硫酸铜的水溶液,蔗糖溶液就是蔗糖的水溶液,所以未指明溶剂的一般为水。
(6)物质在溶解时发生了化学变化,那么在形成的溶液中,溶质是反应后分散在溶液中的生成物。如 Na2O,SO3分别溶于水后发生化学反应,生成物是 NaOH和H2SO4,因此溶质是NaOH和H2SO4,而不是 Na2O和SO3;将足量锌粒溶于稀硫酸中所得到的溶液中,溶质是硫酸锌(ZnSO4),若将蓝矾(CuSO4·5H2O) 溶于水,溶质是硫酸铜(CuSO4),而不是蓝矾。
溶液的导电性:
探究溶液导电性的实验:
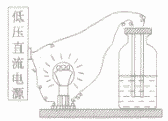
用如图所示的装置试验一些物质的导电性。可以养到蒸馏水、乙醉不导电,而盆酸、硫酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶液、碳酸钠溶液均能导电。
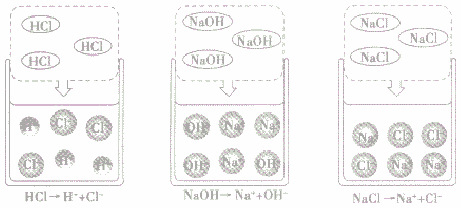
酸、碱、盐溶液导电的原因:
酸、碱、盐溶于水,在水分子作用下,电离成自由移动的带正(或负)电的阳(或阴)离子(如下图所示)。因此酸、碱、盐的水溶液都能导电,导电的原因是溶液中存在自由移动的离子,而蒸馏水和乙醇中不存在自由移动的离子。
发现相似题
与“下列说法中不正确的是( )①溶液都是无色透明、均一、稳定的...”考查相似的试题有:
- 某同学对所学部分化学知识归纳如下,其中有错误的一组是( )A.物质性质与用途:O2助燃--气焊切割金属H2O2:分解放出O2--实...
- 碘酒是一种常见的外科消毒剂,其溶剂是______,欲将600C时接近饱和的硝酸钾溶液变成饱和溶液,可以采用的方法是______(2)__...
- 把少量下列物质分别加入到水中,充分搅拌,不能形成溶液的是A.食盐B.蔗糖C.植物油D.纯碱
- 人体结石有多种,其中一种含有较多的草酸钙(CaC2O4),CaC2O4中碳元素的化合价是( )A.+1B.+2C.+3D.+4
- 下列说法中不正确的是[ ]A.葡萄糖、植物油、蛋白质都可溶于水形成溶液B.浓溶液稀释过程中,溶质的质量保持不变C.析出晶体...
- 下列物质中属于溶液的是[ ]A.澄清石灰水B.水银C.牛奶D.冰水
- 下列有关溶液的叙述正确的是[ ]A.溶液不一定是均匀、稳定的混合物B.向水中加入少量蔗糖固体可增强溶液的导电性C.少量的固...
- 下列物质放入水中,不能形成溶液的是( )A.食盐B.食醋C.纯碱D.花生油
- 2009年4月22日是“世界水日”。水与人类的生活和生产密切相关。 请回答以下问题:(1)生理盐水中的溶剂是 。(2)保护水环境、...
- 下列物质中,放入水里不能形成溶液的是[ ]A.花生油B.白糖C.白醋D.食盐