本试题 “A2+B2═2AB的反应历程可以看作如下(△H表示该过程的能量变化):Ⅰ.A2═A+A△H1Ⅱ.B2═B+B△H2Ⅲ.A+B═AB△H3则下列说法中正确的是( )A.当△H3+(△H1+△H2)>0时,...” 主要考查您对吸热反应、放热反应
焓变、反应热
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 吸热反应、放热反应
- 焓变、反应热
吸热反应:
吸收热量的反应,即生成物的总能量大于反应物的总能量,反应需要吸收能量
放热反应:
放出热量的反应,即生成物的总能量小于反应物的总能量,反应释放出能量
放热反应和吸热反应的比较:
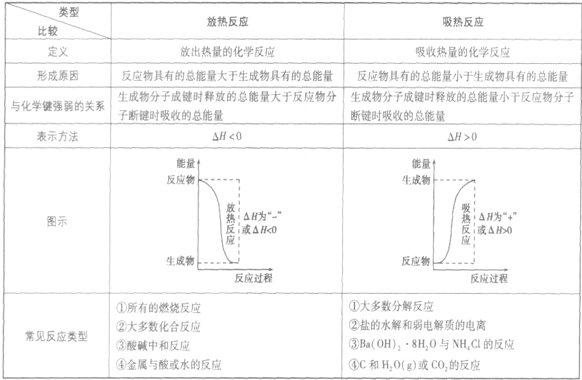
吸收热量的反应,即生成物的总能量大于反应物的总能量,反应需要吸收能量
放热反应:
放出热量的反应,即生成物的总能量小于反应物的总能量,反应释放出能量
放热反应和吸热反应的比较:

反应热,焓变:
化学能可以转化为热能、电能和光能等,化学反应中的能量变化,通常主要表现为热量的变化。
1.定义:在化学反应过程中,当生成物和反应物具有相同温度时所放出或吸收的热量,通常叫做化学反应的反应热。在恒温、恒压条件下,化学反应过程中吸收或放出的热量称为反应的焓变。
2.符号:△Ⅳ
3.单位:kJ·mol-1
4.产生原因:化学反应过程中旧键断裂吸收的总能量与新键形成释放的总能量不相等,故化学反应均伴随着能量变化——吸热或放热。
5.表示方法:放热反应的△H<0,吸热反应的△H>0.
化学能可以转化为热能、电能和光能等,化学反应中的能量变化,通常主要表现为热量的变化。
1.定义:在化学反应过程中,当生成物和反应物具有相同温度时所放出或吸收的热量,通常叫做化学反应的反应热。在恒温、恒压条件下,化学反应过程中吸收或放出的热量称为反应的焓变。
2.符号:△Ⅳ
3.单位:kJ·mol-1
4.产生原因:化学反应过程中旧键断裂吸收的总能量与新键形成释放的总能量不相等,故化学反应均伴随着能量变化——吸热或放热。
5.表示方法:放热反应的△H<0,吸热反应的△H>0.
发现相似题
与“A2+B2═2AB的反应历程可以看作如下(△H表示该过程的能量变化)...”考查相似的试题有:
- 水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s) + H2O(g)CO (g) +H2(g) △H(1)写出该反应的平衡...
- 在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如下图所示。下列说法不正确的是[ ]A. 该反应是...
- 下列说法正确的是[ ]A.需要加热才能发生的反应一定是吸热反应B.化学反应中的能量变化都表现为热量变化C.任何放热反应在常温下...
- 为了研究化学反应X+Y=Z的能量变化情况,某同学设计了右图所示装置.当向盛有X的试管中滴加试剂Y时,看到U型管中甲处液面下降...
- 250℃和1.01×105Pa时,反应2N2O5(g)═4NO2(g)+O2(g)△H=+56.76kJ/mol,自发进行的原因是( )A.是吸热反应B.是放热反应C...
- 某反应的反应过程和能量变化如图所示,下列有关该反应的叙述正确的是( )A.该反应的反应热△H<0B.反应物的总能量低于生成...
- 已知热化学方程式:H2(g)+1/2O2(g)=H2O(l) △H="-285.8KJ/mol" 当lg液态水变为水蒸汽时,其热量变化是A.吸热88kJB.吸热2.44J...
- 甲烷和氨在国民经济中占有重要地位。(1)制备合成氨原料气H2,可用甲烷蒸汽转化法,主要转化反应如下:CH4(g) + H2O(g) CO(g...
- 已知16g硫变成硫蒸汽需要吸收akJ的热量,而2mol硫蒸汽完全燃烧会放出bkJ的热量,则下列热化学方程式正确的是A.S(s)+ O2(g)=...
- (8分)甲醇是一种优质燃料,可制作燃料电池。(1)工业上可用下列两种反应制备甲醇:①CO(g) + 2H2(g)CH3OH(g) ΔH1 ②CO2(g)+3H...