本试题 “下列说法中正确的是( )A.81Br原子的中子数比电子数多11B.金属原子的核外电子在金属晶体中都是自由电子C.NaCl和SiO2晶体溶化时,克服粒子间作用力的类型...” 主要考查您对原子核的组成及组成粒子间的关系
金属晶体
元素周期表
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原子核的组成及组成粒子间的关系
- 金属晶体
- 元素周期表
构成原子的三种微粒的比较:
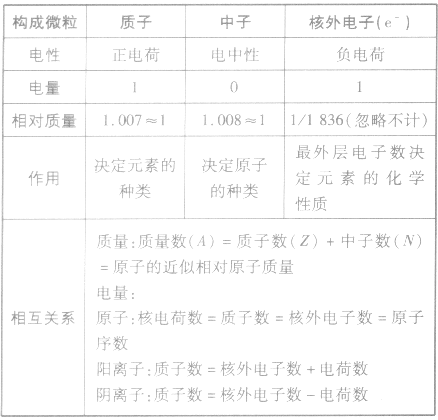
原子的构成:
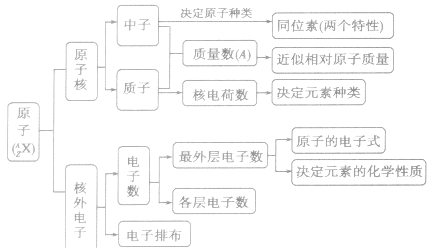
金属晶体:
通过金属离子与自由电子间的较强作用(金属键)形成的单质晶体,熔沸点(除Hg外)高,导热性、延展性良好,易导电,硬度一般较大。
如:金属单质金属晶体原子堆积模型:
(1)简单立方堆积 (2)体心立方堆积 (3)六方最密堆积和面心立方最密堆积
通过金属离子与自由电子间的较强作用(金属键)形成的单质晶体,熔沸点(除Hg外)高,导热性、延展性良好,易导电,硬度一般较大。
如:金属单质金属晶体原子堆积模型:
(1)简单立方堆积 (2)体心立方堆积 (3)六方最密堆积和面心立方最密堆积
晶体的基本类型与性质:
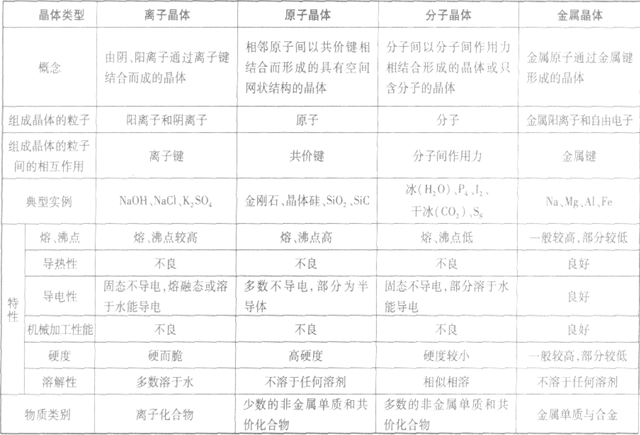
金属晶体的原子堆积模型:
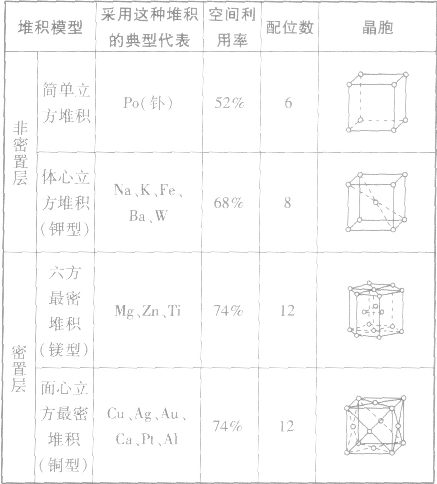
元素周期表编排原则:
(1)把电子层数相同的各种元素按原子序数递增的顺序从左至右排成横行。
(2)把最外层电子数相同的元素按电子层数递增的顺序由上到下排列成纵行。
注意:①元素周期表是元素周期律的具体表现形式,它反映了元素之间相互联系的规律。
②历史上第一个元素周期表是1869年俄国化学家门捷列夫在前人探索的基础上排成的,他将元素按相对原子质量由小到大依次排列,并将化学性质相似的元素放在一个纵行。
元素周期表的结构:
(1)周期
①周期的含义在元素周期表中,把电子层数相同的元素,按原子序数递增的顺序从左到右排成横行,这样每个横行为一个周期。现在使用的元素周期表有7个横行,即7 个周期。
②周期的划分
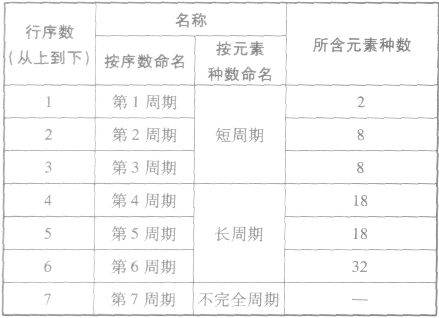
(2)族
①族的含义在周期表中,把不同横行(即周期)中最外层电子数相同的元素,按电子层数递增的顺序由上到下排成纵行,除第8、9、10三个纵行叫做第Ⅷ族外,其余15个纵行,每个纵行为一族。现在使用的元素周期表有18 个纵行,它们被划分为16个族。
②族的划分
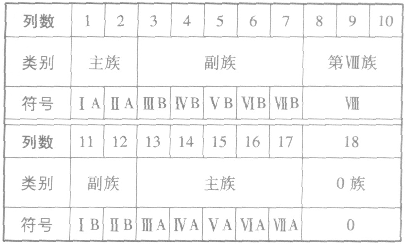
(3)元素周期表中主族元素金属性和非金属性的递变
发现相似题
与“下列说法中正确的是( )A.81Br原子的中子数比电子数多11B....”考查相似的试题有:
- 原子结构模型的演变研究中,首先发现电子的科学家是( )A.道尔顿B.汤姆生C.卢瑟福D.玻尔
- 只含非金属元素的晶体描述正确的是A.有可能是金属晶体B.有可能是离子晶体C.一定是分子晶体D.一定不是原子晶体
- Ⅰ铂(Pt)单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。(1...
- [选修物质结构].铁是地球表面最丰富的金属之一,能形成多种配合物,铁系催化剂是工业生产中常用的催化剂。(1)合成氨工业...
- 下列说法中正确的是( )A.元素周期表中元素排序的依据是元素的相对原子质量B.元素周期表中元素排序的依据是原子的核电荷数...
- 已知X 、Y、 Z 、W、 N是短周期中原子序数依次增大的五种主簇元素,通常情况下Y形成的单质为固体,其余的为气体。N是第三周期...
- 某同学设计了一套实验方案研究第11-18号部分元素的性质变化实验实验目的实验内容Ⅰ探究Mg、Al的金属性强弱1将除去氧化膜的镁条...
- 关于元素周期表中的16号元素的说法不正确的是( )A.最高正价是+6价B.最低负价为-2价C.该元素位于第三周期D.该元素属于ⅤA...
- 现代医学证明,硒是人体中14种必需的营养元素之一,缺硒与贫血、冠心病、不孕症、癌症等疾病直接相关.因此,硒被誉为“生命的...
- 医学研究证明,用放射性13553I治疗肿瘤可收到一定疗效,下列有关13553I叙述正确的是[ ]A.13553I是碘的一种同素异形体C.1355...