本试题 “下列关于有机化合物的说法正确的是[ ]A.甲烷和乙烯都可以与氯气反应B.异丁烷与2-甲基丁烷互为同分异构体C.油脂和淀粉都是高分子化合物D.乙烯可以与氢气发...” 主要考查您对甲烷
乙烯
苯
同分异构体
天然有机高分子化合物
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 甲烷
- 乙烯
- 苯
- 同分异构体
- 天然有机高分子化合物
(1)结构式:
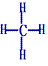 、球棍模型:
、球棍模型:  、比例模型:
、比例模型: 
空间构型为正四面体。
(2)物理性质:无色无味的气体,密度0.717g/L,记忆溶于水。
(3)化学性质:通常情况下甲烷比较稳定,与高锰酸钾等强氧化剂不反应,与强酸强碱不反应,可发生氧化反应、取代反应
①氧化反应:CH4+O2
 CO2+2H2O
CO2+2H2O ②取代反应:CH4+Cl2
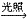 CH3Cl+HCl,甲烷在光照条件下反应,现象:试管内气体颜色逐渐变浅,试管壁上有油状液滴,试管中有少量白雾。甲烷中四个氢原子都可以与氯气发生取代,甲烷的4中氯代产物都不溶于水,常温下,一氯甲烷是气体,其他都为液体,三氯甲烷俗称氯仿。
CH3Cl+HCl,甲烷在光照条件下反应,现象:试管内气体颜色逐渐变浅,试管壁上有油状液滴,试管中有少量白雾。甲烷中四个氢原子都可以与氯气发生取代,甲烷的4中氯代产物都不溶于水,常温下,一氯甲烷是气体,其他都为液体,三氯甲烷俗称氯仿。 甲烷与氯气等卤素单质反应的注意事项:
1.反应条件为光照,在室温或暗处不发生反应,但不能用强光直接照射,以免引起爆炸。
2.甲烷与溴蒸气、碘蒸气等纯卤素也能发生类似反应,但不能与溴水、碘水发生反应。
3.甲烷与氯气的反应是一种连锁反应,不会停留在某一步,因此产物一般是五种物质的混合物。
4.CH4与Cl2在光照条件反应,生成物中HCl的物质的量最多。
5.1mol有机物CxHy与Cl2发生完全取代反应时,消耗Cl2的物质的量为ymol。
原子共面的判断方法:
判断有机物分子中的原子是否共面,首先要熟悉常见的分子构型。如甲烷分子(CH4)为正四面体结构,其分子中最多有三个原子共面;乙烯分子 (CH2=CH2)中的所有原子共面;苯分子(C6H6)中的所有原子共面。在判断有机物分子中原子共面情况时,把要分析的分子看做是简单的常见分子的衍生物,即复杂问题简单处理
(1)在甲烷分子中,一个碳原子和任意两个氢原子可确定一个平面,即甲烷分子中有且只有三个原子共面。当甲烷分子中的某个氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在原来的平面上。
(2)乙烯分子中所有原子在同一平面内,键角为 120。。当乙烯分子中的某个氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯分子所在的平面内。
(3)苯分子中所有原子在同一个平面内,键角为 120。。当苯分子中的某个氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在苯分子所在的平面内。说明有机化合物分子中的单键(包括碳碳单键、碳氢单键、碳氧单键等)可以旋转;而双键、三键不能旋转
乙烯的结构和性质:
1.分子结构:
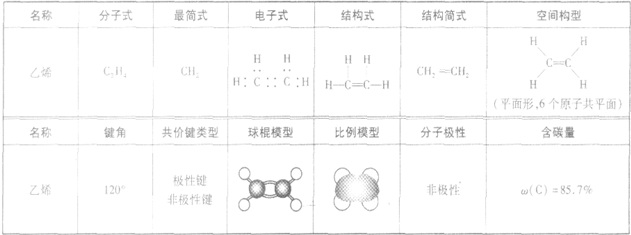
2.物理性质:
在通常状况下,乙烯是无色、稍有气味的气体,难溶于水,易溶于乙醇、乙醚等有机溶剂,密度(标准状况时为1.25g·L-1)比空气略小,因此实验室制取乙烯不用排空气法收集,而用排水法收集。
3.化学性质:
由于碳碳双键中的一个键易断裂,刚此乙烯的性质比较活泼,能发生加成、加聚反应,能使溴水和KMnO4溶液(酸性)褪色。
(1)乙烯易发生氧化反应
①乙烯的燃烧
乙烯在氧气或空气中易燃烧,完全燃烧生成CO2和H2O,反应的化学方程式为:
乙烯含碳量比较高,在一般情况下燃烧不是很充分,因此火焰明亮且伴有黑烟。
②乙烯的催化氧化

③乙烯能被酸性KMnO4溶液氧化
乙烯使酸性KMnO4溶液褪色的实质是乙烯被酸性KMnO4溶液氧化成二氧化碳和水。
(2)乙烯能发生加成反应
有机物分子中不饱和碳原子与其他原子(或原子团) 直接结合生成新的化合物的反应叫做加成反应。
乙烯使溴的四氯化碳溶液褪色的实质是乙烯与溴单质发生加成反应生成了1,2一二溴乙烷,反应的化学方程式为: 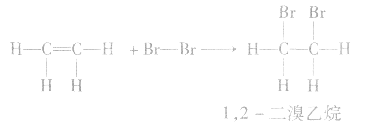
通常简写为
因此,可用溴水或溴的四氯化碳溶液鉴别乙烯和甲烷、乙烷等烷烃,也可用于除去甲烷中混有的乙烯。
(3)加聚反应在一定条件(温度、压强、催化剂)下,乙烯能发生加聚反应:
由相对分子质量小的化合物(单体)分子互相结合成相对分子质量很大的高分子的反应叫做聚合反应。由一种或多种不饱和化合物(单体)分子通过不饱和键互相加成而聚合成高分子化合物的反应叫做加成聚合反应,简称加聚反应。
乙烯的鉴别和除杂:
1.乙烯和其他物质的鉴别利用被鉴别物质性质的差异进行区分,要求操作简单、安全,现象明显,结论准确,以乙烷与乙烯的鉴别为例。操作:将两种气体分别通人酸性KMnO4溶液中。现象:一种气体使酸性KMnO4溶液褪色,一种气体不能使酸性KMnO4溶液褪色。结论:使酸性KMnO4溶液褪色者为乙烯,不能使酸性KMnO4溶液褪色者为乙烷.
2.除杂质乙烯除杂要求:将杂质除净,不能引入新杂质,小能对主要成分产生不利影响。如乙烷中混有乙烯,除杂的方法是用溴水洗气,乙烯与溴发生加成反应破除去,乙烷不反应逸出。
苯的分子结构:
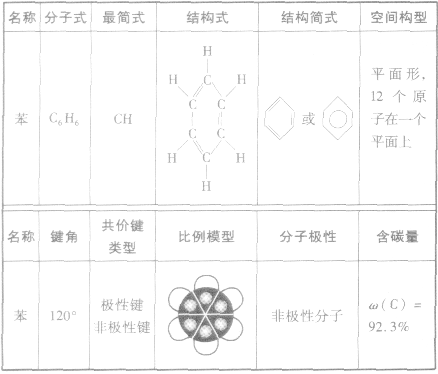
苯的性质:
1.物理性质苯通常是无色、带有特殊气味的液体,有毒,不溶于水,密度比水小,熔点为5.5℃,沸点为80.1℃。若用冰冷却,苯就会凝结成无色的晶体。
2.化学性质由于苯分子中的碳碳键是介于碳碳单键与碳碳双键之间的独特的键,所以它既有饱和烃的性质,又有不饱和烃的一些性质(苯的性质比不饱和烃的性质稳定)。
(1)氧化反应
①燃烧:苯易燃烧,所以在苯的生产、运输、贮存和使用过程中要注意防火。苯在空气中燃烧时有明亮火焰斤带有浓烟。因为苯分子含碳量高,没有得到充分燃烧,有碳单质产生,所以燃烧时有浓烟。
②苯与酸性高锰酸钾溶液不反应向试管中加入2mL苯,然后加入几滴酸性高锰酸钾溶液,振荡后静置,出现分层现象,上层(苯层)为无色,下层(水层)呈紫色。说明苯与酸性高锰酸钾溶液不反应。 
(2)取代反应
①卤代反应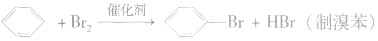
装置图如下图所示。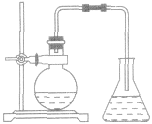
操作:把苯和少量液溴放在烧瓶里,同时加入少量铁屑作催化剂。用带导管的瓶塞塞紧瓶口,跟瓶口垂直的一段导管可以起冷凝器的作用。现象:在常温时,很快就会看到在导管口附近出现白雾(由溴遇水蒸气所形成)。反应完毕后,向锥形瓶内的液体里滴入AgNO3溶液,有浅黄色沉淀生成。把烧瓶里的液体倒在盛有冷水的烧杯里,烧杯底部有褐色不溶于水的液体(不溶于水的液体是溴苯,它是密度比水大的无色液体,由于溶解了溴而显示褐色)。
注意
a.苯只能与液溴发生取代,不与溴水反应,溴水中的溴只可被苯萃取。
b.反应中加入的催化剂是Fe屑,实际起催化作用的是FeBr3
c.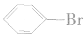 生成的是无色液体,密度大于水。
生成的是无色液体,密度大于水。
d.欲得到较纯的溴苯,可用稀NaOH溶液洗涤,以除去Br2。
②硝化反应
硝化反应是指苯分子中的氢原子被一NO2所取代的反应,也属于取代反应的范畴。 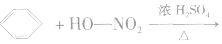

注意
a.硝酸分子中的“一NO2”原子团叫做硝基,要注意硝基(一NO2)与亚硝酸根离子(NO2-)化学式的区别。
b.硝基苯是一种带有苦杏仁味的、无色的油状液体,不溶于水,密度比水大。硝基苯有毒。
c.为便于控制温度,采用水浴加热。
(3)加成反应
苯分子中的碳碳键不是典型的碳碳双键,不容易发生加成反应(不能使溴的四氯化碳溶液褪色),但在一定条件下可与氢气发生加成反应,生成环己烷,反应的化学方程式为: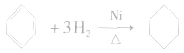
同分异构现象和同分异构体:
1.概念:化合物具有相同的分子式.但结构小同,因而产生了性质上的差异,这种现象叫同分异构现象。具有同分异构现象的化合物互为同分异构体。
2.同分异构体的基本类型
(1)碳链异构:指的是分子中碳骨架不同而产生的同分异构现象。如所有的烷烃异构都属于碳链异构。
(2)位置异构:指的是分子中官能团位置不同而产生的同分异构现象。如l一丁烯与2一丁烯、l一丙醇与2一丙醇、邻二甲苯与间二甲苯及对二甲苯。
(3)官能团异构:指的是有机物分子式相同,但具有不同官能团的同分异构体的现象。常见的官能团异构关系如下表所示: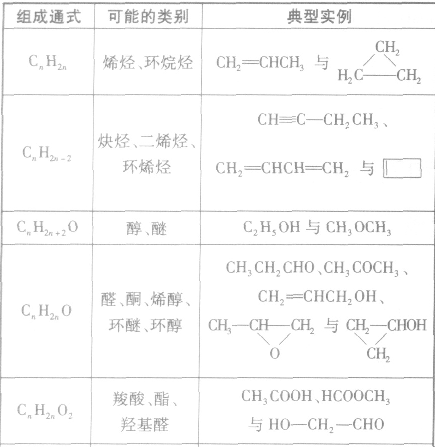
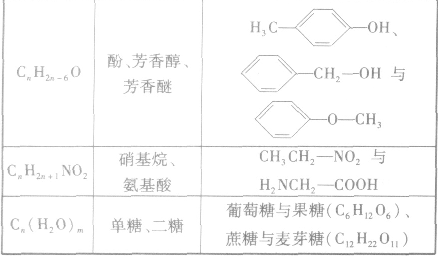
(4)顺反异构:由于碳碳双键不能旋转而导致分子中原子或原子团在空间的排列方式不同所产生的异构现象。两个相同的原子或原子团排列在双键的同一侧的称为顺式结构;两个相同的原子或原子团排列在双键的两侧的称为反式结构。如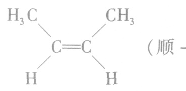
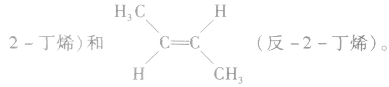
同分异构体的写法:
1.烷烃的同分异构体的写法烷烃只存在碳链异构,其书写技巧一般采用“减碳法”,可概括为“两注意,四句话”。
(1)两注意:①选择最长的碳链为主链;②找出主链的中心对称线。
(2)四句话:主链由长到短、支链由整到散,位置由心到边,排布邻、间、对。
例如,C6H14的同分异构体可按此法完整写出(为了简便,在所写结构式中删去了氢原子): 
2.烯烃的同分异构体的写法分子组成符合CnH2n的烃除烯烃外,还有环烷烃 (n≥3),并且烯烃中双键的位置不同则结构不同,有的烯烃还存在顺反异构,所以烯烃的同分异构体比烷烃复杂得多。以C5H10为例说明同分异构体的写法: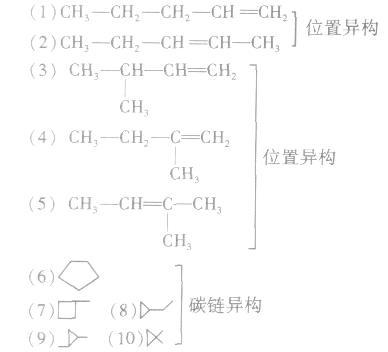
共有5种烯烃,其中(2)还存在顺反异构体,5种环烷烃,共计11种。
3.苯的同系物的同分异构体的写法由于苯环上的侧链位置不同,可以形成多种同分异构体。以C8H10为例写出其属于苯的同系物的同分异构体:
判断同分异构体数目的方法:
1.碳链异构和位置异构:先摘除官能团,书写最长碳链,移动官能团的位置;再逐渐减少碳数,移动官能团的位置。判断分子式为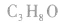 的醇的同分异构体数目:
的醇的同分异构体数目:
先摘除官能团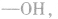 剩余
剩余 和
和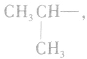 可见有两种属于醇的同分异构体;
可见有两种属于醇的同分异构体;
判断分子式为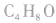 的属于醛的同分异构体数目:
的属于醛的同分异构体数目:
先摘除官能团 剩余
剩余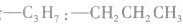 和
和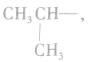 可见有两种属于醛的同分异构体。
可见有两种属于醛的同分异构体。
分子式符合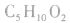 的羧酸的同分异构体数目:
的羧酸的同分异构体数目:
先摘除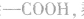 剩余
剩余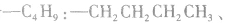
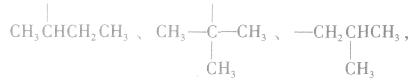 可 见有4种属于酸的同分异构体。
可 见有4种属于酸的同分异构体。
2.官能团衍变:先判断官能团的类别异构,再分别判断同种官能团的异构数目。例如分子式符合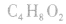 的同分异构体:符合羧酸和酯的通式,属于酸的2种(即摘除
的同分异构体:符合羧酸和酯的通式,属于酸的2种(即摘除 后剩余
后剩余 ),这样一个羧基又可以变为一个醛基和一个羟基,又可以衍变出含有两种不同含氧官能团(含有羟基和醛基)的异构体;属于酯的同分异构体:可以按羧酸和醇的碳数先分类,即酯由一个碳的酸(甲酸)和3个碳的醇(1一丙醇、2一丙醇)得到,酯由2个碳的酸(乙酸)和2个碳的醇(乙醇)得到,酯由3个碳数的酸(丙酸)和1个碳的醇(甲醇)得到,这样就会写出4种酯。
),这样一个羧基又可以变为一个醛基和一个羟基,又可以衍变出含有两种不同含氧官能团(含有羟基和醛基)的异构体;属于酯的同分异构体:可以按羧酸和醇的碳数先分类,即酯由一个碳的酸(甲酸)和3个碳的醇(1一丙醇、2一丙醇)得到,酯由2个碳的酸(乙酸)和2个碳的醇(乙醇)得到,酯由3个碳数的酸(丙酸)和1个碳的醇(甲醇)得到,这样就会写出4种酯。
3.苯环上的位置变换:例如分子式符合 的芳香酯的同分异构体:
的芳香酯的同分异构体: 
4.判断取代产物种类(“一”取代产物:对称轴法; “多”取代产物:一定一动法;数学组合法)。
5.替代法:例如二氯苯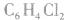 有3种,则四氯苯也为3种(将H替代C1);又如CH4的一氯代物只有一种,新戊烷C(CH3)4的一氯代物也只有一种。
有3种,则四氯苯也为3种(将H替代C1);又如CH4的一氯代物只有一种,新戊烷C(CH3)4的一氯代物也只有一种。
6.对称法(又称等效氢法):等效氢法的判断可按下列三点进行:
(1)同一碳原子上的氢原子是等效的;
(2)同一碳原子所连甲基上的氢原子是等效的;
(3)处于镜面对称位置上的氢原子是等效的(相当于平面成像时,物与像的关系)。
烃的一取代物的数目等于烃分子中等效氢的种数。
天然有机高分子化合物:
由千百个原子彼此以共价键结合形成相对分子质量特别大、具有重复结构单元的有机化合物。是由一类相对分子质量很高的分子聚集而成的化合物,也称为高分子、大分子等。一般把相对分子质量高于10000的分子称为高分子。包括天然和合成有机高分子化合物。常见天然有机高分子化合物:淀粉、纤维素、蛋白质天然橡胶等。
常见的天然有机高分子材料及其特点:
1、棉花:棉花的主要成分是纤维素,纤维素含量高达90%以上。棉纤维能制成多种规格的织物,用它制成的衣服具有耐磨并能在高温下熨烫,良好的吸湿性、透气性和穿着舒适的优点。
2、羊毛:羊毛主要南蛋白质构成,是纺织工业的重要原料,织物具有弹性好、吸湿性强、保暖性好等优点。
3、蚕丝:蚕丝是蚕结茧时形成的长纤维,也是一种天然纤维,其主要成分是蛋白质。蚕丝质轻而细长,织物光泽好、穿着舒适、手感滑顺、导热性差、吸湿透气性好。中国是世界上最早使用丝织物的国家。
4、天然橡胶:天然橡胶是指从橡胶树上采集的天然胶乳,经过凝同、干燥等加工工序制成的弹性固状物。天然橡胶是一种以聚异戊二烯为主要成分的天然高分子化合物。分子式是(C5H8)n,其成分中91%~ 94%是橡胶烃(聚异戊二烯),其余为蛋白质、脂肪酸、糖类等非橡胶物质,是应用最广的通用橡胶。
与“下列关于有机化合物的说法正确的是[ ]A.甲烷和乙烯都可以与...”考查相似的试题有:
- 下列分子中呈正四面体结构的是A.甲烷B.二氯甲烷C.三氯甲烷D.一氯甲烷
- 气态链烃A和B的分子式分别表示为CnH2n+2和CnH2n-2,在一定条件下,200 mL A和B的混合气体与同条件下100 mL氢气恰好反应转化为...
- 25℃时某气态烃与O2混合充入密闭容器中,点燃爆炸后又恢复至25℃,此时容器内压强为原来的,再经NaOH溶液处理,容器内几乎成为...
- 已知乙烯能发生以下转化:(1)乙烯的结构式为:______;B中含官能团的电子式______;C中含官能团的化学式______.(2)写出...
- 下列物质在催化剂作用下和氢气加成不能得到2-甲基戊烷的是( )A.CH3CH=CHCH(CH3)2B.CH3CH=C(CH3)CH2CH3C.(CH3)2C=CHCH2CH...
- 下列涉及的有机物及有机反应类型正确的是( )A.乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应B.除去甲烷气体中的...
- 化合物M是香豆素类天然化合物,对化合物M的叙述错误的是( )A.M的分子式为C12H10O5B.1 mol M最多可和6 mol H2发生加成反应C...
- 2006年3月英国《泰晤士报》报道说,英国食品标准局在对英国与法国贩售的芬达汽水、美年达橙汁等230种软饮料检测,发现含有高...
- 已知碳原子数≥3的烷烃均可裂化为碳原子数更少的一种烷烃和一种烯烃.含有5个碳原子的烷烃催化裂化可生成的烯烃最多有( )A....
- 下列物质中:(1)互为同分异构体的有______________;(2)互为同素异形体的有______________;(3)属于同位素的有________...