本试题 “氨广泛应用于工农业生产。(1)工业合成氨的反应:N2(g)+3H2(g)2NH3( g) △H = -a kJ . mol-1① 1/2N2(g)+3/2H2(g)NH3(g) △H = -b kJ . mol-1② 反应①的化学平衡常...” 主要考查您对氨水
合成氨(人工固氮)
陶瓷的烧制
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氨水
- 合成氨(人工固氮)
- 陶瓷的烧制
氨水:
(1) 浓氨水:易挥发,密度小于水,浓度越大,密度越小,无色,有刺激性气味的液体,熔沸点较低,能导电
(2)氨水是混合物(液氨是纯净物),其中含有3种分子(NH3、NH3·H2O、H2O)和3种离子(NH4+和OH-、极少量的H+)。
氨水的性质:
①刺激性:因水溶液中存在着游离的氨分子。
②挥发性:氨水中的氨易挥发。
③不稳定性:—水合氨不稳定,见光受热易分解而生成氨和水。
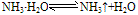
④弱碱性:氨水中一水合氨能电离出OH-,所以氨水显弱碱性,具有碱的通性:
A. 能使无色酚酞试液变红色,能使紫色石蕊试液变蓝色,能使湿润红色石蕊试纸变蓝。实验室中常见此法检验NH3的存在。
B. 能与酸反应,生成铵盐。浓氨水与挥发性酸(如浓盐酸和浓硝酸)相遇会产生白烟。

而遇不挥发性酸(如硫酸、磷酸)无此现象。实验室中可用此法检验NH3或氨水的存在。
工业上,利用氨水的弱碱性来吸收硫酸工业尾气,防止污染环境。
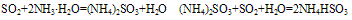
C. 沉淀性:氨水是很好的沉淀剂,它能与多种金属离子反应,生成难溶性弱碱或两性氢氧化物。例如:
生成的Al(OH)3沉淀不溶于过量氨水。
生成的白色沉淀易被氧化生成红褐色沉淀

利用此性质,实验中可制取Al(OH)3、Fe(OH)3等。
D. 络合性:氨水与Ag+、Cu2+、Zn2+三种离子能发生络合反应,当氨水少量时,产生不溶性弱碱或两性氢氧化物,当氨水过量时,不溶性物质又转化成络离子而溶解。
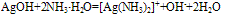
实验室中用此反应配制银氨溶液。
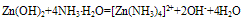
可用此反应来鉴别两性氢氧化物氢氧化铝和氢氧化锌。

现出弱的还原性,可被强氧化剂氧化。如氨水可与Cl2发生反应:
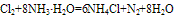
(4)氨水的保存方法:氨水对许多金属有腐蚀作用,所以不能用金属容器盛装氨水.通常把氨水盛装在玻璃容器、橡皮袋、陶瓷坛或内涂沥青的铁桶里。
氨水,液氨和一水合氨的比较:
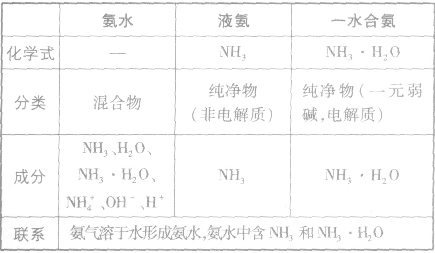
1.定义:氮的固定是指将游离态的氮转化为化合态氮的方法。
2.方法:氮的固定主要方法有:
(1)人工合成氨 :化学固氨法。其条件要求高、成本高、转化率低、效率低。
(2)根瘤菌,生物固氨。常温常压下进行。成本低、转化率高、效率高。
3.工业应用:模拟生物的功能,把生物的功能原理用于化学工业生产,借以改善现有的并创造崭新的化学工艺过程。 二、合成氨的反应原理
1.加热试管中的铁丝绒至红热后注入氢气和氨气的混合气体,可以看到湿润的PH试纸变蓝色
2.用氢 气和氨气合成氨的反应式是
N2+3H2
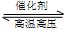 2NH3,属放热反应。
2NH3,属放热反应。 3.工业上,采用以铁为主的催化剂,在400~500℃和10Mpa~30 Mpa的条件下合成氨。
(1)催化剂的主要作用:成千上万倍地加快化学反应速率,缩短达平衡的时间,提高日产量。
(2)合成氨的适宜条件:以铁为主的催化剂,在400~500℃和10Mpa~30 Mpa的条件
(3)选择适宜生产条件的原则:有较高的反应速率和平衡转化率,能最大限度地提高利润。
(4)合成氨生产时,不采用尽可能高的压强,通常采用10MPa~30MPa 的压强,否则会增大设备的动力要求,增大成本。
(5)合成氨的反应为放热反应,降低温度促使平衡向有移动,有利于N2、H2转化为NH3;但降温必然减缓了反应速率,影响单位时间产率。生产中将二者综合考虑,既要保证N2、H2的转化率,又要保证较快的反应速率,只能选择适中的温度400~500℃左右。应注意该温度为催化剂活化温度,低于此温度,催化剂不起作用。
(6)催化剂是影响反应速率的几个因素中,对反应速率影响程度最大的。
催化剂的特点:
①选择性:不 同的反应选择不同的催化剂,如合成氨选择了铁触媒。每种催化剂都是对特定的反应有催化作用,并非能改变任何化学反应的速率。
②灵敏性:催化剂中混入杂质,常常会失去催化作 用,称催化剂“中毒”,因此 反应气体进入反应器前必须净化。 ③催化剂只有在活化温度以上才能起催化作用,如铁触媒活化温度为400~500℃,因此该温度为合成氨的适宜温度。
人工固氮技术——合成氨:
1.生产原理
2.合成氨的基本生产过程
(1)原料气的制备要实现合成氨的工业化生产,首先要解决氢气和氮气的来源问题。
①氮气的制备合成氨所需要的氮气都取自空气。从空气中制取氮气通常有两种方法:一是将空气液化后蒸发分离出氧气而获得氮气;二是将空气中的氧气与碳作用生成二氧化碳,再除去二氧化碳得到氮气。
②氢气的制备氢气主要来源于水和碳氢化合物。氢气的制取有下表中的几条途径。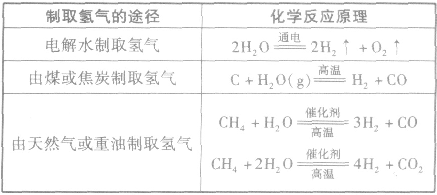
(2)原料气的净化
原料气的净化就是除去原料气中的杂质。在制取原料气的过程中,常混有一些杂质,其中的某些杂质会使合成氨所用的催化剂“中毒”(所谓“中毒”即是催化剂失去催化活性),所以必须除去。原料气净化的主要目的是防止催化剂“中毒”。
(3)氨的合成与分离
①氨的合成工业合成氨的主要设备是合成塔。将净化后的原料气经过压缩机压缩后输人合成塔,经过下列化学反应合成氨: 
②氨的分离从合成塔出来的混合气体,通常约含15%(体积分数)的氨。为了使氨从未反应的氮气和氢气里分离出来,要把混合气体通过冷凝器使氨液化,然后在气体分离器里把液态氨分离出来导入液氨贮罐。南气体分离器出来的气体,经过循环压缩机,再送到合成塔中进行反应。
3.合成氨适宜条件的选择
外加条件要尽可能加快反应速率,提高反应物的转化率.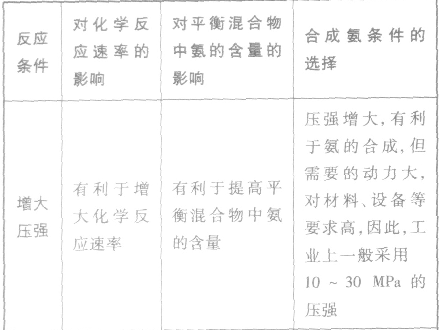
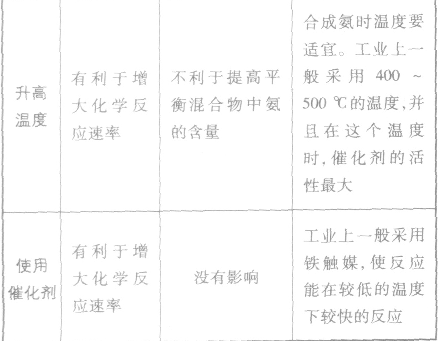
4.合成氨的环境保护
随着环境保护意识的增强,以及相关的法律、法规的严格实施,合成氨生产中可能产生的“三废”的处理越来越成为技术改造的重要问题。
(1)废渣
主要来自造气阶段,特别是以煤为原料而产生的煤渣,用重油为原料产生的炭黑等,现在大都将它们用作建材和肥料的原料。
(2)废气
主要是H2S和CO2等气体。对H2S气体的处理,先后采用了直接氧化法(选择性催化氧化)、循环法(使用溶剂将其吸收浓缩)等回收技术。对CO2 的处理,正在不断研究和改进将其作为尿素和碳铵生产原料的途径。
(3)废液
主要是含氰化物和含氨的污水。目前,处理含氰化物污水主要有生化、加压水解、氧化分解、化学沉淀、反吹回炉等方法;处理含氨废水多以蒸馏的方法回收氨达到综合利用的目的,对浓度过低的含氨废水,可用离子交换法治理。
陶器的烧制:
(1)陶器通常是用普通黏土做原料制成的
(2)黏土主要由铝硅酸盐组成,可表示为:xAl2O3·ySiO2·zH2O,还包含有铁、钛、钙、镁、钾、钠等元素
(3)铝、硅的氧化物起骨架材料的作用钾、钠、钙、镁的氧化物起助熔的作用铁、钛的氧化物起呈色作用,含量越多颜色越深
(4)步骤:制泥,成型,干燥,烧成 
(5)陶器烧成中的主要工艺条件是温度和气氛
(6)需要控制的温度环节是烧成温度,升温温度,保温温度,降温温度。烧成的温度大约是950℃,一般在烧到温度高于原料熔点的三分之二时,胚体中的各种成分间开始发生各种复杂的化学反应,逐渐烧结。温度太低,原料中的各种成分间未发生化学反应而不能烧结;温度太高,超过熔点,固态物质便会融化,使陶器的形状发生改变。
(7)气氛指烧成时使用的火焰是氧化气氛还是还原气氛。
(8)红陶和灰陶中铁的存在形式: 在氧化气氛中(氧气过量)烧成得到红陶,其中铁的氧化物以Fe2O3的形态存在;在还原气氛中(CO或H2)烧成得到灰陶,铁的氧化物以FeO的形态存在。
瓷器的烧制:
(1)原料:纯净的高岭土。主要成分表示为:Al2O3·2SiO2·2H2O
(2)瓷器的烧成温度:1200℃以上(陶器的烧成温度:大约950℃)
(3)瓷器胚体组织细腻,结构致密,强度较高,吸水率较低,瓷器的表面素色洁净,成半透明状。
与“氨广泛应用于工农业生产。(1)工业合成氨的反应:N2(g)+3H2(g)...”考查相似的试题有:
- 有关氨的性质的叙述正确的是[ ]A.氨能在氧气中燃烧B.氨水呈碱性C.氨水和酸相遇都能产生白烟D.在反应NH3+H+=NH4+中,氨失...
- 如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是[ ]A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色B.若A为醋...
- 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间...
- 已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的...
- 下列叙述不正确的是[ ]A.用酒精清洗沾到皮肤上的苯酚B.用氨水清洗度管壁附着的银镜C.用盐析的方法分离没脂皂化反应的产物D...
- 下列有关氨的叙述中,正确的是[ ]A.氨气是无色无味的气体B.氨水的浓度越大,其密度越大C.在化学反应中,氨既能与酸反应,...
- 下列关于工业生产的说法中,正确的是( )A.工业上用氧气在接触室中氧化黄铁矿得到二氧化硫B.工业上通过电解饱和氯化钠溶液...
- 某研究性学习小组为了探究合成氨的原理,设计了下列实验装置。下图中A是简易的氢气发生器,B是圆底烧瓶,C是装有干燥剂的U形...
- 下列有关合成氨工业的说法中,正确的是[ ]A.从合成塔出来的混合气体中,氨气占15%,所以生产氨的工厂的效率都很低B.由于氨...
- [选修一化学与技术]联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:(1)沉淀池中发生反应的化学方程式为______;(...