本试题 “关于甲醛(CH2O)分子,下列说法正确的是[ ]①分子中碳原子采用sp2杂化;②分子中所有原子处于同一平面上;③分子中每个原子都达到8电子稳定结构;④分子的立体构...” 主要考查您对杂化轨道理论(中心原子杂化方式)
有机物分子的空间构型
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 杂化轨道理论(中心原子杂化方式)
- 有机物分子的空间构型
杂化轨道理论:
是鲍林为了解释分子的立体结构提出的。中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见杂化方式:
(1)sp杂化:直线型 如:CO2、CS2
(2)sp2杂化:平面三角形(等性杂化为平面正三角形) 如:BCl3 C2H4
不等性杂化为V字型 如:H2O H2S OF2
(3)sp3杂化:空间四面体(等性杂化为正四面体) 如:CH4、CCl4
不等性杂化为三角锥 如:NH3 PCl3 H3O+
sp3d杂化:三角双锥
sp3d2杂化:八面体(等性杂化为正八面体)
是鲍林为了解释分子的立体结构提出的。中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见杂化方式:
(1)sp杂化:直线型 如:CO2、CS2
(2)sp2杂化:平面三角形(等性杂化为平面正三角形) 如:BCl3 C2H4
不等性杂化为V字型 如:H2O H2S OF2
(3)sp3杂化:空间四面体(等性杂化为正四面体) 如:CH4、CCl4
不等性杂化为三角锥 如:NH3 PCl3 H3O+
sp3d杂化:三角双锥
sp3d2杂化:八面体(等性杂化为正八面体)
分子的构型与杂化类型的关系:
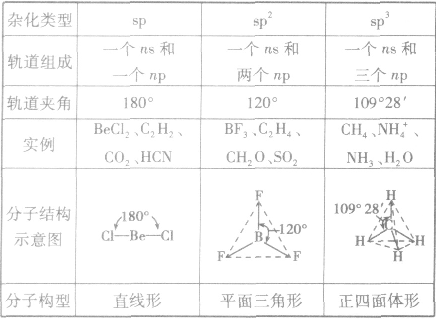
有机物分子的空间构型:
(1)烷、烷基:
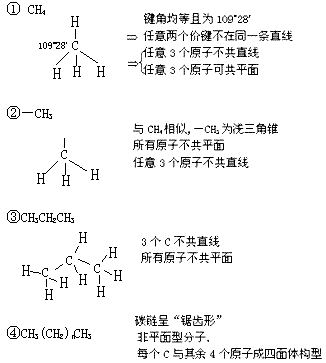
(2)烯:
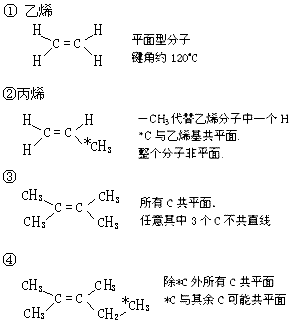
(3)醛、酮、羧酸
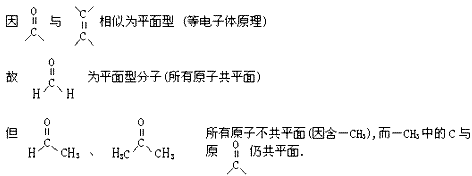
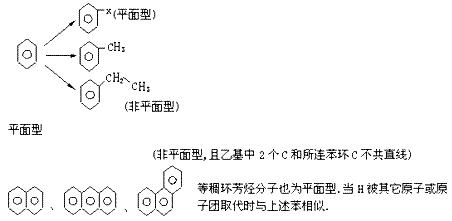
(4)苯、苯的同系物,稠环芳烃
苯是一种平面型分子,当苯环上的H被其它某个原子取代后仍为平面型。当取代基为非平面型,整个分子也就变为非平面型。
(5)炔:因为C2H2为一种直线型分子:H-C≡C-H。所以它的卤代物C2HX、C2X2均为直线型分子:H-C≡C-X、
X-C≡C-X,丙炔CH3-C≡C-H分子中3个C和乙炔基中H共直线整个分子非直线也非平面型(含-CH3)
(1)烷、烷基:

(2)烯:

(3)醛、酮、羧酸

(4)苯、苯的同系物,稠环芳烃
苯是一种平面型分子,当苯环上的H被其它某个原子取代后仍为平面型。当取代基为非平面型,整个分子也就变为非平面型。

(5)炔:因为C2H2为一种直线型分子:H-C≡C-H。所以它的卤代物C2HX、C2X2均为直线型分子:H-C≡C-X、
X-C≡C-X,丙炔CH3-C≡C-H分子中3个C和乙炔基中H共直线整个分子非直线也非平面型(含-CH3)
发现相似题
与“关于甲醛(CH2O)分子,下列说法正确的是[ ]①分子中碳原子采...”考查相似的试题有:
- 铜(Cu)是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答下列问题:(1...
- 已知C-C键可以绕键轴自由旋转,结构简式为的烃,下列说法正确的是( )A.分子中至少有8个碳原子处于同一平面上B.分子中至少...
- 阿司匹林的结构如图所示.有如下各类反应:①银镜反应 ②中和反应 ③酯化反应 ④水解反应 ⑤加成反应,则阿司匹林在一定条件下...
- 芬必得是一种性能优良,使用广泛得解热、镇痛、抗炎症得长效缓释药物,其主要成分的结构简式如图对芬必得的叙述不正确的是( ...
- 癌症(恶性肿瘤)严重威胁着人类的生命。据报道,每年因癌症而死亡的人数呈递增趋势。为了战胜癌症,科学家正致力于研究癌症...
- 下列说法正确的是( )①油脂是一类天然高分子化合物,是高级脂肪酸的甘油酯②蛋白质降解生成氨基酸属于分解反应③硝化甘油、火...
- 某有机物的结构简式为,其不可能发生的反应有( )①加成反应 ②取代反应 ③消去反应 ④氧化反应 ⑤水解反应⑥与氢氧化钠反应 ⑦与稀...
- 关于胡椒粉,植物挥发油中成分)说法正确的是( )A.该化合物属于芳香烃B.分子中9个碳原子一定处于同一平面C.该有机物能和...
- 写出下列反应方程式:(1)苯和浓硝酸、浓硫酸混合60℃水浴______;(2)红热的铜丝插入乙醇中______;(3)苯酚钠溶液中通入C...
- 有机物A在一定条件下能发生水解反应生成两种有机物,B中①~⑥是标出该有机物分子中不同的化学键,在水解时,断裂的键是( )A...