本试题 “I、实验室中常以BaSO4重量法测定BaCl2•nH2O中的Ba的含量.主要步骤如下:①灼烧瓷坩埚至恒重,称得坩埚的质量②称取BaCl2•nH2O并在烧杯中溶解,加盐酸处理③将一...” 主要考查您对测定物质组成、成分含量
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 测定物质组成、成分含量
定量实验介绍:

燃烧法测定氨基酸的组成:
实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现按下图所示装置进行实验。

①实验开始时,首先要通入一段时间的氧气,目的是排除体系中的N2。
②D装置的作用是吸收未反应的O2,保证最终收集的气体是N2。
③读取N2体积时,应注意:量筒内液面与广口瓶中的液面相持平视线与凹液面最低处相切。
④实验中测得N2的体积为VmL(已折算为标准状况)。为确定此氨基酸的分子式,还需要的有关数据为生成二氧化碳气体的质量、生成水的质量、氨基酸的相对分子质量
用氨气还原氧化铜的方法测定铜的近似相对原子质量:
实验室用氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为:2NH3+3CuO
 N2+3Cu+3H2O
N2+3Cu+3H2O(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。
装置图:
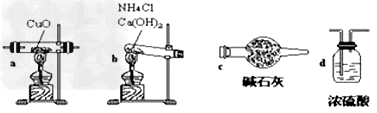
①连接顺序为:bcacd
②d中浓硫酸的作用是吸收未反应的氨、防止空气中水分进入;实验完毕时观察到a中的现象是固体由黑色转变为红色;
③Cu的相对原子质量的表达式
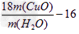
发现相似题
与“I、实验室中常以BaSO4重量法测定BaCl2•nH2O中的Ba的含量.主...”考查相似的试题有:
- 新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化.某课外小组利用碘滴定法测某橙汁中维生素C的...
- 下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数[ ]A.取a克混合物充分加热,减重b克B.取a克混合物与足量稀盐...
- 工业生产的纯碱常含有少量的NaCl等杂质.右图是测定产品中Na2CO3质量分数的实验装置.操作步骤有:A.在干燥管内填满碱石灰,...
- 研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式.有机物A可由葡萄糖发酵得到,也可从酸...
- 某同学进行试验探究时,欲配制1.0mol/LBa(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(化学式量:315)。在室温...
- 人体呼出气体中含有N2、O2、CO2、水蒸气等多种成分。某课外学习小组利用下图装置测定N2、O2、CO2的百分含量(忽略水蒸气等微...
- 下列说法或表示方法正确的是( ) A.电解稀硫酸不可能发生的反应是Cu+H2SO4CuSO4+H2↑ B.李比希燃烧法、钠熔法、铜丝燃烧法...
- (I)小明在做“研究温度对反应速率的影响”实验时,他取了两只试管,均加入4mL 0.01mol/L的KMnO4酸性溶液和2mL 0.1mol/L H2C2O...
- 北京市场销售的某种食用精制盐包装袋上有如下说明(1)碘酸钾与碘化钾在酸性条件下发生反应生成I2,I2可用四氯化碳检验。向碘的...
- 取式量为46的某有机物4.6克,在足量的氧气中充分燃烧,生成8.8克二氧化碳和5.4克水,据此判断该有机物( )A.只由碳、氢两种...