本试题 “W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数一次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成...” 主要考查您对电子排布式
元素周期表
电离能
元素的推断
热化学方程式
盖斯定律
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电子排布式
- 元素周期表
- 电离能
- 元素的推断
- 热化学方程式
- 盖斯定律
电子排布式:
①简化电子排布式
为了避免电子排布式书写过于繁琐,把内层电子达到稀有气体元素原子结构的部分以相应稀有气体的冗素符号外加方括号表示,即为简化电子排布式,如K 的简化电子排布式为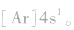
②特殊电子排布式
有个别元素的基态原子的电子排布对于构造原理有1个电子的反常。因为能量相同的原子轨道在全充满( )、半充满(
)、半充满(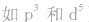 )和全空(
)和全空(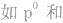
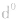 )状态时,体系的能量较低,原子较稳定。
)状态时,体系的能量较低,原子较稳定。 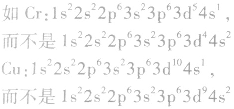
(2)电子排布图:用方框表示一个原子轨道,用箭头“↑”或“↓”来区别自旋状态不同的电子。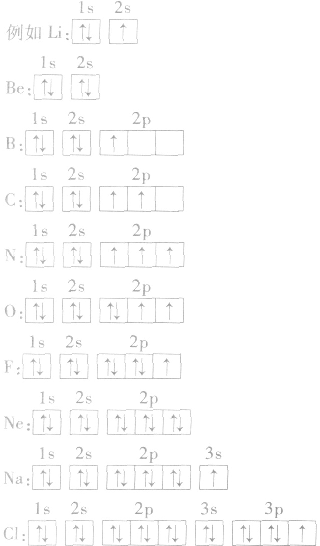
构造原理:
多电子原子的核外电子排布总是按照能量最低原理,由低能级逐步填充到高能级。绝大多数元素的原子核外电子的排布遵循下图所示的排布顺序,这种排布顺序被称为构造原理。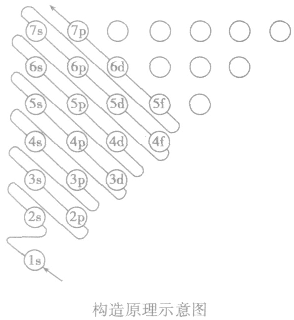
点拨:构造原理中的排布顺序,其实质是各能级的能量高低顺序,可由下列公式得出ns<(n一2)f< (n一1)d<np(n表示能层序数)。常用的重要的能级交错顺序有: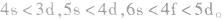
核外电子排布式一构造原理的应用:
根据构造原理,按照能级顺序,用能级符号右上角的数字表示该能级上电子数的式子,叫做电子排布式。例如,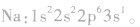
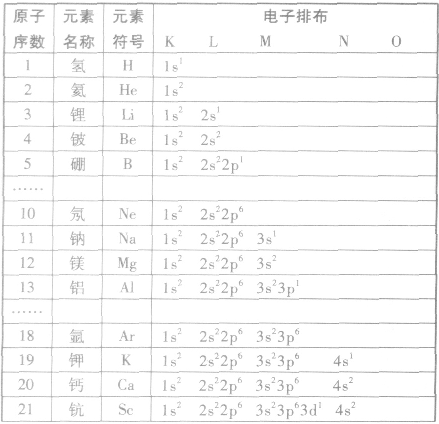
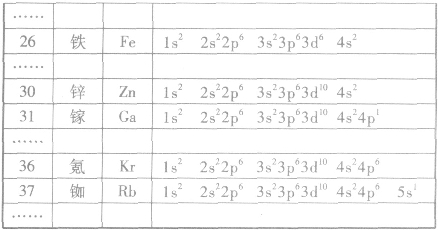
元素周期表编排原则:
(1)把电子层数相同的各种元素按原子序数递增的顺序从左至右排成横行。
(2)把最外层电子数相同的元素按电子层数递增的顺序由上到下排列成纵行。
注意:①元素周期表是元素周期律的具体表现形式,它反映了元素之间相互联系的规律。
②历史上第一个元素周期表是1869年俄国化学家门捷列夫在前人探索的基础上排成的,他将元素按相对原子质量由小到大依次排列,并将化学性质相似的元素放在一个纵行。
元素周期表的结构:
(1)周期
①周期的含义在元素周期表中,把电子层数相同的元素,按原子序数递增的顺序从左到右排成横行,这样每个横行为一个周期。现在使用的元素周期表有7个横行,即7 个周期。
②周期的划分
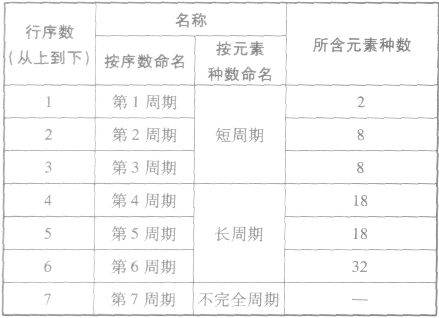
(2)族
①族的含义在周期表中,把不同横行(即周期)中最外层电子数相同的元素,按电子层数递增的顺序由上到下排成纵行,除第8、9、10三个纵行叫做第Ⅷ族外,其余15个纵行,每个纵行为一族。现在使用的元素周期表有18 个纵行,它们被划分为16个族。
②族的划分
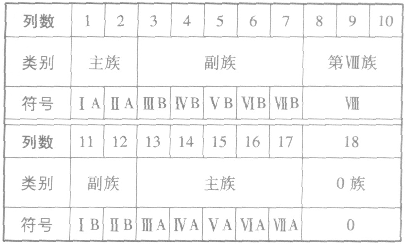
(3)元素周期表中主族元素金属性和非金属性的递变
电离能:
(1)概念
气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量叫做第一电离能。
(2)元素第一电离能的意义:可以衡量元素的原子在气态时失去一个电子的难易程度。第一电离能数值越小,在气态时原子越容易失去一个电子;第一电离能数值越大,在气态时原子越难失去一个电子。
(3)电离能的变化规律
①随核电荷数递增,元素的第一电离能呈周期性变化。
②同一周期内,随着原子序数的增加,原子半径逐渐变小(稀有气体除外),原子核对外层电子的吸引越来越强,元素的原子越来越难失电子,因此元素的第一电离能呈增大的趋势。同一周期内,碱金属元素的第一电离能最小,稀有气体元素的第一电离能最大。
③同一主族,从上到下,随着原子序数的增加,电子层数逐渐增多,原子半径逐渐增大,原子核对外层电子的吸引越来越弱,元素的原子越来越易失电子,故同一主族,随着电子层数的增加,元素的第一电离能逐渐减小。注意通常ⅡA族元素的第一电离能大于ⅢA 族元素、VA族元素的第一电离能大于ⅥA族元素。这是由于ⅡA、VA族元素原子的价电子排布分别为 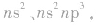 是较稳定的全充满或半充满状态,因而失去电子所需的能量较高。
是较稳定的全充满或半充满状态,因而失去电子所需的能量较高。
元素性质推断知识点归纳:
(1)质量最轻的元素是氢(H),其单质可以填充气球;质量最轻的金属是锂(Li);熔点最高的非金属单质是石墨;熔点最高的金属单质是钨(W);熔点最低的金属单质是汞(Hg)。
(2)地壳中含量最多是氧(O),其次是Si、Al、Fe、Ca、Na、K、Mg、H、Ti。
(3)既难得电子,又难失电子且为单原子分子的气体是稀有气体。
(4)最高正价与最低负价绝对值之差为4的是硫(S);最高正价与最低负价绝对值之差为零的是碳(C)和硅(Si)。
(5)碳(C)是形成化合物最多的元素,是构成有机物的骨架元素,可形成多种同素异形体,其中硬度最大的是金刚石,而C60是分子晶体,熔点较低。
(6)常温下能与水反应放出氧气,单质是氟(F2),化合物是过氧化钠(Na2O2)。
(7)硅(Si)是构成地壳岩石骨架的主要元素,单质硅可被强碱溶液腐蚀且能放出氢气,还能被弱酸氢氟酸所溶解。
(8)能在空气中自然的非金属单质是白磷(P4),白磷有毒,能溶于CS2,和红磷互为同素异形体,红磷不能自然,不溶于CS2,白磷与红磷在一定的条件下可以相互转化。
(9)既能在二氧化碳中燃烧,又能在氮气中燃烧的金属是Mg,既能与酸溶液又能与碱溶液作用且均放出氢气的金属是铝(Al)。
(10)同一元素的气态氢化物和最高价氧化物的水化物化合生成盐的元素一定是氮(N)。
(11)同一元素的气态氢化物和气态氧化物反应生成该元素得单质和水,该元素可能是氮(N)或硫(S)。
(12)光照时可以释放电子的是铷(Rb)和铯(Cs);常温下呈液态的金属是汞(Hg),非金属单质是溴(Br2)。
解元素推断题必备知识归纳
(1)与元素的原子结构相关知识归纳
①最外层电子数等于次外层电子数的元素是Be、Ar;最外层电子数是次外层电子数2倍的元素有C;最外层电子数是次外层电子数3倍的元素有O;最外层电子数是次外层电子数4倍的元素有Ne。
②次外层电子数是最外层电子数2倍的元素有Li、Si;次外层电子数是最外层电子数4倍的元素有Mg。
③内层电子数是最外层电子数2倍的元素有Li、P;电子总数是最外层电子数2倍的元素有Be。原子核内无中子的元素是11H。
④常见等电子微粒:
|
电子数 |
分子 |
阳离子 |
阴离子 |
|
2 |
H2、He |
Li+、Be2+ |
H- |
|
10 |
Ne、HF、H2O、NH3、CH4 |
Na+、Mg2+、Al3+、H3O+、NH4+ | O2-、F-、OH-、NH2- |
|
18 |
Ar、HCl、H2S、PH3、SiH4、F2、H2O2、N2H4、C2H6、CH3OH |
K+、Ca2+ |
S2-、HS-、Cl- |
①主族序数与周期序数相同的元素有H、Be、Al;主族序数是周期序数2倍的元素有C、S;主族序数是周期序数3倍的元素有O。
②周期序数是主族序数2倍的元素有Li、Ca;周期序数是主族序数3倍的元素有Na。
③最高正价与最低负价的绝对值相等的元素有C、Si;最高正价是最低负价的绝对值3倍的元素有S。
④上一周期元素所形成的阴离子和下一周期元素最高价态阳离子的电子层结构与上一周期零族元素原子的电子层结构相同。
(3)与元素性质相关知识归纳
①元素所形成的单质及化合物的物理特性
A.颜色:常温下,单质为有色气体的元素是F、Cl;单质为淡黄色固体的元素是S;焰色反应火焰呈黄色的元素是Na,呈紫色的元素是K(通过兰色钴玻璃)。
B.状态:常温下,单质呈液态的非金属元素是Br;单质为白色蜡状固体的元素是P。
C.气味:有臭鸡蛋气味的非金属元素是S。
D.熔点:单质熔点最低的金属元素是Hg;熔点最高的金属元素是W。单质熔点最高的非金属元素是C。氢化物熔点最高的非金属元素是O。氧化物熔点最高的非金属元素是Si。
E.硬度:单质为天然物质中硬度最大的元素是C。
F.密度:单质最轻的金属元素是Li;单质最轻的非金属元素是H。
G.溶解性:气态氢化物最易溶于水的元素是N。
H.导电性:单质能导电的非金属元素是C;单质属于半导体材料的是Si。
②元素所形成的单质及化合物的化学特性
A.无正价、无含氧酸的元素是F;单质氧化性最强、其氢化物水溶液可雕刻玻璃的元素是F;气态氢化物稳定性最强的元素是F;最高价氧化物对应的水化物酸性最强的元素是Cl。
B.其两种同素异形体对人类生存都非常重要的元素是O(O3层被称为人类和生物的保护伞);气态氢化物与最低价氧化物能反应生成单质的是S。
C.气态氢化物与最高价氧化物对应水化物能起化合反应的元素是N;气态氢化物能使湿润的红色石蕊试纸变蓝的元素是N;其中一种同素异形体在空气中能自燃的元素是P。
③元素性质递变规律
A.元素金属性强弱比较规律
I.依据元素周期表,同一周期中,从左到右,金属性逐渐减弱;同一主族中,由上到下,金属性逐渐增强。
II.依据最高价氧化物的水化物碱性强弱,碱性越强,金属性越强。
III.依据金属活动性顺序(极少数例外)。
IV.依据金属单质与酸或水反应的剧烈程度,反应越剧烈,金属性越强。
V.依据金属单质与盐溶液之间的置换反应。
VI.依据原电池原理,原电池中作负极的金属比作正极的金属金属性强。
VII.依据电解原理,电解时,阴极上后析出的金属比先析出的金属金属性强。
B.元素非金属性强弱比较规律
I.依据元素周期表,同一周期中,从左到右,非金属性逐渐增强;同一主族中,由上到下,非金属性逐渐减弱。
II.依据最高价氧化物的水化物的酸性强弱,酸性越强,非金属性越强。
III.依据与H2化合的难易,越容易化合,非金属性越强。
IV.依据其气态氢化物的稳定性,稳定性越强,非金属性越强。
V.依据非金属单质与盐溶液之间的置换反应。
C.微粒半径大小比较规律
I.同周期阳离子半径随原子序数递增逐渐减小,如第3周期中:Na+>Mg2+>Al3+;同周期阴离子半径随原子序数递增逐渐减小,如第3周期中:P3->S2->Cl-。
II.同主族阳离子半径随原子序数递增逐渐增大,如第IA族中:Li<Na+<K+,同主族阴离子半径随原子序数递增逐渐增大,如第VIIA族中:F-<Cl-<Br-。
III.阳离子半径总比相应原子半径小,如Na+<Na,阴离子半径总比相应原子半径大,如S2->S。
IV.电子层结构相同的离子半径随原子序数的增大而减小,如S2->Cl->K+>Ca2+,O2->F->Na+>Mg2+>Al3+。
④元素的含量地壳中质量分数最大的元素是O,其次是Si;地壳中质量分数最大的金属元素是Al,其次是Fe;氢化物中氢元素质量分数最大的是C;所形成的有机化合物中种类最多的是C。
(3)解元素推断题的方法解答元素推断题,必须抓住原子结构和元素的有关性质,掌握元素周期表中主要规律,熟悉某些元素(短周期或前20号元素)的性质、存在和用途的特殊性,用分析推理法确定未知元素在周期表中的位置。对于有突破口的元素推断题,可利用题目暗示的突破口,联系其它条件,顺藤摸瓜,各个击破,推出结论。对无明显突破口的元素推断题,可利用题示条件的限定,逐渐缩小推求范围,并充分考虑各元素的相互关系予以推断。有时限制条件不足,则可进行讨论,得出合理结论,有时答案不止一组,只要能解释通都可以,若题目只要求一组,则选择自己最熟悉、最有把握的。有时需要运用直觉,大胆尝试、假设,再根据题给条件进行验证,也可推出。
1.定义表示反应所放出或吸收热量的化学方程式,叫做热化学方程式。
2.表示意义不仅表明了化学反应中的物质变化,也表明厂化学反应中的能量变化。例如:
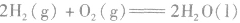 :
: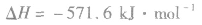 ,表示在25℃、101kPa下,2molH2(g)和1mol O2(g)完全反应生成2molH2O(l)时要释放571.6kJ 的能量。
,表示在25℃、101kPa下,2molH2(g)和1mol O2(g)完全反应生成2molH2O(l)时要释放571.6kJ 的能量。热化学反应方程式的书写:
热化学方程式与普通化学方程式相比,在书写时除厂要遵守书写化学方程式的要求外还应注意以下问题:
1.注意△H的符号和单位 △H只能写在标有反应物和生成物状态的化学方程式的右边。若为放热反应,△H为“-”;若为吸热反应,△H为“+”。△H的单位一般为kJ/moJ。
2.注意反应条件反衄热△H与测定条件(温度、压强等)有关。因此书写热化学方程式时应注明△H的测定条件。绝大多数△H是是25℃、101kPa下测定的,此条件下进行的反应可不注明温度和压强。
3.注意物质的聚集状态反应物和生成物的聚集状态不同,反应热△H不同。因此,必须注明物质的聚集状态才能完整地体现出热化学方程式的意义。气体用“g”,液体用:l“,固体用“s”,溶液用“aq”。
4.注意热化学方程式的化学计量数
(1)热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物质的量,并不表示物质的分子数或原子数,因此化学计量数可以是整数,也可以是分数。
(2)热化学方程式中的反应热表示反应已完成时的热量变化,由于△H与反应完成的量有关,所以方程式中化学式前面的化学计量数必须与△H相对应,如果化学计量数加倍,则△H也要加倍。当反应逆向进行时,其反应热与正反应的反应热数值相等,符号相反。
不管化学反应是一步完成还是分几步完成,其反应热是相同的。换句话说,化学反应的反应热只与反应的始态和终态有关,而与反应进行的途径无关。如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一一步完成时的反应热是相同的,这就是盖斯定律。
盖斯定律的意义:
利用盖斯定律可以间接计算某些不能直接测得的反应的反应热。例如:
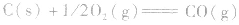 的△H无法直接测得,可以结合下面两个反应的△H,利用盖斯定律进行计算。
的△H无法直接测得,可以结合下面两个反应的△H,利用盖斯定律进行计算。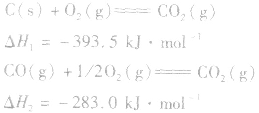
根据盖斯定律,就可以计算出所给反应的△H。分析上述两个反应的关系,即知
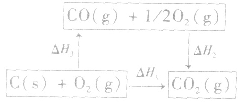
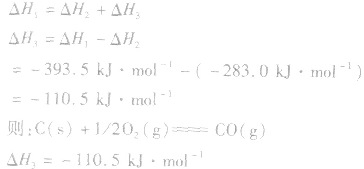
盖斯定律在反应热大小比较中的应用:
1.同一反应生成物状态不同时
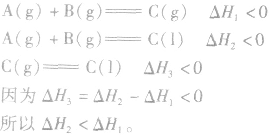
若按以下思路分析:
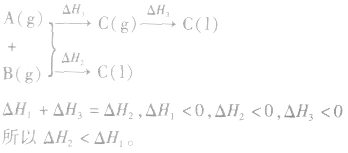
2.同一反应物状态不同时
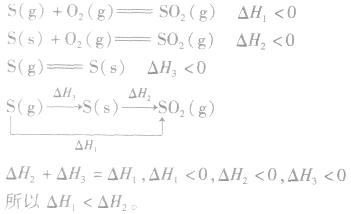
3.两个有联系的不同反应相比
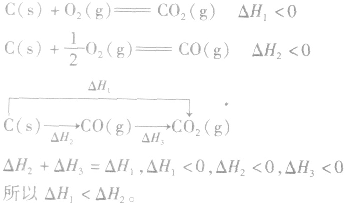
并且据此可写出下面的热化学方程式:

与“W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数...”考查相似的试题有:
- (1)在上面元素周期表中全部是金属元素的区域为__________。(a) A (b) B (c) C (d) D(2)有人认为形成化合物最多的元素不是...
- 下列叙述中,甲金属一定比乙金属活泼性强的是( )A.甲原子电子层数比乙原子的电子层数多B.在甲乙两种金属和盐酸构成的原电...
- 某周期ⅡA族元素的原子序数为x,则同周期的Ⅲ族元素的原子序数是[ ]A.只有x+1B.可能是x+8或x+18C.可能是x+2D.可能是x+1或x+...
- 根据元素周期表,判断下列元素中不属于主族元素的是[ ]A.钙B.铁C.磷D.碘
- 短周期元素X、Y的原子序数相差2。下列有关叙述正确的是[ ]A.X与Y不可能位于同一主族B.X与Y一定位于同一周期C.X与Y可能形成...
- W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne...
- 下表是元素周期表的一部分,回答下列问题:(1)写出①---⑿号元素的元素符号①___ ②___ ③____ ④____ ⑤____ ⑥____ ⑦___ ⑧____ ⑨_...
- 煤燃烧的反应热可通过以下两个途径来利用:Ⅰ.利用煤在充足的空气中直接燃烧产生的反应热;Ⅱ.先使煤与水蒸气反应得到氢气和...
- 已知一些共价键的键能如下(单位:kJ/mol) H-H:436.4 Cl-Cl:242.7 H-C1:431.8(1)写出氢气在氯气中燃烧生成氯化氢气体的热化学...
- 已知2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol,则关于方程式2H2O(l)===2H2(g)+O2(g)的ΔH的说法中正确的是[ ]A.方程式...