本试题 “物质的性质与物质的组成、结构、用途密切相关.请回答:(1)金刚石和石墨都是碳的单质,但由于______不同,两者物理性质有很大差异.(2)浓硫酸由于具有___...” 主要考查您对浓硫酸的稀释
单质和化合物
二氧化碳的用途
碱的性质
碱的用途
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 浓硫酸的稀释
- 单质和化合物
- 二氧化碳的用途
- 碱的性质
- 碱的用途
浓硫酸:
俗称坏水。坏水指浓度大于或等于70%的硫酸溶液。浓硫酸在浓度高时具有强氧化性,这是它与普通硫酸或普通浓硫酸最大的区别之一。同时它还具有脱水性,强氧化性,难挥发性,酸性,稳定性,吸水性等。
浓硫酸的稀释:
稀释浓硫酸时,一定要将浓硫酸沿着器壁慢慢地注入水里,并不断搅拌,使产生的热量迅速地扩散,切不可把水倒入浓硫酸中,因为水的密度较小,浮在浓硫酸上面,溶解时放出的热会使水立刻沸腾。使硫酸液滴向四周飞溅,这是非常危险的(如下图)。若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%一5%的 NaHCO3溶液。
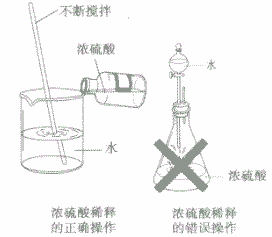
切记“酸入水,沿器壁,慢慢倒,不断搅”。注酸入水不断搅拌
俗称坏水。坏水指浓度大于或等于70%的硫酸溶液。浓硫酸在浓度高时具有强氧化性,这是它与普通硫酸或普通浓硫酸最大的区别之一。同时它还具有脱水性,强氧化性,难挥发性,酸性,稳定性,吸水性等。
浓硫酸的稀释:
稀释浓硫酸时,一定要将浓硫酸沿着器壁慢慢地注入水里,并不断搅拌,使产生的热量迅速地扩散,切不可把水倒入浓硫酸中,因为水的密度较小,浮在浓硫酸上面,溶解时放出的热会使水立刻沸腾。使硫酸液滴向四周飞溅,这是非常危险的(如下图)。若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%一5%的 NaHCO3溶液。

切记“酸入水,沿器壁,慢慢倒,不断搅”。注酸入水不断搅拌
单质:
(1)概念:由同种元素组成的纯净物。
(2)单质的分类:依据组成单质元素的性质把一单质分为三类。
金属单质:由金属元素组成的单质,如铁、铜、银等
非金属单质:由非金属元素组成的单质,如碳、磷、氧气等
稀有气体单质:由稀有气体元素组成的单质,如氦、氖、氛等单质
化合物:
(1)概念:由不同种元素组成的纯净物。
(2)化合物的分类:化合物分为有机化合物和无机化合物。
单质和化合物的区别和联系:
化合物与氧化物的区别和联系:
同种元素组成的物质一定是单质吗?
由同种元素组成的纯净物叫做单质。理解单质的概念必须抓住两点:①由同种元素组成;②必须是纯净物,如氧气是一单质。由同种元素组成的物质不一定是单质,也可能是混合物,但绝不可能是化合物,如氧气 (O2)、臭氧(O3)两种物质混在一起是一种混合物,但是只有一种氧元素;同样的例子还有红磷和白磷,金刚石和石墨等。
对单质和化合物概念的理解:
(1)单质的概念:
①理解一单质的概念不仅要关注它是由一种元素组成,还应注意它首先是一种纯净物。如:氧气、氮气、碳、硫、铁、铜、各种稀有气体等都属于单质。
②由同种元素组成的物质不一定是单质,还可能是混合物:如:氧气与臭氧的混合物、白磷与红磷的混合物、金刚石与石墨的混合物等都只含一种元素,但都属于混合物。
(2)化合物的概念:理解化合物的概念同样不仅要关注它是由两种或两种以上的元素组成,还应注意它首先是一种纯净物。如二氧化碳,氯化钠、高锰酸钾等都属于化合物。
(1)概念:由同种元素组成的纯净物。
(2)单质的分类:依据组成单质元素的性质把一单质分为三类。
金属单质:由金属元素组成的单质,如铁、铜、银等
非金属单质:由非金属元素组成的单质,如碳、磷、氧气等
稀有气体单质:由稀有气体元素组成的单质,如氦、氖、氛等单质
化合物:
(1)概念:由不同种元素组成的纯净物。
(2)化合物的分类:化合物分为有机化合物和无机化合物。
单质和化合物的区别和联系:
| 单质 | 化合物 | ||
| 区别 | 宏观组成 | 同种元素 | 不同种元素 |
| 微观构成 | 有同种原子构成 | 由不同种原子构成 | |
| 化学性质 | 不能发生分解反应 | 一定条件下发生分解反应 | |
| 联系 | 相互转变 | 它们均属于纯净物。单质发生化合反应可以生成化合物,化合物发生分解反应可以生成单质 | |
| 质子数 | 同一种元素的原子,不论在一单质里还是在化合物里,原子核内质子数保持不变 | ||
化合物与氧化物的区别和联系:
| 化合物 | 氧化物 | |
| 区别 | ①由不同种元素组成的纯净物叫化合物 ②由两种或两种以上元素组成 ③不一定含有氧元素 ④属于纯净物中的一类 |
①由两种元素组成的化合物中,如果有一种元素是氧元素,这种化合物叫氧化物 ②一定由两种元素组成 ③一定含有氧元素 ④属于化合物中的一类 |
| 联系 | 氧化物和化合物是个体与总体的关系,氧化物属于化合物中的一类 | |
同种元素组成的物质一定是单质吗?
由同种元素组成的纯净物叫做单质。理解单质的概念必须抓住两点:①由同种元素组成;②必须是纯净物,如氧气是一单质。由同种元素组成的物质不一定是单质,也可能是混合物,但绝不可能是化合物,如氧气 (O2)、臭氧(O3)两种物质混在一起是一种混合物,但是只有一种氧元素;同样的例子还有红磷和白磷,金刚石和石墨等。
对单质和化合物概念的理解:
(1)单质的概念:
①理解一单质的概念不仅要关注它是由一种元素组成,还应注意它首先是一种纯净物。如:氧气、氮气、碳、硫、铁、铜、各种稀有气体等都属于单质。
②由同种元素组成的物质不一定是单质,还可能是混合物:如:氧气与臭氧的混合物、白磷与红磷的混合物、金刚石与石墨的混合物等都只含一种元素,但都属于混合物。
(2)化合物的概念:理解化合物的概念同样不仅要关注它是由两种或两种以上的元素组成,还应注意它首先是一种纯净物。如二氧化碳,氯化钠、高锰酸钾等都属于化合物。
共价化合物与离子化合物的区别:
1. 共价化合物
(1)概念:像HCl、CO2这样以共用电子对结合在一起的化合物为共价化合物。
(2)共价化合物的类型:
①两种非金属原子结合成的化合物,如HCl、CO2等。
②非金属与酸根构成的化合物,如H2SO4、HNO3等。
2. 离子化合物与共价化合物的区别:
离子化合物是由阴、阳离子相互作用形成的化合物;共价化合物是原子间全部以共用电子对结合形成的化合物。离子化合物由离子构成,共价化合物大多数由分子构成。
二氧化碳用途:
1.二氧化碳不支持燃烧,不能燃烧,比空气重,可用于灭火
2.干冰升华时吸收大量的热,可用它做制冷剂或人工降雨
3.工业制纯碱和尿素,是一种重要的化工原料
4.植物光合作用,绿色植物吸收太阳能,利用二氧化碳和水,合成有机物放出氧气
二氧化碳中毒:
二氧化碳中毒是人吸入高浓度的二氧化碳所出现的昏迷及脑缺氧情况,一般大气中二氧化碳含量超过1%时,人即有轻度中毒反应;当超过3%时,开始出现呼吸困难;超过6%时,就会重度中毒甚至死亡。
(1)征状
中毒主要征状有:头痛、头愫晕、耳鸣、气急、胸闷、乏力、心跳加快,面颊发绀、烦躁、谵妄、呼吸困难,如情况持续,就会出现嗜睡、淡漠、昏迷、反射消失、瞳孔散大、大小便失禁、血压下降甚至死亡。
(2)补救
打开门窗、通风孔,抢救者才可进入。将病人救出后,在空气新鲜处进行人工呼吸,心脏按摩,吸氧(避免高压、高流量、高浓度给氧,以免呼吸中枢更为抑制),开始1~2L/分,随病人呼吸好转逐渐增大给氧量(4--5L/分),以至采用高压氧治疗。(最好是纯氧)
吸入兴奋剂:多种兴奋剂交替、联合使用,如洛贝林、山梗菜碱等。
防止脑和肺水肿:应用脱水剂、激素,限制液量和速度,吸入钠的份量亦应限制。
对症治疗:给予多种维生素、细胞色素C、能量合剂、高渗糖,以防感染。
抢救同时要留意有没有其他有毒气体存在,如一氧化碳等。
1.二氧化碳不支持燃烧,不能燃烧,比空气重,可用于灭火
2.干冰升华时吸收大量的热,可用它做制冷剂或人工降雨
3.工业制纯碱和尿素,是一种重要的化工原料
4.植物光合作用,绿色植物吸收太阳能,利用二氧化碳和水,合成有机物放出氧气
二氧化碳中毒:
二氧化碳中毒是人吸入高浓度的二氧化碳所出现的昏迷及脑缺氧情况,一般大气中二氧化碳含量超过1%时,人即有轻度中毒反应;当超过3%时,开始出现呼吸困难;超过6%时,就会重度中毒甚至死亡。
(1)征状
中毒主要征状有:头痛、头愫晕、耳鸣、气急、胸闷、乏力、心跳加快,面颊发绀、烦躁、谵妄、呼吸困难,如情况持续,就会出现嗜睡、淡漠、昏迷、反射消失、瞳孔散大、大小便失禁、血压下降甚至死亡。
(2)补救
打开门窗、通风孔,抢救者才可进入。将病人救出后,在空气新鲜处进行人工呼吸,心脏按摩,吸氧(避免高压、高流量、高浓度给氧,以免呼吸中枢更为抑制),开始1~2L/分,随病人呼吸好转逐渐增大给氧量(4--5L/分),以至采用高压氧治疗。(最好是纯氧)
吸入兴奋剂:多种兴奋剂交替、联合使用,如洛贝林、山梗菜碱等。
防止脑和肺水肿:应用脱水剂、激素,限制液量和速度,吸入钠的份量亦应限制。
对症治疗:给予多种维生素、细胞色素C、能量合剂、高渗糖,以防感染。
抢救同时要留意有没有其他有毒气体存在,如一氧化碳等。
碱的定义:
碱是指在溶液中电离成的阴离子全部是OH-的化合物。碱由金属离子(或铵根离子)和氢氧根离子构成,可用通式R(OH)n表示。从元素组成来看,碱一定含有氢元素和氧元素。
常见的碱:
(1)氢氧化钠、氢氧化钙都属于碱。除这两种碱外,常见的碱还有氢氧化钾(KOH)、氨水(NH3·H2O)、治疗胃酸过多的药物中的氢氧化铝[Al(OH)3)。
(2)晶体(固体)吸收空气里的水分.表而潮湿而逐步溶解的现象叫做潮解。氢氧化钠、粗盐、氯化镁等物质都易潮解,应保存在密闭干燥的地方。同时称量 NaOH固体时要放在玻璃器皿中,不能放在纸上,防止 NaOH固体潮解后腐蚀天平的托盘。
(3)熟石灰可由生石灰(CaO)与水反应制得,反应的化学方程式为:CaO+H2O==Ca(OH)2,反应时放出大量的热。
碱的通性
常见的碱有NaOH、KOH、Ca(OH)2、氨水的特性:
①氢氧化钠(NaOH)俗名苛性钠、火碱、烧碱,这是因为它有强腐蚀性。NaOH是一种可溶性强碱。白色固体,极易溶于水,暴露在空气中易潮解,可用作碱性气体(如NH3)或中性气体(如H2、O2、CO等)的干燥剂。NaOH易与空气中的CO2反应生成Na2CO3固体。NaOH溶液可以腐蚀玻璃,盛NaOH溶液的试剂瓶不能用磨口的玻璃塞,只能用橡胶塞。
②氢氧化钙[Ca(OH)2]是白色粉末,微溶于水,俗称熟石灰或消石灰,其水溶液称为石灰水。Ca(OH)2也有腐蚀作用。Ca(OH)2与CO2反应生成白色沉淀CaCO3,常用于检验CO2。 Ca(OH)2+CO2=CaCO3↓+H2O Ca(OH)2能跟Na2CO3反应生成NaOH,用于制取NaOH。反应方程式为: Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
③氨水(NH3·H2O)是一种可溶性弱碱,NH3溶于水可得氨水。有刺激性气味,有挥发性。将氨气通过盛放氧化铜的玻璃管,生成氮气、水和铜,其反应方程式为: 2NH3+3CuO=(加热)=3Cu+N2↑+3H2O,说明氨气具有还原性。
此外,KOH、Ba(OH)2也是常见的可溶性强碱。不溶的碱大多是弱碱,如:Fe(OH)3、Cu(OH)2等。他们的共同性质是热稳定性差,受热易分解生成对应的金属氧化物和水。
氢氧化钠、氢氧化钙的物理性质和用途比较
氢氧化钠、氢氧化钙化学性质的比较
几种碱的颜色和溶解度
概念性质的理解
①氢氧化钠有强烈的腐蚀性,使用时必须十分小心,要防止沽到皮肤.上或洒在衣服上。如果不慎将碱液沽到皮肤上,应立即用较多的水冲洗,再涂上硼酸溶液。
②浓硫酸、氢氧化钠固体溶于水放热,属于物理变化;而氧化钙溶于水放热是氧化钙与水反应放出大量的热,属于化学变化;生石灰具有强烈的吸水性,可以作某些气体的干燥剂。
③由于NaOH易潮解,同时吸收空气中的CO2发生变质,所以NaOH必须密封保存。
④保存碱溶液的试剂瓶应用橡胶塞、不能用玻璃塞,以防止长期不用碱溶液,碱溶液腐蚀玻璃造成打不开的情况。
⑤只有可溶性碱溶液才能使指示剂变色,如NaOH溶液能使无色酚酞变红;但不溶性碱不能使指示剂变色,如Mg(OH)2中滴加无色酚酞,酚酞不变色。
⑥盐和碱的反应,反应物中的盐和碱必须溶于水,生成物中至少有一种难溶物、气体或H2O。铵盐与碱反应生成的碱不稳定,分解为NH3和H2O。
⑦碱与酸的反应中碱可以是不溶性碱,如 Cu(OH)2+H2SO4==CuSO4+2H2O。
氢氧化钠和氢氧化钙的鉴别:
NaOH与Ca(OH)2的水溶液都能使酚酞变红,故鉴别NaOH和Ca(OH)2不能用指示剂,通常情况下,可采用以下两种方法来鉴别NaOH和Ca(OH)2
方法一:通入CO2气体,NaOH溶液与CO2气体反应后无明显现象,但Ca(OH)2溶液即澄清石灰水与 CO2反应生成白色沉淀。
方法二:滴加Na2CO3溶液或K2CO3溶液,NaOH溶液与K2CO3,Na2CO3溶液不反应,但Ca(OH)2溶液与 Na2CO3、K2CO3溶液反应均生成白色沉淀。Ca(OH)2+ Na2CO3==CaCO3↓+2NaOH,Ca(OH)2+K2CO3 ==Na2CO3+2KOH。
检验二氧化碳气体是否与氢氧化钠溶液反应的方法
通常情况下,将二氧化碳气体直接通人装有氢氧化钠溶液的试管中,很难直接判断二氧化碳气体是否与氢氧化钠溶液反应。因此,要判断二氧化碳气体确实能与氢氧化钠反应,可以采取如下两种方法:
(1)检验产物的方法:验证通入二氧化碳气体后的溶液中是否含有碳酸钠,检验碳酸根离子是否存在。通常检验碳酸根离子的方法是:
方法1:取样,加入稀盐酸,并将产生的气体通入澄清石灰水中,若澄清石灰水变浑浊,则证明溶液中存在碳酸根离子。
方法2:取样,加入氢氧化钙溶液,若产生白色沉淀,则证明溶液中存在碳酸根离子。上述两种方法其实也可以检验氢氧化钠溶液是否变质.而且方法I还可以用于除去变质后的氢氧化钠溶液中的碳酸钠。
(2)改进实验装置,通过一些明显的实验现象间接证明二氧化碳气体能与氢氧化钠反应。如:
碱的命名:
一般读作氢氧化某,如:NaOH读作氢氧化钠。变价金属元素形成的碱,高价金属碱读作氢氧化某,如Fe(OH)3读作氢氧化铁,低价金属碱读作氢氧化亚某,如Fe(OH)2读作氢氧化亚铁。
氨水:
氨气的水溶液俗称氨水,主要成分是NH3·H2O,通常状况下是无色液体,具有挥发性。浓氨水能挥发出具有刺激性气味的氨气NH3。
氨水显碱性,能使指示剂变色。
氨水的组成中含有N元素,因此可通过与酸反应生成铵盐来制氮肥,其本身也是一种氮肥。在化学实验中一般可用浓氨水做分子运动的探究实验。
碱是指在溶液中电离成的阴离子全部是OH-的化合物。碱由金属离子(或铵根离子)和氢氧根离子构成,可用通式R(OH)n表示。从元素组成来看,碱一定含有氢元素和氧元素。
常见的碱:
(1)氢氧化钠、氢氧化钙都属于碱。除这两种碱外,常见的碱还有氢氧化钾(KOH)、氨水(NH3·H2O)、治疗胃酸过多的药物中的氢氧化铝[Al(OH)3)。
(2)晶体(固体)吸收空气里的水分.表而潮湿而逐步溶解的现象叫做潮解。氢氧化钠、粗盐、氯化镁等物质都易潮解,应保存在密闭干燥的地方。同时称量 NaOH固体时要放在玻璃器皿中,不能放在纸上,防止 NaOH固体潮解后腐蚀天平的托盘。
(3)熟石灰可由生石灰(CaO)与水反应制得,反应的化学方程式为:CaO+H2O==Ca(OH)2,反应时放出大量的热。
碱的通性
| 碱的通性 | 反应规律 | 化学方程式 | 反应类型 |
| 碱溶液与指示剂的反应 | 碱溶液能使紫色石蕊试液变蓝,无色酚酞试液变红 | —— | —— |
| 碱与非金属氧化物反应 | 碱+非金属氧化物→盐+水 | 2NaOH+CO2==Na2CO3+H2O Ca(OH)2+CO2==CaCO3↓+H2O |
—— |
| 碱与酸反应 | 碱+酸→盐+水 | NaOH+HCl==NaCl+H2O 2NaOH+H2SO4==Na2SO4+2H2O |
复分解反应 |
| 碱与某些盐反应 | 碱1+盐1→碱2+盐2 | 2NaOH+CuSO4==Cu(OH)2↓+Na2SO4 Ca(OH)2+Na2CO3==CaCO3↓+2NaOH |
复分解反应 |
| 碱+铵盐→氨气+水+盐 | NH4Cl+NaOH NaCl+NH3↑+H2O NaCl+NH3↑+H2O |
复分解反应 |
常见的碱有NaOH、KOH、Ca(OH)2、氨水的特性:
①氢氧化钠(NaOH)俗名苛性钠、火碱、烧碱,这是因为它有强腐蚀性。NaOH是一种可溶性强碱。白色固体,极易溶于水,暴露在空气中易潮解,可用作碱性气体(如NH3)或中性气体(如H2、O2、CO等)的干燥剂。NaOH易与空气中的CO2反应生成Na2CO3固体。NaOH溶液可以腐蚀玻璃,盛NaOH溶液的试剂瓶不能用磨口的玻璃塞,只能用橡胶塞。
②氢氧化钙[Ca(OH)2]是白色粉末,微溶于水,俗称熟石灰或消石灰,其水溶液称为石灰水。Ca(OH)2也有腐蚀作用。Ca(OH)2与CO2反应生成白色沉淀CaCO3,常用于检验CO2。 Ca(OH)2+CO2=CaCO3↓+H2O Ca(OH)2能跟Na2CO3反应生成NaOH,用于制取NaOH。反应方程式为: Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
③氨水(NH3·H2O)是一种可溶性弱碱,NH3溶于水可得氨水。有刺激性气味,有挥发性。将氨气通过盛放氧化铜的玻璃管,生成氮气、水和铜,其反应方程式为: 2NH3+3CuO=(加热)=3Cu+N2↑+3H2O,说明氨气具有还原性。
此外,KOH、Ba(OH)2也是常见的可溶性强碱。不溶的碱大多是弱碱,如:Fe(OH)3、Cu(OH)2等。他们的共同性质是热稳定性差,受热易分解生成对应的金属氧化物和水。
氢氧化钠、氢氧化钙的物理性质和用途比较
| 俗名 | 苛性钠,火碱,烧碱 | 熟石灰,消石灰 |
| 颜色、状态 | 白色,片状固体 | 白色,粉末状固体 |
| 腐蚀性 | 强烈腐蚀性 | 较强腐蚀性 |
| 溶解性 | 易溶于水,易潮解,溶解时放热 | 微溶于水,其水溶液俗称石灰水 |
| 用途 | 化工原料,用于肥皂、石油、纺织、印染工业等;生活中用于除油污 | 用于建筑工业,制漂自粉,改良土壤,配制农药等 |
氢氧化钠、氢氧化钙化学性质的比较
| 氢氧化钠 | 氢氧化钙 |
| 跟指示剂作用.使紫色石蕊试液变成蓝色,使无色酚酞试液变成红色 | 跟指示剂作用,使紫色石蕊试液变成蓝色,使无色酚酞试液变成红色 |
| 跟某些非金属氧化物反应 2NaOH+CO2==Na2CO3+H2O 2NaOH+SO2==Na2SO3+H2O 2NaOH+SO3==Na2SO4+H2O |
跟某些非金属氧化物反应 Ca(OH)2+CO2==CaCO3↓+H2O Ca(OH)2+SO2==CaSO3↓+H2O Ca(OH)2+SO3==CaSO4+H2O |
| 跟酸发生中和反应 2NaOH+H2SO4==Na2SO4+2H2O |
跟酸发生中和反应 Ca(OH)2+H2SO4==CaSO4+2H2O |
| 跟某些盐反应 2NaOH+CuSO4==Cu(OH)2↓+Na2SO4 |
跟某些盐反应 Ca(OH)2+Na2CO3==CaCO3↓+2NaOH |
几种碱的颜色和溶解度
| 碱 | 颜色 | 溶解性 |
| NaOH、KOH、Ba(OH)2 | 白色 | 易溶 |
| Ca(OH)2 | 白色 | 微溶 |
| Mg(OH)2、Al(OH )3、Fe(OH )2 | 白色 | 难溶 |
| Fe(OH )3 | 红褐色 | 难溶 |
| Cu(OH)2 | 蓝色 | 难溶 |
概念性质的理解
①氢氧化钠有强烈的腐蚀性,使用时必须十分小心,要防止沽到皮肤.上或洒在衣服上。如果不慎将碱液沽到皮肤上,应立即用较多的水冲洗,再涂上硼酸溶液。
②浓硫酸、氢氧化钠固体溶于水放热,属于物理变化;而氧化钙溶于水放热是氧化钙与水反应放出大量的热,属于化学变化;生石灰具有强烈的吸水性,可以作某些气体的干燥剂。
③由于NaOH易潮解,同时吸收空气中的CO2发生变质,所以NaOH必须密封保存。
④保存碱溶液的试剂瓶应用橡胶塞、不能用玻璃塞,以防止长期不用碱溶液,碱溶液腐蚀玻璃造成打不开的情况。
⑤只有可溶性碱溶液才能使指示剂变色,如NaOH溶液能使无色酚酞变红;但不溶性碱不能使指示剂变色,如Mg(OH)2中滴加无色酚酞,酚酞不变色。
⑥盐和碱的反应,反应物中的盐和碱必须溶于水,生成物中至少有一种难溶物、气体或H2O。铵盐与碱反应生成的碱不稳定,分解为NH3和H2O。
⑦碱与酸的反应中碱可以是不溶性碱,如 Cu(OH)2+H2SO4==CuSO4+2H2O。
氢氧化钠和氢氧化钙的鉴别:
NaOH与Ca(OH)2的水溶液都能使酚酞变红,故鉴别NaOH和Ca(OH)2不能用指示剂,通常情况下,可采用以下两种方法来鉴别NaOH和Ca(OH)2
方法一:通入CO2气体,NaOH溶液与CO2气体反应后无明显现象,但Ca(OH)2溶液即澄清石灰水与 CO2反应生成白色沉淀。
方法二:滴加Na2CO3溶液或K2CO3溶液,NaOH溶液与K2CO3,Na2CO3溶液不反应,但Ca(OH)2溶液与 Na2CO3、K2CO3溶液反应均生成白色沉淀。Ca(OH)2+ Na2CO3==CaCO3↓+2NaOH,Ca(OH)2+K2CO3 ==Na2CO3+2KOH。
检验二氧化碳气体是否与氢氧化钠溶液反应的方法
通常情况下,将二氧化碳气体直接通人装有氢氧化钠溶液的试管中,很难直接判断二氧化碳气体是否与氢氧化钠溶液反应。因此,要判断二氧化碳气体确实能与氢氧化钠反应,可以采取如下两种方法:
(1)检验产物的方法:验证通入二氧化碳气体后的溶液中是否含有碳酸钠,检验碳酸根离子是否存在。通常检验碳酸根离子的方法是:
方法1:取样,加入稀盐酸,并将产生的气体通入澄清石灰水中,若澄清石灰水变浑浊,则证明溶液中存在碳酸根离子。
方法2:取样,加入氢氧化钙溶液,若产生白色沉淀,则证明溶液中存在碳酸根离子。上述两种方法其实也可以检验氢氧化钠溶液是否变质.而且方法I还可以用于除去变质后的氢氧化钠溶液中的碳酸钠。
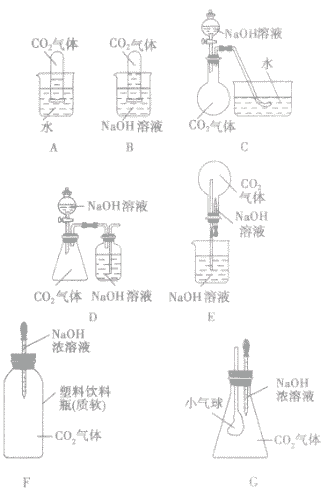
(2)改进实验装置,通过一些明显的实验现象间接证明二氧化碳气体能与氢氧化钠反应。如:

| 所选装置 | 操作方法 | 实验现象 |
| A | 将充满二氧化碳的试管倒扣在水中 | 试管内的液面略有上升 |
| B | 将充满二氧化碳的试管倒扣在氢氧化钠溶液中 | 试管内的液面明显上升 |
| C | 将氢氧化钠溶液滴入烧瓶 | 水槽中的水倒吸入烧瓶内 |
| D | 将氢氧化钠溶液滴入锥形瓶 | 集气瓶中,NaOH溶液中的长导管下端产生气泡 |
| E | 将胶头滴管中氢氧化钠溶液挤入烧瓶 | 烧瓶内产生“喷泉” 现象 |
| F | 将胶头滴管中的氢氧化钠溶液挤入软塑料瓶 | 塑料瓶变瘪 |
| G | 将胶头滴管中的氢氧化钠溶液挤入锥形瓶中 | 小气球胀大 |
碱的命名:
一般读作氢氧化某,如:NaOH读作氢氧化钠。变价金属元素形成的碱,高价金属碱读作氢氧化某,如Fe(OH)3读作氢氧化铁,低价金属碱读作氢氧化亚某,如Fe(OH)2读作氢氧化亚铁。
氨水:
氨气的水溶液俗称氨水,主要成分是NH3·H2O,通常状况下是无色液体,具有挥发性。浓氨水能挥发出具有刺激性气味的氨气NH3。
氨水显碱性,能使指示剂变色。
氨水的组成中含有N元素,因此可通过与酸反应生成铵盐来制氮肥,其本身也是一种氮肥。在化学实验中一般可用浓氨水做分子运动的探究实验。
常见的碱的用途:
1. 氢氧化钠:是重要的化工原料,广泛用于肥皂、石油、造纸、纺织和印染等工业。实验室中可作干燥剂。
2. 氢氧化钙:用于建筑业,制漂白粉,改良土壤。常用于实验室二氧化碳的检验。
1. 氢氧化钠:是重要的化工原料,广泛用于肥皂、石油、造纸、纺织和印染等工业。实验室中可作干燥剂。
2. 氢氧化钙:用于建筑业,制漂白粉,改良土壤。常用于实验室二氧化碳的检验。
发现相似题
与“物质的性质与物质的组成、结构、用途密切相关.请回答:(1)...”考查相似的试题有:
- 下图是生活中一些常见物质的pH,其中能使无色酚酞溶液变红的是
- 日常生活中的下列做法,可行的是 ( )A.高层住房着火时,立即打开所有门窗B.夜晚发现液化气泄漏立即开灯检查C.用氢氧化镁...
- 如图所示是某反应前后的微观示意图,“○”和“●”表示两种不同的原子,则该反应( )A.是化合反应 B.有单质生成 C.反应前后分子...
- 大棚种植农作物时,冬季需要向棚内定期补充适量的CO2.某同学设计的施放CO2的方案如下:在棚内高处挂上塑料桶,内盛工业废盐...
- 我市连续三年大旱造成部分地区人畜饮水困难,各地采取多种措施积极抗旱.(1)某些地方用混浊的河塘水作生活用水,可加絮凝剂...
- 工业用盐酸因含FeCl3而显黄色,现向1~2ml工业盐酸中逐滴加入NaOH溶液,其加入量(x)与生成沉淀量(y)的关系图应是( )A....
- 请从“a熟石灰,b食盐,c石墨,d酚酞溶液,e石蕊溶液”中选择合适的物质填空.(1)常用于改良酸性土壤的物质是______;(2)可...
- A、B、C、D、E、F、G都是初中化学中常见的化合物,其中E是酸,B、C是碱,它们之间可发生如下反应:1A+3B=C↓+3D ②E+F=G↓+HNO3③...
- (2011年·衡阳) 下图表示的是身边一些物质在常温时的近似PH,有关这些物质的比较或判断不正确的是( )A.草木灰水呈碱性B....
- 下列各组物质的溶液,不需要外加试剂就能鉴别出来的是( )A.NaOH,FeCl3,HCl,KClB.Na2SO4,NaCl,BaCl2,KNO3C.Na2SO4...