本试题 “在①洁净的空气;②液态氧;③四氧化三铁;④高锰酸钾;⑤二氧化碳;⑥自来水中(1)属混合物的是______(填序号,下同);(2)属于纯净物的是______;(3)属于氧...” 主要考查您对爆炸、自燃
纯净物和混合物
氧化物
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 爆炸、自燃
- 纯净物和混合物
- 氧化物
自燃:
1. 概念:自燃是由缓慢氧化引起的自发燃烧。如果缓慢氧化产生的热量不能及时散失,就会越积越多,当温度升高到可燃物的着火点时,如果再遇到氧气就会引起自发的燃烧,这就是自燃。
爆炸:
1. 概念:通常说的爆炸指可燃物拒有限空间内急速燃烧,短时间内聚积大量的热量,使气体体积迅速膨胀引起的爆炸。
自燃:
露在地表的煤层,由于气候炎热,发生缓慢氧化反应而导致自燃。
贮存棉花、饲草的仓库,沾满机器油的破布、棉丝等堆积时间长了,通风不好有时就会自燃。在干燥的季节,森林也会自燃。
在坟地里出现“磷火”也是一种自燃现象。
人和动物机体里含磷的有机物腐败分解能生成磷化氢气体。这种气体着火点很低,接触空气就会自燃。在缺乏科学知识的时代,常把这种自燃现象说成是“鬼火”。
平时将白磷浸泡在冷水里,防止自燃。白磷的着火点低(40℃),可用它做自燃实验。取出少许白磷溶解在二硫化碳中,然后把溶液倒在滤纸上,待二硫化碳挥发后,白磷在滤纸上与空气中氧气充分接触就会自燃。
爆炸:
爆炸是我们日常生活中常见的观象,但有的爆炸仅仅是由物理变化引起的,如轮胎爆炸;有螳爆炸则是由化学变化引起的,如火药爆炸,汽油、液化气等燃料的爆炸等。其中,由化学变化引起的爆炸是学习的重点,这种类型的爆炸主要是由于:
①在有限的空间 (如炸弹)内,发生急速的燃烧,短时问聚积大量的热,使气体的体积迅速膨胀;
②氧气的浓度高,或者可燃物 (气体、粉尘)与氧气的接触面积很大,燃烧范围广,周围的空气迅速猛烈膨胀。防止这类爆炸的方法:通风,禁止烟火等。
燃烧,缓慢氧化,自燃,爆炸(由化学变化引起)的比较:
| 燃烧 | 缓慢氧化 | 自燃 | 爆炸 | |
| 概念 | 可燃物与氧气发生的一种发光放热的剧烈的氧化反应 | 缓慢进行的氧化反应 | 由缓慢氧化引起的自发燃烧 | 可燃物在有限空间内发生的急速燃烧 |
| 能量变化 | 放热明显 | 放出热量随时散失 | 放热明显 | 放热明显 |
| 温度 | 达到可燃物的着火点 | 未达到可燃物的着火点 | 达到可燃物的着火点 | 达到可燃物的着火点 |
| 是否发光 | 发光 | 无明显发光现象 | 发光 | 发光 |
| 联系 | 均属于氧化反应,均放出热量 | |||
易燃易爆物的安全知识:
(1)易燃物:一般来说,易燃物指的是那些易燃的气体和液体,容易燃烧、自燃或遇水可以燃烧的固体,以及一些可以引起其他物质燃烧的物质等。常见的有硫;磷、酒精,液化石油气、氢气、乙炔、沼气、石油产品、面粉、棉絮等。
(2)易爆物:指的是那受热或受到撞击时.容易发生爆炸的物质。
(3)一些与燃烧和爆炸有关的图标:

(4)再生产、运输、使用、储存易燃、易爆物时的注意事项:
①对厂房和仓库的要求:与周围建筑物间有足够的防火距离。车间,仓库要有防火、防爆、通风、静电除尘、消防等器材设备,严禁烟火,杜绝一切可能产生火花的因素。容器要求:要牢固、密封、警示标志明显且要注明物品名称、化学性质、注意事项。
③存放要求:单存、单放、远离火种:注意通风。
④运输要求:轻拿轻放、勿撞击。
⑤工作人员要求:严禁烟火、人走电断。
火灾自救及逃生策略:
(1)可燃性气体泄漏时的注意事项当室内天然气、液化石油气、煤气泄漏后室内充满可燃性气体.在此环境中打电话或打开换气扇开关,可能产生电火花,造成爆炸、所以应先关闭总阀、开窗通风,并在杜绝一切明火的同时,查找泄露的原因。
(2)火灾自救策略
①迅速找到安全通道;
②火灾时上层空气中氧气少,毒气浓度大,所以要匍匐前进:
③房间发生火灾时不能随时开门开窗,开门开窗会增加氧气量,使火势更加凶猛;
④火灾时,会产生大量浓烟,使人窒息,因此最好用湿布捂住口鼻;
⑤在山林中遇到火灾时,应逆风而跑,因为顺着风更容易被烧伤或发生危险。
爆炸极限:
(1)概念:可燃性气体在空气中达到一定浓度时,遇到明火会发生爆炸,人们把容易导致爆炸的空气中可燃性气体的体积分数范围,称为该气体的爆炸极限。
①当可燃性气体在混合气体中的含量高于爆炸极限的上限时,可燃性气体可以安静地燃烧;而低于爆炸极限的下限时,则无法燃烧。
②我们通常所说额可燃性气体检验纯度,其实就是检验可燃性气体有没有达到爆炸极限,只要超过爆炸极限的上限,可燃性气体就可以安静的燃烧。
(2)几种常见物质的爆炸极限
| 可燃物 | 爆炸极限 |
| 甲烷 | 5%-15% |
| 丙烷 | 2.2%-9.5% |
| 乙醇 | 3.4%-19% |
| 氢气 | 4.0%-75% |
| 一氧化碳 | 12.5%-74% |
| 液化气 | 2.0%-12% |
| 水煤气 | 7.0%-72% |
粉尘爆炸实验:
(1)实验装置及步骤
下面是模拟粉尘爆炸的一个实验:如下图所示,在无盖小塑料筒里放入干燥面粉,点燃蜡烛,用塑料盖盖住金属筒,迅速鼓入大量空气,不久,便会听到“砰”的一声,爆炸的气浪将金属筒的塑料盖掀起。
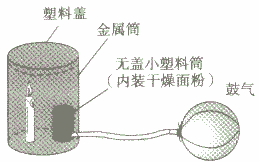
(2)现象:砰的一声响,伴随着一团火光产生,放热,塑料盖被掀起。
(3)分析:面粉被吹起,与空气充分接触,又被蜡烛点燃,在有限空间内发生急剧地燃烧,并让出大量热,产生的气浪将塑料盖掀起,说明可燃物的粉尘在有限的空间内急剧燃烧,能发生爆炸。
混合物:
(1)概念:由两种或多种物质混合而成的物质,没有有固定的组成,各成分保持自己原有的化学性质。
(3)常见的混合物:空气、合金、矿石、溶液等。
(4)混合物的提纯:混合物经过物理或化学的方法可以提纯。
纯净物:
(1)概念:只由一种物质组成的物质。
(3)纯净物的分类:纯净物根据物质组成的元素种类,分为两大类:单质和化合物。
纯净物和氧化物的区别:
| 纯净物 | 混合物 | |
| 概念 | 宏观:由一种物质组成的物质 微观:由同种分子构成(对于由分子构成的物质而言) |
宏观:由两种或多种物质组成的物质 微观:由不同种分子构成(对于由分子构成的物质而言) |
| 区别 | 由同种物质组成(对于由分子构成的物质,是由同种分子构成的),组成是固定的 | 由不同种物质组成(对于由分子构成的物质. 是由不同种分子构成的),组成是不固定的 |
| 特点 | ①具有固定的组成 ②具有一定的性质 ③有专门的化学符号 |
①没有固定的组成和性质 ②各成分保持各自的性质 ③没有专门的化学符号 |
| 分离方法 | 组成固定,不需分离;若需将化合物分成几种单质,则必须通过化学方法才能实现 | 物理方法: 筛选 过滤 蒸馏 |
| 实例 | 氧气,二氧化碳,高锰酸钾 | 空气,粗盐,蔗糖水 |
| 联系 | 纯净物是相对而言的,自然界中绝对纯净的物质是不存在的,通常的纯净物是指含杂质很少的具有高纯度的物质。两者间的关系为 | |
对纯净物和混合物概念的理解:
(1)混合物概念:混合物可以看作是由几种纯净物混合而成的,混合物的形成过程中发生的是物理变化。由于混合物的组成一般不固定,所以往往不能用化学式表示。
(2)纯净物概念:纯净物只由一种物质组成,有固定的组成.可以用化学式表示。
常考的纯净物与混合物:
(1)混合物:石油、煤、天然气、洁净的空气、生理盐水、矿泉水、汽水、碘酒、白酒、双氧水、盐酸、合金等都是混合物。
(2)纯净物:水银、烧碱、纯碱、胆矾、液态氧、液态氮、蒸馏水(纯水)、干冰、冰水共存物、金刚石、石墨、生石灰、熟石灰、氯化钠、氧化铁等都是纯净物:
物质的分类示意图:
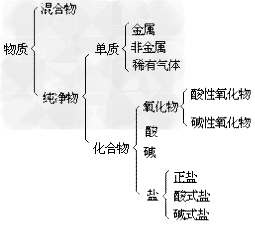
1.定义:由两种元素组成,其中一种是氧元素的化合物(即由氧元素和另一种元素组成的化合物)。
2.分类:
(1)根据组成分类:
金属氧化物,如Na2O,CuO等
非金属氧化物,如CO2,NO等
(2)根据性质分类:
①酸性氧化物
能和碱反应生成盐和水的氧化物如CO2,SO3等
②碱性氧化物
能和酸反应生成盐和水的氧化物如CaO、Fe2O3等
③两性氧化物(初中不作要求)
④不成盐氧化物
不能直接反应生成盐的氧化物如CO,NO等
金属氧化物性质小结:
1.与水反应生成碱(可溶性金属氧化物)
Na2O+H2O==2NaOH
CaO+H2O==Ca(OH)2
2.与强酸反应
CaO+2HCI==CaCl2+H2O
Fe2O3+6HCl==2FeCl3+3H2O
Fe2O3+3H2SO4==Fe2(SO)3+3H2O
CuO+2HCl==CuCl2+H2O
CuO+H2SO4==CuSO4+H2O
3.与H2、CO或C反应
CuO+H2==Cu+H2O
2CuO+C==2Cu+CO2↑
CuO+CO==Cu+CO2
Fe2O3+3H2==2Fe+3H2O
2Fe2O3+3C==4Fe+3CO2↑
Fe2O3+3CO==2Fe+3CO2
Fe3O4+4H2==3Fe+4H2O
Fe3O4+2C==3Fe+2CO2↑
Fe3O4+4CO==3Fe+4CO2
非金属氧化物性质小结:
1.部分非金属氧化物与水反应生成相应的酸
CO2+H2O==H2CO3
SO2+H2O==H2SO3
2.与碱反应生成盐和水
Ca(OH)2+CO2==CaCO3↓+H2O
2NaOH+CO2==Na2CO3+H2O
Ca(OH)2+SO2==CaSO3↓+H2O
2NaOH+SO2==Na2SO3+H2O
易错点:
①酸性氧化物多数是非金属氧化物,但也可能是金属氧化物(如Mn2O7);碱性氧化物肯定是金属氧化物。
②非金属氧化物一般都是酸性氧化物,但H2O、CO、NO等不是酸性氧化物。
过氧化物:
常见的过氧化物有过氧化氢(H2O2)、过氧化钠 (Na2O2)。
过氧化氢俗称双氧水,在催化剂的催化作用下能分解生成水和氧气,常用于实验室制取氧气。过氧化氢具有极强的氧化性,可用作杀菌剂,漂白剂。
过氧化钠能与二氧化碳反应:2Na2O2+2CO2== 2Na2CO3+O2,根据该性质,可将过氧化钠用在坑道、潜艇或宁宙飞船等缺氧的场所,将人们呼出的CO2转换成O2,供给呼吸。
与“在①洁净的空气;②液态氧;③四氧化三铁;④高锰酸钾;⑤二氧化碳...”考查相似的试题有:
- 下列变化中,由化学变化而引起的爆炸是( )A.火药爆炸B.蒸气锅爆炸C.气球爆炸D.压力锅爆炸
- 安全火柴的火柴头上主要含有氯酸钾、二氧化锰、硫和玻璃粉等,火柴杆上涂有少量的石蜡,火柴盒两边的摩擦层是由红磷和玻璃粉...
- 自来水消毒过程中通常会发生化学反应,其反应的微观过程可用下图表示: (1)请写出该反应的化学方程式 。(2)A物质属于 。(...
- 已知一种粒子的核电荷数,一定能知道…………………………………………… ( )A.相对原子质量B.相对分子质量C.中子数D.质子数
- 某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水蒸气都是可再生能源;③使用车用乙醇汽油防止“温室效应;④...
- 根据下图所示的信息及所学知识判断,下列对CO和Co的说法中,正确的是① 钴的相对原子质量为27 ② Co表示钴元素③ CO表示由两种元...
- 下列说法错误的是( )。A.质子数相同的粒子不一定是同种元素的原子B.单质和化合物属于包含关系C.加碘盐中的“碘”通常是指...
- 在“宏观——微观——符号”之间建立联系,是化学学科特有的思维方式。下图表示两种气体发生的化学反应的微观示意图,其中相同的球...
- 以下每小题由三种物质组成一组。从备选答案中找出跟它们同一类别的物质,将编号填入空格内。⑴氧气,氮气,氦气, 。[ ]A.水蒸...
- 下列物质中,属于纯净物的是A.生铁B.洁净的空气C.蒸馏水D.澄清石灰水