本试题 “NH3在催化剂存在时能还原NOx为N2和H2O,这是目前国外硝酸厂进行尾气治理所普遍采用的一种方法.下图是某校化学兴趣小组设计的模拟氨气还原NO的装置.回答下列...” 主要考查您对氨气的制取
化学平衡的有关计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氨气的制取
- 化学平衡的有关计算
(1)实验室用氢氧化钙和氯化铵制取氨气
2NH4Cl+Ca(OH)2 CaCl2+2NH3+2H2O
CaCl2+2NH3+2H2O
(2)仪器:铁架台,铁夹,酒精灯,两个大试管,棉花;氯化铵固体,氢氧化钙固体。
(3)装置图: 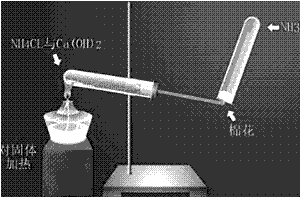
(4)注意:
a. 一般用Ca(OH)2,而不用NaOH,因NaOH碱性太强,对大试管腐蚀比Ca(OH)2强。
b. 选用Ca(OH)2时要检验消石灰是否变质, 因经过长期存放后消石灰部分变成碳酸钙,最好用新制的消石灰。
c. NH4CL与Ca(OH)2质量比5:8为宜,如用(NH4)2SO4代替NH4CL,则质量比为1:1,消石灰过量,以防止生成氨合物。
d. 试管口(盛固体药品的试管)要略向下倾斜;
e. 固体药品要平铺试管底部;
f.导出氨气的导管要短,收集氨气的导管要长,伸入试管底部;
g.为使氨气收集更多,防止空气中的水蒸汽进入收集氨气的试管,在试管口防一块,但不能堵死
h.酒精灯加热用外焰,先均匀加热,后对固体加热。
(5)收集方法: 用向下排气法取气法收集。因氨气极易溶于水,比空气轻。
干燥氨气: 用碱石灰,不能用浓硫酸和氯化钙干燥氨气。
检验氨气:用湿润的红色石蕊试纸,氨气能使湿润的红色石蕊试纸变蓝。
化学平衡计算的一般思路和方法:
有天化学平衡的计算一般涉及各组分的物质的量、浓度、转化率、百分含量,气体混合物的密度、平均摩尔质量、压强等。通常的思路是写出反应方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的火系,列出比例式或等式或依据平衡常数求解,这种思路和方法通常称为“三段式法”、如恒温恒压下的反应mA(g)+nB(g) pC(g)+ qD(g)
pC(g)+ qD(g)
(1)令A、B的起始物质的量分别为amol,bmol 达到平衡后,A的消耗量为m·xmol,容器容积为VL。
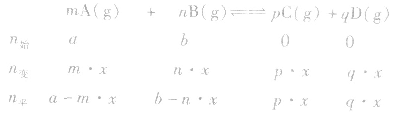
则有:

(2)对于反应物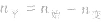 ,对于生成物
,对于生成物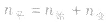
(3)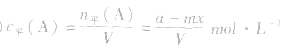
(4)A的转化率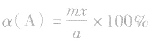
(5)平衡时A的体积(物质的量)分数
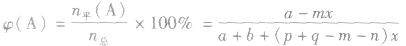
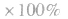
(6)
(7)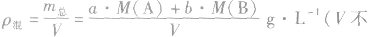
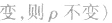
(8)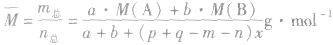
有天化学平衡的计算一般涉及各组分的物质的量、浓度、转化率、百分含量,气体混合物的密度、平均摩尔质量、压强等。通常的思路是写出反应方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的火系,列出比例式或等式或依据平衡常数求解,这种思路和方法通常称为“三段式法”、如恒温恒压下的反应mA(g)+nB(g)
 pC(g)+ qD(g)
pC(g)+ qD(g) (1)令A、B的起始物质的量分别为amol,bmol 达到平衡后,A的消耗量为m·xmol,容器容积为VL。
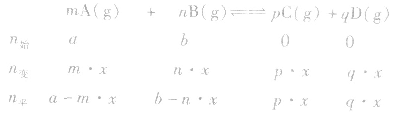
则有:

(2)对于反应物
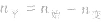 ,对于生成物
,对于生成物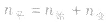
(3)
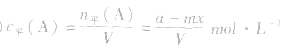
(4)A的转化率
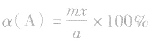
(5)平衡时A的体积(物质的量)分数
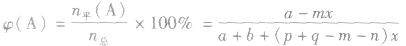
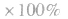
(6)

(7)
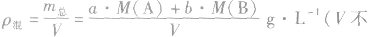
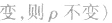
(8)
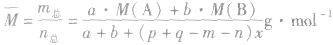
发现相似题
与“NH3在催化剂存在时能还原NOx为N2和H2O,这是目前国外硝酸厂进...”考查相似的试题有:
- X、Y、Z为三种气体,把a mol X和b mol Y充入一密闭容器中,发生反应X+2Y2Z,达到平衡时,若它们的物质的量满足:n(X)+n(Y)...
- 在密闭容器中发生如下反应:mA(g)+nB(g)pC(g)达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,...
- 体积完全相同的恒容容器A和B,已知A装有SO2和O2各1g,B装有SO2和O2各2g,在相同温度下反应达到平衡时A中SO2的转化率为a%,B中...
- 下列事实不能用勒夏特列原理解释的是 ( )A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 B.合成氨工厂...
- 下列生产、生活等实际应用,不能用勒夏特列原理解释的是( )A.合成氨的反应温度控制在500℃进行 B.用难溶FeS固体除去工业...
- 在容积为2L的密闭容器中进行反应:CO(g)+2H2(g)CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化...
- 对于反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) ΔH=-444.3 kJ·mol-1,且熵减小,在常温常压下该反应能自发进行,对反...
- 在密闭容器中,发生反应H2(g)+ I2(g)2HI(g),通入xmol H2和ymol I2蒸气,当x=2,y=1时在一密闭容器中某温度条件下反应达到平衡时...
- 在一个固定容积的密闭容器中加入2LX和3LY气体,同时发生如下反应:nX(气)+3Y(气)2R(气)+Q(气),反应达到平衡时,测得...
- 在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:物质XYZ初始浓度/mol·L-10.10.20平衡浓度/mol·L-10.050.050...