本试题 “下列说法不正确的是( )A.铵态氮肥一定不能与碱同时施用B.原子中质子数一定等于中子数C.PH>7的溶液一定是碱性物质D.酸溶液中一定含有氢离子” 主要考查您对化肥
原子结构
原子的定义
酸、碱、盐
氧化物
溶液的酸碱性与pH值
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化肥
- 原子结构
- 原子的定义
- 酸、碱、盐
- 氧化物
- 溶液的酸碱性与pH值
化学肥料的概念:
化学肥料是指以矿物、空气、水做原料,经过化学加工制成含有植物生长所需的营养元素的物质,简称化肥。农作物所必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等,其中氮、磷、钾需要量较大,因此氮肥、磷肥、钾肥是最主要的化学肥料。另外还有同时含有两种或两种以上营养元素的复合肥,植物生长过程中需要量比较少的微量元素肥料。
常见化学肥料:
1、氮肥
①作用:氮是合成蛋白质、核酸和叶绿素的重要元素,氮肥充足会使植物枝繁叶茂、果实硕大。缺少氮元素,会使植物生长发育迟缓或停滞,光合作用减慢等。外观表现为植株矮小,瘦弱,叶片发黄,严重时叶脉为棕色。
②氮肥的特性
a.氮盐与碱混合受热可产生一种无色、有刺激性气味的气体,它能使湿润的红色石蕊试纸变蓝。例如: NaOH+NH4NO3=NaNO3+H2O+NH3↑
检验按根离子(NH4+)时,需有可溶性碱和红色石蕊试纸。
b.氨水是氨气的水溶液,溶于水的氨气大部分与水反应生成一水合氨。一水合氨在水中发生电离,生成铵根离子和氢氧根离子。由于氨水中存在的阴离子全部是OH-,所以氨水呈碱性,一水合氨属于碱类。请注意,通常情况下氨水指氨气溶于水后生成的一水合氨(NH3·H2O),切勿将氨水的化学式写成NH4OH,因为氨水中没有NH4OH存在。
c.碳酸氢按受热分解:NH4HCO3==NH3↑+ CO2↑+H2O↑。
③氮的固定将氮气转化为氮的化合物的方法。如:豆科植物根部的根瘤菌能把空气中的氮气转化为含氮化合物,这类植物无需或只需少量使用氮肥。
2、磷肥
①作用:磷能促进作物生长,增强抗寒、抗旱能力。若缺乏磷元素,常表现为生长迟缓、产量降低,但磷过量则会引起作物贪青晚熟,结实率下降。外观表现为植株特别矮小,叶片出现紫色。
②常见磷肥有磷矿粉[Ca3(PO4)2]、钙镁磷肥(钙和镁的磷酸盐)、过磷酸钙[磷酸二氢钙Ca(H2PO4)2 和CaSO4的混合物]等。
3、钾肥
①作用:钾肥能保证各种代谢过程的顺利进行、促进植物生民、增强抗病虫害和抗倒伏能力。若缺乏钾元素,常表现为茎秆软弱、容易倒伏、叶片的边缘和尖端呈褐色,并逐渐焦枯。
②常见钾肥有硫酸钾(K2SO4)、氯化钾(KCl)和草木灰(主要成分为K2CO3)等。
(4)复合肥
含两种或两种以土营养元素的化肥。
①特点能同时均匀地供给作物几种养分,充分发挥营养元素间的互补作用,有效成分高。
②种类磷酸按〔磷酸二氢铵NH4H2PO4和磷酸氢二按 (NH4)2HPO4的混合物」、硝酸钾(KNO3)。
常见氮肥及性质:
化肥和农家肥的比较:
使用化肥、农药的利与弊:
①利:化肥、农药对提高农作物的产量具有重要的作用。
②弊:
a.不合理施用化肥会带来很多环境问题,一方面化肥中含有一些重金属元素、有毒有机物和放射性物质,施人后会引起潜在的土壤污染;另一方面化肥在施用过程中,因某些成分的积累、流失或变化,引起土壤酸化,水域中氮和磷含量升高,氮化物和硫化物气体排放等,造成土壤退化和水、大气环境的污染。
b.农药本身有毒,在杀灭病虫害的同时也带来了对自然环境的污染和对人体健康的危害。
使用化肥的注意事项:
①铰态氮肥不能与碱性物质(如碱、草木灰等)一起使用,因为铵态氮肥中的NH4+遇到OH-会生成易挥发的NH3,降低肥效。
②使用氨水或磷酸氢铵时要防止挥发,立即灌溉或用土盖上,人要站在上风口,因氨气对人的眼、鼻等膜有刺激作用。
③硝酸按受热易分解,在高温或猛烈撞击时易发生爆炸。所以当硝酸铵受潮结块时,不要用铁锤砸碎。
④硫酸按不易长时间使用,以免造成土壤酸性增强或土壤板结。
化肥鉴别的方法:
①一看、二闻、三溶看外观,氮肥、钾肥为白色晶体,磷肥是灰白色粉末;闻气味,碳酸氢按有强烈的氨味,可直接将它与其他氮肥相区别;加水溶解,氮肥、钾肥全部溶于水,磷肥大多不溶于水。铵盐的鉴别:(NH4)2SO4、NH4NO3等和熟石灰混合研磨,放出具有刺激性气味的氨气。
②氮肥的简易鉴别氮肥中的氨水呈液态,碳酸氧钱有强烈的氨味,据此可直接将它们与其他氮肥相区别。其他常见氮肥可按下列步骤鉴别:
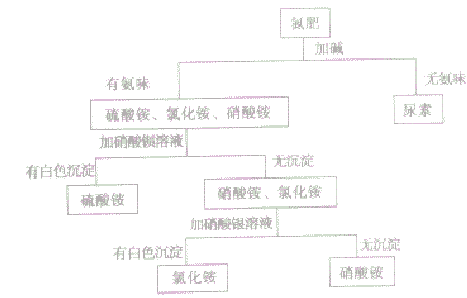
注意硫酸铵、氯化铵、硝酸铵同时鉴别时,不能先加硝酸银溶液鉴别氯化铵,因为硝酸银与硫酸铵反应,可能生成微溶物硫酸银,也可能出现沉淀。所以要区分含SO42-、Cl-和NO3-的三种物质时,一般是先加硝酸钡来鉴别出含有SO42-的物质,再加入硝酸银,鉴别出含有Cl-的物质,无现象的则是含有NO3-的物质。
③化肥鉴别歌鉴别化肥简易行,无锈铁片火烧红;化肥分别铁上放,各自现象皆不同;遇铁冒烟化成水,定是尿素不可疑;若是只熔不冒烟,刺鼻气味是磷铵;一阵烟后冒火星,必是硝铵显神通;铁上发出紫火焰,吱吱微响是硫铵;要想测知氯化铵,触铁味如浓盐酸;磷肥多为灰白色,置于红铁味难闻;放于红铁爆噼啪,无氨味者硫酸钾,氨化磷肥与有别,无烟臭气呛煞人;上述现象若不符,其中有诈须谨慎;认真鉴别把握准,防止上当把钱费。
盐的命名:
(1)只有两种元素组成的盐,读作“某化某”,如 NaCl读作氯化钠,AgI读作碘化银。
(2)构成中含有酸根的,读作“某酸某”。如Na2CO3、ZnSO4、AgNO3、KMnO4、KClO3分别读作:碳酸钠、硫酸锌、硝酸银、高锰酸钾、氯酸钾。
(3)含铵根的化合物,读作“某化铵”或“某酸铵”。如NH4Cl、(NH4)2SO4读作:氯化铵、硫酸铵。
(4)其他:Cu2(OH)2CO3读作“碱式碳酸铜”, NaHSO4读作“硫酸氢钠”, NaHCO3读作“碳酸氢钠”。
化学肥料是指以矿物、空气、水做原料,经过化学加工制成含有植物生长所需的营养元素的物质,简称化肥。农作物所必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等,其中氮、磷、钾需要量较大,因此氮肥、磷肥、钾肥是最主要的化学肥料。另外还有同时含有两种或两种以上营养元素的复合肥,植物生长过程中需要量比较少的微量元素肥料。
常见化学肥料:
1、氮肥
①作用:氮是合成蛋白质、核酸和叶绿素的重要元素,氮肥充足会使植物枝繁叶茂、果实硕大。缺少氮元素,会使植物生长发育迟缓或停滞,光合作用减慢等。外观表现为植株矮小,瘦弱,叶片发黄,严重时叶脉为棕色。
②氮肥的特性
a.氮盐与碱混合受热可产生一种无色、有刺激性气味的气体,它能使湿润的红色石蕊试纸变蓝。例如: NaOH+NH4NO3=NaNO3+H2O+NH3↑
检验按根离子(NH4+)时,需有可溶性碱和红色石蕊试纸。
b.氨水是氨气的水溶液,溶于水的氨气大部分与水反应生成一水合氨。一水合氨在水中发生电离,生成铵根离子和氢氧根离子。由于氨水中存在的阴离子全部是OH-,所以氨水呈碱性,一水合氨属于碱类。请注意,通常情况下氨水指氨气溶于水后生成的一水合氨(NH3·H2O),切勿将氨水的化学式写成NH4OH,因为氨水中没有NH4OH存在。
c.碳酸氢按受热分解:NH4HCO3==NH3↑+ CO2↑+H2O↑。
③氮的固定将氮气转化为氮的化合物的方法。如:豆科植物根部的根瘤菌能把空气中的氮气转化为含氮化合物,这类植物无需或只需少量使用氮肥。
2、磷肥
①作用:磷能促进作物生长,增强抗寒、抗旱能力。若缺乏磷元素,常表现为生长迟缓、产量降低,但磷过量则会引起作物贪青晚熟,结实率下降。外观表现为植株特别矮小,叶片出现紫色。
②常见磷肥有磷矿粉[Ca3(PO4)2]、钙镁磷肥(钙和镁的磷酸盐)、过磷酸钙[磷酸二氢钙Ca(H2PO4)2 和CaSO4的混合物]等。
3、钾肥
①作用:钾肥能保证各种代谢过程的顺利进行、促进植物生民、增强抗病虫害和抗倒伏能力。若缺乏钾元素,常表现为茎秆软弱、容易倒伏、叶片的边缘和尖端呈褐色,并逐渐焦枯。
②常见钾肥有硫酸钾(K2SO4)、氯化钾(KCl)和草木灰(主要成分为K2CO3)等。
(4)复合肥
含两种或两种以土营养元素的化肥。
①特点能同时均匀地供给作物几种养分,充分发挥营养元素间的互补作用,有效成分高。
②种类磷酸按〔磷酸二氢铵NH4H2PO4和磷酸氢二按 (NH4)2HPO4的混合物」、硝酸钾(KNO3)。
常见氮肥及性质:
| 名称 | 化学式 | 性质 | 注意事项 |
| 尿素 | CO(NH2)2 | 白色或淡黄色晶体,易溶 于水,含氮量不超过46.7%, 肥效高且持久,对土壤无 不良影响 |
—— |
| 碳酸氢铵 | NH4HCO3 | 白色晶体,易溶于水,受潮 时常温下就能分解,温度越 高,分解越快,在土壤中不 残留有害杂质,含氮量低于 17.7% |
防分解,贮存和运输时 都要密封.不要受潮或暴 晒,施肥后掩盖或立即 灌溉,不要与碱性物质 混合使用 |
| 硝酸铵 | NH4NO3 | 白色晶体,易溶于水,高温 或受猛烈撞击时易爆炸,含 氮量低于35%,对土壤无不 良影响 |
不要与易燃物质或碱性 物质混合在一起,结块 时,不要用铁锤砸碎 |
| 硫酸铵 | (NH4)2SO4 | 白色固体,易溶于水,常温 下性质稳定,不宜长期大量 使用,否则会使土壤酸化、 板结硬化 |
不能与碱性物质混合, 不宜长期大量使用 |
| 氨水 | NH3·H2O | 氨气的水溶液,易挥发,显碱性 | 运愉、扩存、使用时要 防挥发 |
化肥和农家肥的比较:
| 所含元素种类少,但营养元素含量大 | 常含有多种营养元素,但营养元素含量较少 |
| 一般易溶于水,易被农作物吸收,肥效较快 | 一般较难溶于水,经腐熟后逐步转化为可溶于水、能被作物吸收的物质,肥效慢但肥期较长 |
| 便于工业生产,成本较高 | 便于就地取材,成本低廉 |
| 长期使用会破坏土壤的结构,使果蔬、谷物含有超量化肥,影响人体健康;化肥还会造成水体污染,引起水体富营养化 | 能改良土壤结构 |
使用化肥、农药的利与弊:
①利:化肥、农药对提高农作物的产量具有重要的作用。
②弊:
a.不合理施用化肥会带来很多环境问题,一方面化肥中含有一些重金属元素、有毒有机物和放射性物质,施人后会引起潜在的土壤污染;另一方面化肥在施用过程中,因某些成分的积累、流失或变化,引起土壤酸化,水域中氮和磷含量升高,氮化物和硫化物气体排放等,造成土壤退化和水、大气环境的污染。
b.农药本身有毒,在杀灭病虫害的同时也带来了对自然环境的污染和对人体健康的危害。
使用化肥的注意事项:
①铰态氮肥不能与碱性物质(如碱、草木灰等)一起使用,因为铵态氮肥中的NH4+遇到OH-会生成易挥发的NH3,降低肥效。
②使用氨水或磷酸氢铵时要防止挥发,立即灌溉或用土盖上,人要站在上风口,因氨气对人的眼、鼻等膜有刺激作用。
③硝酸按受热易分解,在高温或猛烈撞击时易发生爆炸。所以当硝酸铵受潮结块时,不要用铁锤砸碎。
④硫酸按不易长时间使用,以免造成土壤酸性增强或土壤板结。
化肥鉴别的方法:
①一看、二闻、三溶看外观,氮肥、钾肥为白色晶体,磷肥是灰白色粉末;闻气味,碳酸氢按有强烈的氨味,可直接将它与其他氮肥相区别;加水溶解,氮肥、钾肥全部溶于水,磷肥大多不溶于水。铵盐的鉴别:(NH4)2SO4、NH4NO3等和熟石灰混合研磨,放出具有刺激性气味的氨气。
②氮肥的简易鉴别氮肥中的氨水呈液态,碳酸氧钱有强烈的氨味,据此可直接将它们与其他氮肥相区别。其他常见氮肥可按下列步骤鉴别:

注意硫酸铵、氯化铵、硝酸铵同时鉴别时,不能先加硝酸银溶液鉴别氯化铵,因为硝酸银与硫酸铵反应,可能生成微溶物硫酸银,也可能出现沉淀。所以要区分含SO42-、Cl-和NO3-的三种物质时,一般是先加硝酸钡来鉴别出含有SO42-的物质,再加入硝酸银,鉴别出含有Cl-的物质,无现象的则是含有NO3-的物质。
③化肥鉴别歌鉴别化肥简易行,无锈铁片火烧红;化肥分别铁上放,各自现象皆不同;遇铁冒烟化成水,定是尿素不可疑;若是只熔不冒烟,刺鼻气味是磷铵;一阵烟后冒火星,必是硝铵显神通;铁上发出紫火焰,吱吱微响是硫铵;要想测知氯化铵,触铁味如浓盐酸;磷肥多为灰白色,置于红铁味难闻;放于红铁爆噼啪,无氨味者硫酸钾,氨化磷肥与有别,无烟臭气呛煞人;上述现象若不符,其中有诈须谨慎;认真鉴别把握准,防止上当把钱费。
盐的命名:
(1)只有两种元素组成的盐,读作“某化某”,如 NaCl读作氯化钠,AgI读作碘化银。
(2)构成中含有酸根的,读作“某酸某”。如Na2CO3、ZnSO4、AgNO3、KMnO4、KClO3分别读作:碳酸钠、硫酸锌、硝酸银、高锰酸钾、氯酸钾。
(3)含铵根的化合物,读作“某化铵”或“某酸铵”。如NH4Cl、(NH4)2SO4读作:氯化铵、硫酸铵。
(4)其他:Cu2(OH)2CO3读作“碱式碳酸铜”, NaHSO4读作“硫酸氢钠”, NaHCO3读作“碳酸氢钠”。
原子的构成:

原子核的构成:

原子核相对原子来说,体积很小,但质量却很大,原子的质量主要集中在原子核上,电子的质量约为质子质量的 。
。
质子的质量为:1.6726×10-27kg
中子的质量为:1.6749×10-27kg
构成原子的粒子间的关系:

对原子构成的正确理解:
(1)原子核位于原子中心,绝大多数由质子和中构成 (有一种氢原子的原子核内只含有1个质子,无中子),体积极小,密度极大,几乎集中了原子的全部质量,核外电子质量很小,可以忽略不计。
(2)每个原子只有一个原子核,核电荷数(核内质子数)的多少,决定了原了的种类。
(3)在原子中:核电荷数二质子数二核外电子数。
(4)原子核内的质子数不一定等干中子数,如钠原子中,质子数为11,中子数为12。
(5)并不是所有的原子中都有中子,如有一种氢原子中就没有中子。
(6)在原子中,由于质子(原子核)与电子所带电荷数相等,且电性相反,因而原子中虽然存在带电的粒子,但原子在整体上不显电性。
核外电子的排布:
①电子层核外电子运动有自己的特点,在含有多个电子的原子里,有的电子通常在离核较近的区域运动,有的电子通常在离核较远的区域运动,科学家形象地将这些区域称为电子层。
②核外电子的分层排布通常用电子层来形象地表示运动着的电子离核远近的不同:离核越近,电子能量越低;离核越远,电子能量越高。电子层数、离核远近、能量高低的关系如下所示:
电子层数 1 2 3 4 5 6 7
离核远近 近→ 远
能量高低 低→ 高
③核外电子排布的规律了解一些核外电子排布的简单规律对理解原子核外电子排布的情况有很重要的作川,核外电子排布的简单规律主要有:
a.每层上的电子数最多不超过2n2(n为电子层数),如第一电子层上的电子数可能为1,也可能为2,但最多为2。
b.核外电子排布时先排第一层,排满第一层后,再排第二层,依次类推。
c.最外层上的电子数不超过8;当只有一个电子层时,最外层上的电子数不超过2。

原子的不可再分与原子的结构:
化学变化中原子不会由一种原子变成另外一种原子,即化学变化中原了的种类不变,其原因是化学变化中原子核没有发生变化。如硫燃烧生成了二氧化硫,硫和氧气中分别含有硫原子和氧原子,反应后生成的二氧化硫中仍然含硫原子和氧原子。原子不是最小粒子,只是在化学变化的范围内为“最小粒子”,它还可再分,如原子弹爆炸时的核裂变,就是原子发生了变化。原子尽管很小,但具有一定的构成,是由居于原子中心的带正电的原子核和核外带负电的电子构成的。

原子核的构成:

原子核相对原子来说,体积很小,但质量却很大,原子的质量主要集中在原子核上,电子的质量约为质子质量的
 。
。质子的质量为:1.6726×10-27kg
中子的质量为:1.6749×10-27kg
构成原子的粒子间的关系:

对原子构成的正确理解:
(1)原子核位于原子中心,绝大多数由质子和中构成 (有一种氢原子的原子核内只含有1个质子,无中子),体积极小,密度极大,几乎集中了原子的全部质量,核外电子质量很小,可以忽略不计。
(2)每个原子只有一个原子核,核电荷数(核内质子数)的多少,决定了原了的种类。
(3)在原子中:核电荷数二质子数二核外电子数。
(4)原子核内的质子数不一定等干中子数,如钠原子中,质子数为11,中子数为12。
(5)并不是所有的原子中都有中子,如有一种氢原子中就没有中子。
(6)在原子中,由于质子(原子核)与电子所带电荷数相等,且电性相反,因而原子中虽然存在带电的粒子,但原子在整体上不显电性。
核外电子的排布:
①电子层核外电子运动有自己的特点,在含有多个电子的原子里,有的电子通常在离核较近的区域运动,有的电子通常在离核较远的区域运动,科学家形象地将这些区域称为电子层。
②核外电子的分层排布通常用电子层来形象地表示运动着的电子离核远近的不同:离核越近,电子能量越低;离核越远,电子能量越高。电子层数、离核远近、能量高低的关系如下所示:
电子层数 1 2 3 4 5 6 7
离核远近 近→ 远
能量高低 低→ 高
③核外电子排布的规律了解一些核外电子排布的简单规律对理解原子核外电子排布的情况有很重要的作川,核外电子排布的简单规律主要有:
a.每层上的电子数最多不超过2n2(n为电子层数),如第一电子层上的电子数可能为1,也可能为2,但最多为2。
b.核外电子排布时先排第一层,排满第一层后,再排第二层,依次类推。
c.最外层上的电子数不超过8;当只有一个电子层时,最外层上的电子数不超过2。

原子的不可再分与原子的结构:
化学变化中原子不会由一种原子变成另外一种原子,即化学变化中原了的种类不变,其原因是化学变化中原子核没有发生变化。如硫燃烧生成了二氧化硫,硫和氧气中分别含有硫原子和氧原子,反应后生成的二氧化硫中仍然含硫原子和氧原子。原子不是最小粒子,只是在化学变化的范围内为“最小粒子”,它还可再分,如原子弹爆炸时的核裂变,就是原子发生了变化。原子尽管很小,但具有一定的构成,是由居于原子中心的带正电的原子核和核外带负电的电子构成的。
原子结构示意图:
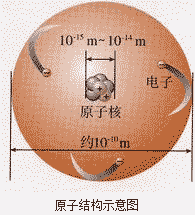
由原子构成的物质:
绝大多数的单质是由原子构成的,如金属单质、稀有气体均是由原子直接构成的,碳、硫、磷等大多数的非金属单质也是由原子直接构成的。
原子的定义:
原子是化学变化中最小的粒子。例如,化学变化中,发生变化的是分子,原子的种类和数目都未发生变化。
对原子的概念可从以下三个方面理解:
①原子是构成物质的基本粒子之一。
②原了也可以保持物质的化学性质,如由原子直接构成的物质的化学性质就由原子保持。
③原子在化学变化中不能再分,是“化学变化中最小的粒子”,脱离化学变化这一条件,原子仍可再分。
原子的性质:
①原子的质量、体积都很小;
②原子在不停地运动;
③原子之间有一定的间隔;
④原子可以构成分子,如一个氧分子是由两个氧原子构成的;也可以直接构成物质,如稀有气体、铁、汞等都是由原子直接构成的;
⑤化学反应中原子不可再分。
原子的表示方法—元素符号:
原子可用元索符号表示:如O既可表示氧元素,也可表示1个氧原子。
分子和原子的联系与区别:
道尔顿的原子模型:
英国自然科学家约翰·道尔顿将古希腊思辨的原子论改造成定量的化学理论,提出了世界上第一个原子的理论模型。他的理论主要有以下四点:
①所有物质都是由非常微小的、不可再分的物质微粒即原子组成
②同种元素的原子的各种性质和质量都相同,不同元素的原子,主要表现为质量的不同
③原子是微小的、不可再分的实心球体
④原子是参加化学变化的最小单位,在化学反应中,原子仅仅是重新排列,而不会被创造或者消失。 虽然,经过后人证实,这是一个失败的理论模型,但道尔顿第一次将原子从哲学带入化学研究中,明确了今后化学家们努力的方向,化学真正从古老的炼金术中摆脱出来,道尔顿也因此被后人誉为“近代化学之父”。

由原子构成的物质:
绝大多数的单质是由原子构成的,如金属单质、稀有气体均是由原子直接构成的,碳、硫、磷等大多数的非金属单质也是由原子直接构成的。
原子的定义:
原子是化学变化中最小的粒子。例如,化学变化中,发生变化的是分子,原子的种类和数目都未发生变化。
对原子的概念可从以下三个方面理解:
①原子是构成物质的基本粒子之一。
②原了也可以保持物质的化学性质,如由原子直接构成的物质的化学性质就由原子保持。
③原子在化学变化中不能再分,是“化学变化中最小的粒子”,脱离化学变化这一条件,原子仍可再分。
原子的性质:
①原子的质量、体积都很小;
②原子在不停地运动;
③原子之间有一定的间隔;
④原子可以构成分子,如一个氧分子是由两个氧原子构成的;也可以直接构成物质,如稀有气体、铁、汞等都是由原子直接构成的;
⑤化学反应中原子不可再分。
原子的表示方法—元素符号:
原子可用元索符号表示:如O既可表示氧元素,也可表示1个氧原子。
分子和原子的联系与区别:
| 项目 | 分子 | 原子 | |
| 不同点 | 本质区别 | 在化学反应中可以分成原子 | 在化学反应中不能再分 |
| 构成物质情况 | 大多数物质由分子构成 | 原子也能直接构成物质,但分子是由原子构成的 | |
| 相同点 | ①质量和体积都很小 ②都在不停地运动 ③粒子间有间隔 ④都是构成物质的粒子 ⑤同种粒子性质相同,不同种粒子性质不同 | ||
| 注意事项 | ①分子是保持物质化学性质的最小粒子 ②原子是化学变化中的最小粒子 ③分子是由原子构成的 ④对于由原子直接构成的物质,原子是保持其化学性质的最小粒子 | ||
| 联系 | 分子是由原子构成的,分子,原子都是构成物质的粒子,它们的关系是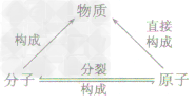 | ||
道尔顿的原子模型:
英国自然科学家约翰·道尔顿将古希腊思辨的原子论改造成定量的化学理论,提出了世界上第一个原子的理论模型。他的理论主要有以下四点:
①所有物质都是由非常微小的、不可再分的物质微粒即原子组成
②同种元素的原子的各种性质和质量都相同,不同元素的原子,主要表现为质量的不同
③原子是微小的、不可再分的实心球体
④原子是参加化学变化的最小单位,在化学反应中,原子仅仅是重新排列,而不会被创造或者消失。 虽然,经过后人证实,这是一个失败的理论模型,但道尔顿第一次将原子从哲学带入化学研究中,明确了今后化学家们努力的方向,化学真正从古老的炼金术中摆脱出来,道尔顿也因此被后人誉为“近代化学之父”。
酸:
1. 定义:电离时生成的阳离子全部是H+的化合物
2. 常见的酸:HCl,H2SO4,HNO3,H3PO4。
碱:
1. 定义:电离时生成的阴离子全部是OH-的化合物
2. 常见的碱:NaOH,KOH,Cu(OH)2,Fe(OH)3等
盐:
1. 定义:电离时生成金属离子(包括NH4+)和酸根离子的化合物
2. 常见的盐:NaCO3,NaCl,NaSO4等
酸、碱、盐的比较:
1. 定义:电离时生成的阳离子全部是H+的化合物
2. 常见的酸:HCl,H2SO4,HNO3,H3PO4。
碱:
1. 定义:电离时生成的阴离子全部是OH-的化合物
2. 常见的碱:NaOH,KOH,Cu(OH)2,Fe(OH)3等
盐:
1. 定义:电离时生成金属离子(包括NH4+)和酸根离子的化合物
2. 常见的盐:NaCO3,NaCl,NaSO4等
酸、碱、盐的比较:
| 从化学组成看 | 从电离观点看 | 组成特点 | |
| 酸 | 由氢元素和酸根组成 | 电离时生成的阳离子全都是氢离子(H+)的化合物 | 一定含氢元素 |
| 碱 | 由金属元素和氢氧根组成(氨水也是碱) | 电离时生成的阴离子全都是氢氧根离子(OH-)的化合物 | 一定含氢、氧 元素 |
| 盐 | 含有金属元素(或NH4+) 和酸根 | 电离时能生成金属离子(或NH4+)和酸根离子的化合物 | 酸式盐中一定含氢元素,碱式盐中一定含氢、氧元素 |
氧化物:
1.定义:由两种元素组成,其中一种是氧元素的化合物(即由氧元素和另一种元素组成的化合物)。
2.分类:
(1)根据组成分类:
金属氧化物,如Na2O,CuO等
非金属氧化物,如CO2,NO等
(2)根据性质分类:
①酸性氧化物
能和碱反应生成盐和水的氧化物如CO2,SO3等
②碱性氧化物
能和酸反应生成盐和水的氧化物如CaO、Fe2O3等
③两性氧化物(初中不作要求)
④不成盐氧化物
不能直接反应生成盐的氧化物如CO,NO等
金属氧化物性质小结:
1.与水反应生成碱(可溶性金属氧化物)
Na2O+H2O==2NaOH
CaO+H2O==Ca(OH)2
2.与强酸反应
CaO+2HCI==CaCl2+H2O
Fe2O3+6HCl==2FeCl3+3H2O
Fe2O3+3H2SO4==Fe2(SO)3+3H2O
CuO+2HCl==CuCl2+H2O
CuO+H2SO4==CuSO4+H2O
3.与H2、CO或C反应
CuO+H2==Cu+H2O
2CuO+C==2Cu+CO2↑
CuO+CO==Cu+CO2
Fe2O3+3H2==2Fe+3H2O
2Fe2O3+3C==4Fe+3CO2↑
Fe2O3+3CO==2Fe+3CO2
Fe3O4+4H2==3Fe+4H2O
Fe3O4+2C==3Fe+2CO2↑
Fe3O4+4CO==3Fe+4CO2
非金属氧化物性质小结:
1.部分非金属氧化物与水反应生成相应的酸
CO2+H2O==H2CO3
SO2+H2O==H2SO3
2.与碱反应生成盐和水
Ca(OH)2+CO2==CaCO3↓+H2O
2NaOH+CO2==Na2CO3+H2O
Ca(OH)2+SO2==CaSO3↓+H2O
2NaOH+SO2==Na2SO3+H2O
易错点:
①酸性氧化物多数是非金属氧化物,但也可能是金属氧化物(如Mn2O7);碱性氧化物肯定是金属氧化物。
②非金属氧化物一般都是酸性氧化物,但H2O、CO、NO等不是酸性氧化物。
过氧化物:
常见的过氧化物有过氧化氢(H2O2)、过氧化钠 (Na2O2)。
过氧化氢俗称双氧水,在催化剂的催化作用下能分解生成水和氧气,常用于实验室制取氧气。过氧化氢具有极强的氧化性,可用作杀菌剂,漂白剂。
过氧化钠能与二氧化碳反应:2Na2O2+2CO2== 2Na2CO3+O2,根据该性质,可将过氧化钠用在坑道、潜艇或宁宙飞船等缺氧的场所,将人们呼出的CO2转换成O2,供给呼吸。
1.定义:由两种元素组成,其中一种是氧元素的化合物(即由氧元素和另一种元素组成的化合物)。
2.分类:
(1)根据组成分类:
金属氧化物,如Na2O,CuO等
非金属氧化物,如CO2,NO等
(2)根据性质分类:
①酸性氧化物
能和碱反应生成盐和水的氧化物如CO2,SO3等
②碱性氧化物
能和酸反应生成盐和水的氧化物如CaO、Fe2O3等
③两性氧化物(初中不作要求)
④不成盐氧化物
不能直接反应生成盐的氧化物如CO,NO等
金属氧化物性质小结:
1.与水反应生成碱(可溶性金属氧化物)
Na2O+H2O==2NaOH
CaO+H2O==Ca(OH)2
2.与强酸反应
CaO+2HCI==CaCl2+H2O
Fe2O3+6HCl==2FeCl3+3H2O
Fe2O3+3H2SO4==Fe2(SO)3+3H2O
CuO+2HCl==CuCl2+H2O
CuO+H2SO4==CuSO4+H2O
3.与H2、CO或C反应
CuO+H2==Cu+H2O
2CuO+C==2Cu+CO2↑
CuO+CO==Cu+CO2
Fe2O3+3H2==2Fe+3H2O
2Fe2O3+3C==4Fe+3CO2↑
Fe2O3+3CO==2Fe+3CO2
Fe3O4+4H2==3Fe+4H2O
Fe3O4+2C==3Fe+2CO2↑
Fe3O4+4CO==3Fe+4CO2
非金属氧化物性质小结:
1.部分非金属氧化物与水反应生成相应的酸
CO2+H2O==H2CO3
SO2+H2O==H2SO3
2.与碱反应生成盐和水
Ca(OH)2+CO2==CaCO3↓+H2O
2NaOH+CO2==Na2CO3+H2O
Ca(OH)2+SO2==CaSO3↓+H2O
2NaOH+SO2==Na2SO3+H2O
易错点:
①酸性氧化物多数是非金属氧化物,但也可能是金属氧化物(如Mn2O7);碱性氧化物肯定是金属氧化物。
②非金属氧化物一般都是酸性氧化物,但H2O、CO、NO等不是酸性氧化物。
过氧化物:
常见的过氧化物有过氧化氢(H2O2)、过氧化钠 (Na2O2)。
过氧化氢俗称双氧水,在催化剂的催化作用下能分解生成水和氧气,常用于实验室制取氧气。过氧化氢具有极强的氧化性,可用作杀菌剂,漂白剂。
过氧化钠能与二氧化碳反应:2Na2O2+2CO2== 2Na2CO3+O2,根据该性质,可将过氧化钠用在坑道、潜艇或宁宙飞船等缺氧的场所,将人们呼出的CO2转换成O2,供给呼吸。
溶液的酸碱度及表示方法
1. 溶液的酸碱性:溶液呈酸性、碱性或中性,通常用指示剂来测定。
2. 溶液的酸碱度:指溶液酸碱性的强弱程度,即酸碱度是定量表示溶液酸碱性强弱的一种方法.溶液的酸碱度通常用pH表示。
3. pH的范围:0—14
溶液酸碱度和pH值的关系
| 溶液的pH值 | 溶液的酸碱度 |
| <7 | 酸性溶液(pH越小,酸性越强) |
| =7 | 中性溶液 |
| >7 | 碱性溶液(pH越大,碱性越大) |
(2)粗略测定溶液的酸碱度常用pH试纸。
pH的测定方法:
测定溶液pH通常用pH试纸和pH计。其中用pH试纸测定溶液pH的具体操作为:测定时,将pH试纸放在表面皿上,用干净的玻璃棒蘸取被测溶液并滴在pH试纸上,半分钟后把试纸显示的颜色与标准比色卡对照,读出溶液的pH,简记为:“一放、二蘸、三滴、四比”。
改变溶液pH的方法:
溶液的pH实质是溶液中H+浓度或OH-浓度大小的外在表现。改变溶液中H+浓度或OH-浓度,溶液的pH就会发生改变。
方法一加水:只能改变溶液的酸碱度,不能改变溶液的酸碱性,即溶液的pH只能无限地接近于7。
①向酸性溶液中加水,pH由小变大并接近7,但不会等于7,更不会大于7(如下图所示)。
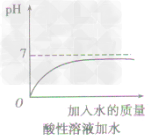
②向碱性溶液中加水,pH由大变小并接近于7,但不会等于7,更不会小于7(如下图所示)。

方法二加酸碱性相同,pH不同的溶液:原溶液酸碱性不会发生变化,但混合后溶液的pH介于两种溶液之间:
方法三加酸碱性相反的溶液:混合后发生中和反应,溶液的pH可能等于7,若加入的溶液过量,原溶液的酸碱性就会与原来相反(如下图所示)。

pH值测定时的注意事项:
①不能直接把pH试纸浸入待测的溶液中,以免带入杂质,同时还可能溶解pH试纸上的一部分指示剂,致使比色时产生较大误差。
②不能先用水将pH试纸润湿再进行测定。因为将待测溶液滴到用水润湿后的pH试纸上,其溶质质量分数将变小。
③用pH试纸测得溶液的pH一般为整数。
了解溶液的酸碱度的重要意义:
①化工生产中许多反应必须在一定pH溶液里才能进行;
②在农业生产中.农作物一般适宜在pH为7或接近于7的土壤中生长;
③测定雨水的pH(因溶解有二氧化碳,正常雨水的pH约为5.6,酸雨的pH小于5.6),可以了解空气的污染情况;
④测定人体内或排出的液体的pH,可以了解人体的健康状况。
身边一些物质的pH:

发现相似题
与“下列说法不正确的是( )A.铵态氮肥一定不能与碱同时施用B....”考查相似的试题有:
- 化学就在我们身边。回答下列问题:(1)吃蔬菜能补充人体需要的___________(填“维生素”或“油脂”)。(2)甲醛(HCHO)是室内...
- 张伟家的小麦生长迟缓,农技员判断是缺磷,应施用的肥料是( )A.KClB.KNO3C.NH4ClD.Ca(H2PO4)2
- 下列叙述中正确的是( )A.催化剂在化学反应前后质量和性质都没有改变B.不同元素的原子其核电荷数一定不同C.原子是构成物...
- 英国化学家道尔顿在他的著作《化学哲学新体系》中提出了下列有关物质构成的观点:“一切物质都是由大量的. 极其微小的粒子(原...
- 在①分子、②原子、③质子、④中子、⑤电子、 ⑥离子;这些微粒中,(1)物质的微粒有 ; (2)显示电中性的微粒有 ;(3)一定带负...
- 下列物质中属于氧化物的是[ ]A.O2B.KMnO4C.H2SO4D.MgO
- ①红磷,②高锰酸钾,③空气,④二氧化硫,⑤冰水,⑥氮气,⑦铝箔,属于混合物的是______,属于单质的是______,属于化合物的是____...
- 油炸食物不宜多吃,因为食物长时间煎炸后会产生微量的丙烯醛(化学式为C3H4O)等有毒物质,损害人体健康。下列有关丙烯醛的说法...
- 甲物质是初中化学中的常见物质,请根据下列叙述回答问题:(1)若甲物质在常温下是液态,可以做一些溶液的溶剂,其75%的溶液...
- 能确定某一物质一定是酸的依据是( )A.某水溶液能够导电B.能跟碱反应生成盐和水C.在水溶液中能离解成氢离子和酸根离子D....