本试题 “将下列四个化学实验的实验目的填写在横线上,并回答相关问题。(1) (2)在实验A中使用的计量仪器是________(填仪器的名称,下同)。 在上述四个实验中有三个实...” 主要考查您对空气中氧气含量的测定
二氧化碳的性质实验
验证质量守恒定律
验证分子特点的实验
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 空气中氧气含量的测定
- 二氧化碳的性质实验
- 验证质量守恒定律
- 验证分子特点的实验
空气中氧气含量的测定实验是初中化学的一个重要实验,同时也是历年各地中考命题的热点。近年来在课本实验的基础上进行拓展、创新,旨在考查同学们的实验探究能力及创新思维能力已成为中考命题的趋势。
空气中氧气含量的测定实验:
| 原理 | 利用红磷在空气中燃烧,将瓶内氧气消耗掉,生成五氧化二磷固体,使空气内压强减少,在大气压作用下,进入容器内水的体积即为减少的氧气的体积。4P + 5O2 2P2O5 2P2O5 |
| 装置 | 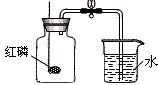 |
| 步骤 | ①连接装置,检查装置气密性 ②把集气瓶的容积分成5等份,做好记号。 ③用止水夹夹紧胶管。 ④在燃烧匙内放入过量的红磷。 ⑤点燃燃烧匙中的红磷,立即伸入集气瓶中,把塞子塞紧 ⑥待红磷熄灭并冷却后,打开止水阀 |
| 现象 | ①集气瓶中有大量的白烟生成,并放出热量 ②打开止水夹,烧杯中的水倒流到集气瓶中,并上升到约1/5处 |
| 结论 | 空气中氧气的体积分数约为1/5。 |
实验中的注意事项:
1.测定空气中氧气的体积分数时,所用物质应满足的条件:
①此物质能够在空气中中燃烧,不能用铁丝代替,铁丝在空气中不能燃烧
②此物质在空气中燃烧的时只能消耗氧气,不能消耗其他气体。不能选用镁代替红磷,因为镁不仅与空气中的氧气反应,还和二氧化碳反应。
③此物质在空气中燃烧时只能生成固体,而不能生成气体,一般不用木炭,硫代替红磷。
2.实验失败与成功的原因:
①装置不漏气是本实验成功的关键,所以实验前应检查装置的气密性。如果气密性不好,外界空气会进入容器,使测定结果低于1/5。
②实验中红磷要过量,以消耗容器内全部氧气,否则会使测定结果低于1/5.
③实验完毕,待容器冷却至室温后,再打开止水夹,观察进水的体积,避免因温度高,气体膨胀,使测定结果低于1/5.
空气中氧气含量测定实验的改进:
1.测定原理:
(1)红磷(白磷)在密闭的容器中燃烧,消耗氧气,生成白色固体五氧化二磷。密闭容器内压强减小,大气压将水压入容器,通过测定容器中的水的量测定氧气在空气中的含量。
(2)利用金属与氧气反应,消耗密闭容器中的氧气使密闭容器内压强减小,在大气压的作用下,推动刻度器上的活塞移动,测出氧气体积。
2.装置
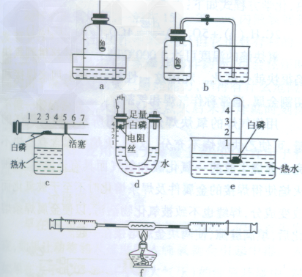
3.实验现象
(1)红磷(白磷)燃烧,产生大量白烟
(2)a中睡眠上升约占钟罩内空气体积的1/5
b中进入集气瓶中水的体积约占集气瓶液面以上容积的1/5
c中活塞移动到4处
d中U形管左侧液面上升至刻度1处
e中试管中液面上升至刻度1处
f中右侧的活塞会左移
4.结论
空气中氧气体积约占空气总体积的1/5
5.注意事项
(1)实验中红磷要过量,以消耗容器内全部氧气,否则会使测定结果低于1/5.
(2)装置不漏气是本实验成功的关键,所以实验前应检查装置的气密性。如果气密性不好,外界空气会进入容器,使测定结果低于1/5。
(3)不能用硫、木炭、铁丝等代替红磷(白磷)。因为硫或木炭燃烧后产生的气体会弥补反应所消耗的氧气,导致测得的体积不准确,而细铁丝在空气中难以燃烧,氧气体积几乎不变,因此密闭空气内水面不上升。
(4)导气管要夹紧,燃烧匙放入集气瓶时要迅速,防止空气受热膨胀,从导气管或集气瓶逸出,导致进入水的体积增多,使实验结果偏高。
探究二氧化碳的三个性质实验:
1.证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
2.二氧化碳溶于水显酸性
3.二氧化碳能溶于水
二氧化碳性质探究实验:
1.证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
(1)装置: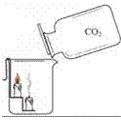
(2)现象:蜡烛由低到高依次熄灭
结论:证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
2.二氧化碳溶于水显酸性
(1)装置:
(2)现象:1和4实验中的白花变红,2和3白花不变色
(3)结论:二氧化碳不能使紫色石蕊试液变红,二氧化碳的水溶液能使紫色石蕊试液变红。
(或二氧化碳溶于水显酸性)
3.二氧化碳能溶于水
(1)装置: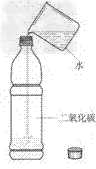
(2)现象:塑料瓶变瘪
(3)结论:二氧化碳能溶于水。
1.证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
2.二氧化碳溶于水显酸性
3.二氧化碳能溶于水
二氧化碳性质探究实验:
1.证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
(1)装置:

(2)现象:蜡烛由低到高依次熄灭
结论:证明二氧化碳的密度比空气的大;二氧化碳既不燃烧也不支持燃烧
2.二氧化碳溶于水显酸性
(1)装置:

(2)现象:1和4实验中的白花变红,2和3白花不变色
(3)结论:二氧化碳不能使紫色石蕊试液变红,二氧化碳的水溶液能使紫色石蕊试液变红。
(或二氧化碳溶于水显酸性)
3.二氧化碳能溶于水
(1)装置:

(2)现象:塑料瓶变瘪
(3)结论:二氧化碳能溶于水。
验证质量守恒定律:
通过研究体系体积的变化对探究质量守恒定律的影响,增强学生对质量守恒定律的理解,从而养成实事求是、勇于探索的科学态度。
质量守值定律的实验探究:
(1)实验装置
①无气态物质参加或生成的反应可在敞口装置中进行,如Fe+CuSO4==FeSO4+Cu
②有气态物质参加或生成的反应,应在密闭容器中进行,如白磷燃烧,NaOH与CO2反应,Zn与稀硫酸反应等。
③为确保实验成功,有时在装置上系一个气球来保证装置的密闭。如白磷燃烧实验,但也要考虑气球最终不能恢复原状,则装置在空气中受到的浮力会改变,装置对天平托盘的压力会改变,影响对质量守恒定律的探究。
(2)实验方案及结论
通过研究体系体积的变化对探究质量守恒定律的影响,增强学生对质量守恒定律的理解,从而养成实事求是、勇于探索的科学态度。
质量守值定律的实验探究:
(1)实验装置
①无气态物质参加或生成的反应可在敞口装置中进行,如Fe+CuSO4==FeSO4+Cu
②有气态物质参加或生成的反应,应在密闭容器中进行,如白磷燃烧,NaOH与CO2反应,Zn与稀硫酸反应等。
③为确保实验成功,有时在装置上系一个气球来保证装置的密闭。如白磷燃烧实验,但也要考虑气球最终不能恢复原状,则装置在空气中受到的浮力会改变,装置对天平托盘的压力会改变,影响对质量守恒定律的探究。
(2)实验方案及结论
| 方案一 | 方案二 | |
| 实验现象 | 白磷燃烧,产生大量白烟,放出热量,天平平衡 | 铁钉表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色,天平平衡 |
| 反应前总质量 | m1 | m1 |
| 反应后总质量 | m2 | m2 |
| 反应前后总质量的关系 | m1=m2 | m1=m2 |
| 分析 | 磷+氧气 五氧化二磷 五氧化二磷容器密闭,物质没有进入或散失 |
铁+硫酸铜→铜+硫酸亚铁 反应无气体参加,无气体生成,没有物质从烧杯中散失 |
| 结论 | 分析比较两个方案的实验结果,可以发现反应前后物质的质量总和不变 | |
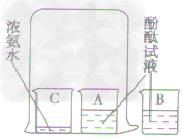
验证分子特点的实验:
通过对分子特点的探究,可以让学生直观的感受到微观世界里分子构成物质的特点。
探究分子运动的实验:
| 实验装置 |
| ||
| 实验步骤 | 步骤1 | 步骤2 | 步骤3 |
| 在盛有约40ml 蒸馏水的烧杯中加 如5一6滴酚酞试液,搅拌均匀, 观察现象 |
取步骤I得到的溶液,置于 试管中,再向其中滴加浓 氨水,观察现象 |
将烧杯中的溶液分别倒入 A、B两个小烧杯中,另取 一个小烧杯C,加入约5ml 浓 氨水。用一个大烧杯罩住 A,C两个小烧杯,烧杯B 置于大烧杯外 | |
| 实验现象 | 无明显现象 | 溶液由无色变成红色 | 烧杯A中液体由无色变为红色,烧杯B中无变化 |
| 实验解释 | 烧杯中的浓氨水挥发出氛分子,氨分了进人烧杯A中,使溶液变成红色.而烧杯B中没有氨分子进入 | ||
探究分子间有间隙的实验:
| 实验原理 | 分子之间存在间隙且分子总是做不停地无规则运动。将水和酒精充满容量瓶,混合均匀后,若液面发生下降,则可验证分子间存在间隙。 | ||
| 实验用品 | 100ml 容量瓶 1 只、 100ml 烧杯 2 只、餐纸、保鲜膜、棉线一根、无水酒精、 纯净水、品红溶液。 | ||
| 实验装置 | 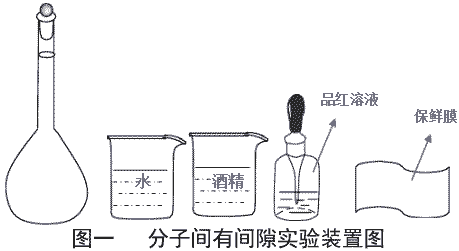 | ||
| 实验步骤 | 实验结果 | 实验结论 | |
| 实验方案一 | (1) 打开容量瓶,用小烧杯移取 70ml 已滴加了品红溶液的水于容量瓶中。 (2) 用小烧杯移取酒精于容量瓶中直至容量瓶满。 (3) 塞上容量瓶塞,有液体溢出,用餐纸擦干。倒置容量瓶几次,使液体充分混 合,观察液面下降情况。 |
液面下降 1.5cm 左右,实验现象非常明显 | 优点: (1) 酒精用量少,该实验只需耗费 30ml 左右的酒精 (2) 滴入品红溶液的水呈红色,可明显观察到在容量瓶倒置前,容量瓶中液体分 层,上层无色,下层红色。而倒置后溶液呈均匀红色。 (3) 倒置前容量瓶充满液体,排除了会有部分液体残留在容量瓶上导致的误差。 (4) 实验现象明显,混合后液面下降 1.5cm 左右 (5) 实验操作简单,实验用品少 缺点:将充满的容量瓶塞上容量瓶塞会有液体溢出,这个操作不规范。 |
| 实验方案二 | (1) 打开容量瓶,用小烧杯移取 70ml 已滴加了品红溶液的水于容量瓶中。 (2) 用小烧杯移取酒精于容量瓶中直至容量瓶满。 (3) 用保鲜膜迅速包裹容量瓶,然后将保鲜膜用细线捆紧。用手掌压住容量瓶口, 倒置容量瓶几次,使液体充分混合,观察液面下降情况。 |
液面下降 1cm 左右,实验现象非常明显。用无水硫酸铜检验容量瓶外壁, 并无液体溢出。 | 优点: (1) 酒精用量少,该实验只需耗费 30ml 左右的酒精 (2) 滴入品红溶液的水呈红色,可明显观察到在容量瓶倒置前,容量瓶中液体分 层,上层无色,下层红色。而倒置后溶液呈均匀红色。 (3) 倒置前容量瓶充满液体,排除了会有部分液体残留在容量瓶上导致的误差。 (4) 实验现象明显,混合后液面下降 1cm 左右 (5) 实验操作简单,实验用品少 (6) 方案二很好的解决了方案一的缺陷,且实验效果好。 |
发现相似题
与“将下列四个化学实验的实验目的填写在横线上,并回答相关问题...”考查相似的试题有:
- 下列是初中化学的三个实验,按要求回答问题:(1)实验C中烧杯③的作用是______.(2)上述不能达到实验目的实验是______(填...
- (1)利用如图所示装置可测定空气中氧气的含量.①实验现象,红色物质逐渐变成______.②反应的化学方程式为______.③停止加热...
- 小思实验操作考试的题目是探究金属的化学性质,内容包括:铜在空气中灼烧、锌与稀硫酸反应、铝丝与硫酸铜溶液反应。如图是他...
- (4分)比较类推、寻找规律是学习化学的有效方法。(1)氯元素常见的化合价有十7、+5、+3、+1、-1,下面五种物质都是含氯...
- 科学研究小组的同学在用一定浓度的硫酸溶液处理废金属材料(主要是生铁、镀锌铁皮)时,溶液发烫并闻到了刺激性气味,这种反...
- 探究活动一:在室温条件下进行如图所示实验。已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支...
- 叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究.应用研究:(1)汽车经撞击后,30毫秒内引发NaN3,...
- “凤凰”号火星探测器发回的照片上显示,火星上确有液态水存在。下列微粒模型示意图可表示构成水的微粒的是A B C D
- 下图是探究分子运动的实验装置图。向盛有约40 mL蒸馏水的烧杯中加入5~6滴酚酞溶液,搅拌均匀观察溶液的颜色是____ ;将烧杯中...
- 下列各组物质中,都是由分子构成的是( )A.水、氢气B.铁、氧气C.二氧化锰、铝D.氯化钠、水