本试题 “下列叙述中正确的是( )A.SiO2和CO2都是共价化合物B.根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质C.2g氦气所含原子数为NAD.CH4的...” 主要考查您对摩尔质量
共价键
强电解质、弱电解质
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 摩尔质量
- 共价键
- 强电解质、弱电解质
摩尔质量:
定义:单位物质的量的物质所具有的质量
符号:M
单位:g/mol(g·mol-1)
计算公式:摩尔质量(M)=质量(m)/物质的量(n)
摩尔质量、相对分子质量、1mol物质的质量三者的区别和联系:
1mol物质的质量在数值上和摩尔质量相同,二者的区别在于单位不一样,质量的单位是千克(kg),而摩尔质量的单位是g/mol。相对分子质量与摩尔质量单位不同,但在数值上二者相等。
平均摩尔质量的计算方法:
- 已知混合物质的总质量m(混)和总物质的量n(混):M =m(混)/n(混)
- 已知同温同压下混合气体的密度ρ(混)是一种简单气体A的密度ρ(A)的倍数d(也叫相对密度)d= ρ(混)/ ρ(A),则M混= ρ混M混/ ρ(A)
- 在溶液中,M=1000ρw%/c(ρ指溶液的密度,w%指溶液中溶质的质量分数,c表示溶液的浓度)
- 已知某状况下的混合气体的密度M=ρVm(ρ表示气体的密度,Vm表示在该状况下的气体的摩尔体积)
- 已知混合物各成分的摩尔质量和其在混合体系内的物质的量分数或体积分数M=M1×n1%+M2×n2% =M1×V1%+M2×V2%
共价键:
1.本质原子之间形成共用电子对(或电子云重叠),使得电子出现在核间的概率增大。
2.特征
具有方向性与饱和性。
(1)共价键的饱和性一个原子中的一个未成对电子与另一个原子中的一个未成对电子配对成键后,一般来说就不能再与其他原子的未成对电子配对成键了,即每个原子所能形成共价键的总数或以单键连接的原子数目是一定的,这称为共价键的饱和性。
例如,氯原子中只有一个未成对电子,所以两个氯原子之间可以形成一个共价键,结合成氯分子,表示为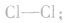 氮原子中有三个未成对电子,两个氮原子之间能够以共价三键结合成氮分子,表示为
氮原子中有三个未成对电子,两个氮原子之间能够以共价三键结合成氮分子,表示为 一个氮原子也可与_二个氢原子以三个共价键结合成氨分子,表示为
一个氮原子也可与_二个氢原子以三个共价键结合成氨分子,表示为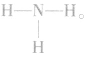
(2)共价键的方向性
共价键将尽可能沿着电子出现概率最大的方向形成,这就是共价键的方向性。除s轨道是球形对称外,其他原子轨道都具有一定的空间分布。在形成共价键时,原子轨道重叠得越多,电子在核间出现的概率越大,所形成的共价键就越牢固。
例如,硫原子的价电子排布是 有两个未成对电子,如果它们分布在互相垂直的
有两个未成对电子,如果它们分布在互相垂直的 轨道中,那么当硫原子和氢原子结合生成硫化氢分子时,一个氢原子的1s轨道上的电子能与硫原子的
轨道中,那么当硫原子和氢原子结合生成硫化氢分子时,一个氢原子的1s轨道上的电子能与硫原子的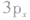 轨道上的电子配对成键,另一个氢原子的1s轨道上的电子只能与硫原子的
轨道上的电子配对成键,另一个氢原子的1s轨道上的电子只能与硫原子的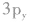 轨道上的电子配对成键。
轨道上的电子配对成键。
说明:
①共价键的饱和性决定着各种原子形成分子时相互结合的数量关系。如一个氢分子只能由两个氢原子构成,一个水分子只能由两个氢原子和一个氧原子构成。
②共价键的方向性决定着分子的空间构型。
3.分类
(1)按成键原子是否相同或共用电子对是否偏移分 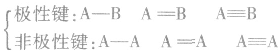
(2)按成键方式分

(3)按共用电子对数分
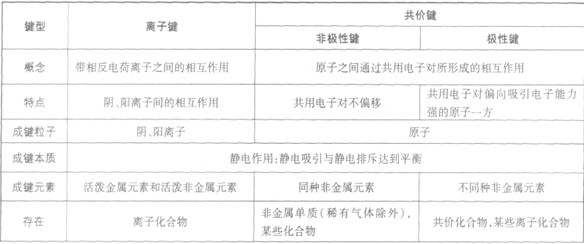
离子键和共价键:

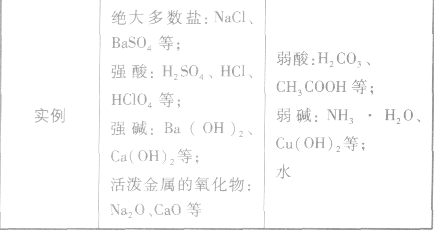
在水溶液里或熔融状态下,能全部电离的化合物。包括:强酸、强碱、大多数盐、活泼金属氧化物等;完全电离、不可逆、不存在电离平衡;电离方程式用“=”表示。
弱电解质:
在水溶液里或熔融状态下,不能全部电离的化合物。包括:弱酸、弱碱、少数盐等;部分电离、可逆、存在电离平衡,电离方程式用“
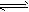 ”表示。
”表示。 强电解质和弱电解质的比较:
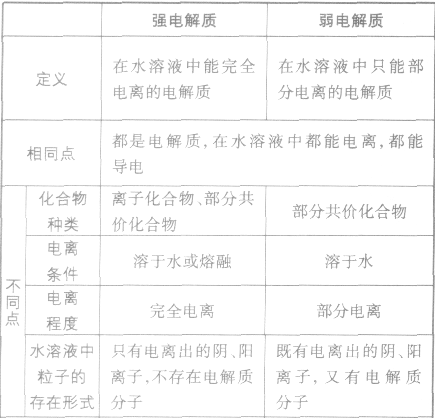
强弱电解质的判断依据:
1.在相同浓度、相同温度下,与强电解质做导电性对比实验.
2.浓度与pH的关系。如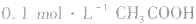 溶液的pH>1,则证明
溶液的pH>1,则证明 是弱电解质。
是弱电解质。
3.测定对应盐溶液的酸碱性。如 溶液呈碱性,则证明醋酸是弱电解质。
溶液呈碱性,则证明醋酸是弱电解质。
4.稀释前后的pH变化与稀释倍数的关系。例如,将pH=2的酸溶液稀释1000倍,若pH<5,则证明该酸为弱电解质;若pH=5,则证明该酸为强电解质。
5.采用实验证明电离平衡。如向醋酸溶液中滴人石蕊试液,溶液变红,再加入醋酸钠晶体,颜色变浅。
与“下列叙述中正确的是( )A.SiO2和CO2都是共价化合物B.根据...”考查相似的试题有:
- 有一空瓶的质量为W1g,向该瓶充入氧气后的质量为W2g,在相同条件下充入某一单质气体,其质量为W3g,则此单质气体的摩尔质量为...
- 根据所学知识,完成下列各题:(1)在标准状况下,气体A的密度为3.17g•L-1,则气体A的摩尔质量为______;(2)MgSO4和Al2(SO...
- A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物;B与Z的最外...
- 下列各组物质熔化或气化时,所克服的粒子间作用属于同种类型的是[ ]A.C60和SiO2熔化B.Mg和S熔化C.氯酸钾和蔗糖熔化D.碘和...
- 对于HCl、H2SO4、NaOH、NaCl、Ne、金刚石、N2,回答下列问题:(1)不存在化学键的是___________。(2)属于共价化合物的是__...
- 下列物质溶于水时会破坏水的电离平衡,且属于电解质的是( )A.氯气B.醋酸钠C.碘化钾D.二氧化碳
- 下列物质中,能导电的且属于电解质的是A.铜B.食盐水C.酒精D.熔融的氯化钾
- 下列物质属于弱电解质的是( )A.金属钠B.硫酸C.次氯酸D.氯酸钾
- 能表明氨水是弱电解质的叙述是[ ]A.NH3·H2O的导电性比NaOH溶液弱得多B.0.1ml/L的NH3·H2O,是PH小于12,大于7C.NH4Cl的水...
- 类比是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观事实。下列各种类比推测的说法中正...