本试题 “下列有关说法正确的是[ ]A.电解饱和食盐水可制得金属钠B.铜锌原电池工作时电子沿外电路从铜电极流向锌电极C.铅蓄电池在放电过程中负极质量减小,正极质量...” 主要考查您对原电池原理
电解饱和氯化钠溶液
金属的化学腐蚀
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原电池原理
- 电解饱和氯化钠溶液
- 金属的化学腐蚀
原电池:
1.定义:将化学能转化为电能的装置。
2.工作原理:
以铜-锌原电池为例
(1)装置图:
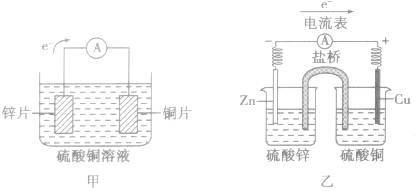
(2)原理图:
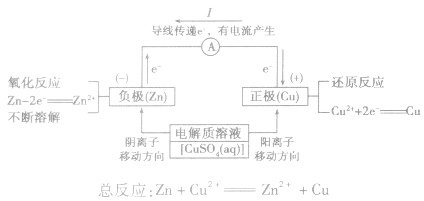
3.实质:化学能转化为电能。
4.构成前提:能自发地发生氧化还原反应。
5.电极反应:
负极:失去电子;氧化反应;流出电子
正极:得到电子;氧化反应;流入电子
6.原电池正负极判断的方法:
①由组成原电池的两级材料判断,一般是活泼金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②根据电流方向或电子流动方向判断,电流是由正极流向负极,电子流动方向是由负极流向正极。
③根据原电池里电解质溶液内离子的定向移动方向,在原电池的电解质溶液中,阳离子移向正极,阴离子移向负极。
④根据原电池两级发生的变化来判断,原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
⑤X极增重或减重:X极质量增加,说明溶液中的阳离子在X极(正极)放电,反之,X极质量减少,说明X极金属溶解,X极为负极。
⑥X极有气泡冒出:发生可析出氢气的反应,说明X极为正极。
⑦X极负极pH变化:析氢或吸氧的电极发生反应后,均能使该电极附近电解质溶液的pH增大,X极附近的pH增大,说明X极为正极。
1.定义:将化学能转化为电能的装置。
2.工作原理:
以铜-锌原电池为例

(1)装置图:

(2)原理图:

3.实质:化学能转化为电能。
4.构成前提:能自发地发生氧化还原反应。
5.电极反应:
负极:失去电子;氧化反应;流出电子
正极:得到电子;氧化反应;流入电子
6.原电池正负极判断的方法:
①由组成原电池的两级材料判断,一般是活泼金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②根据电流方向或电子流动方向判断,电流是由正极流向负极,电子流动方向是由负极流向正极。
③根据原电池里电解质溶液内离子的定向移动方向,在原电池的电解质溶液中,阳离子移向正极,阴离子移向负极。
④根据原电池两级发生的变化来判断,原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
⑤X极增重或减重:X极质量增加,说明溶液中的阳离子在X极(正极)放电,反之,X极质量减少,说明X极金属溶解,X极为负极。
⑥X极有气泡冒出:发生可析出氢气的反应,说明X极为正极。
⑦X极负极pH变化:析氢或吸氧的电极发生反应后,均能使该电极附近电解质溶液的pH增大,X极附近的pH增大,说明X极为正极。
原电池中的电荷流动:
在外电路(电解质溶液以外),电子(负电荷)由负极经导线(包括电流表和其他用电器)流向正极,使负极呈正电性趋势、正极呈负电性趋势。在内电路(电解质溶液中),阳离子(带正电荷)向正极移动,阴离子 (带负电荷)向负极移动。这样形成了电荷持续定向流动,电性趋向平衡的闭合电路。
电解饱和氯化钠溶液:
在小烧杯(或U型管)里装入饱和食盐水,滴入几滴酚酞试液。用导线把碳棒、电池、电流表和铁钉相连(如图)。接通直流电源后,注意观察电流表的指针是否偏转,以及小烧杯内发生的现象,并用湿润的碘化钾淀粉试纸检验阳极放出的气体。
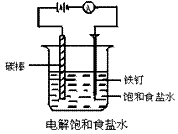
注:粗铁钉要与直流电源的阴极相连,碳棒与阳极相连。
用玻璃棒沾湿润的KI淀粉试纸检验阳极气体。
(1)饱和食盐水电解时,电流表指针发生偏转,阴、阳极均有气体放出,阳极气体有刺激性气味,并能使湿润的KI淀粉试纸变蓝,且阴极区溶液变红。
(2) 阳极:2Cl--2e-==Cl2↑
阴极:2H++2e-==H2↑(或2H2O+2e-==2OH-+H2↑)
总反应式:2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(3)阴极区溶液变红的原因:这是由于饱和食盐水中,水所电离出的H+在阴极放电,破坏了水的电离平衡
(H2O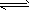 H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。
H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。
(4)例用电解饱和食盐水溶液可制取氢气、氯气和烧碱。
在小烧杯(或U型管)里装入饱和食盐水,滴入几滴酚酞试液。用导线把碳棒、电池、电流表和铁钉相连(如图)。接通直流电源后,注意观察电流表的指针是否偏转,以及小烧杯内发生的现象,并用湿润的碘化钾淀粉试纸检验阳极放出的气体。

注:粗铁钉要与直流电源的阴极相连,碳棒与阳极相连。
用玻璃棒沾湿润的KI淀粉试纸检验阳极气体。
(1)饱和食盐水电解时,电流表指针发生偏转,阴、阳极均有气体放出,阳极气体有刺激性气味,并能使湿润的KI淀粉试纸变蓝,且阴极区溶液变红。
(2) 阳极:2Cl--2e-==Cl2↑
阴极:2H++2e-==H2↑(或2H2O+2e-==2OH-+H2↑)
总反应式:2NaCl+2H2O
 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑ (3)阴极区溶液变红的原因:这是由于饱和食盐水中,水所电离出的H+在阴极放电,破坏了水的电离平衡
(H2O
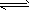 H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。
H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。 (4)例用电解饱和食盐水溶液可制取氢气、氯气和烧碱。
金属的化学腐蚀:
1、定义:金属跟接触到的干燥气体(如O2、Cl2、SO2 等)或非电解质液体 (如石油)等直接发生化学反应而引起的腐蚀
2、条件:金属跟氧化剂直接接触
3、现象:无电流产生
4、本质:金属被氧化而腐蚀
5、反应速率:v(电化学腐蚀)>v(化学腐蚀)
发现相似题
与“下列有关说法正确的是[ ]A.电解饱和食盐水可制得金属钠B.铜...”考查相似的试题有:
- 下列有关原电池和电解池的叙述中正确的是A.钢铁腐蚀时,铁有时候作负极有时候作正极B.将铜片锌片用导线连接插入稀硫酸中,...
- 将0.23 mol SO2和0.11 mol O2放入容积为1 L的密闭容器中,发生反应2SO2+O22SO3,在一定温度下,反应达到平衡,得到0.12 mol ...
- 请判断下列原电池的正负极:___________________________________________________
- 如图所示,在不同的电解质溶液中可以组成不同的电池。(1)①当电解质溶液为稀硫酸时,Fe电极是 (填“正”或“负”)极,其电极反应式...
- (2014届江西省八校高三下学期联考理综化学试卷)瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)的传感器煤矿巷道中...
- 某原电池反应的离子方程式为Fe+2H+=Fe2++H2↑,则下列说法正确的是[ ]A.HNO3为电解质溶液B.锌为原电池正极C.铁极质量不...
- 下列有关原电池的叙述中正确的是 ( )A.把电能转变为化学能的装置B.活泼金属做正极,不活泼金属或非金属做负极C.外电路中...
- (7分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能...
- 电解NaCl溶液的装置如图所示,下列说法不正确的是[ ]A.铁电极上的电极反应式为Fe-2e-==Fe2+B.溶液中Na+由石墨电极向铁电极...
- 为了保护地下钢管不受腐蚀,可使它与( )A.直流电源正极相连B.铜板相连C.锌板相连D.直流电源负极相连