本试题 “常温下,0.1mol/L某一元酸(HA)溶液中,下列叙述正确是[ ]A.该一元酸溶液的pH=1B.该溶液中HA的电离度为1%C.该溶液中水的离子积常数为1×10-22D.若加水稀...” 主要考查您对弱电解质的电离
水的离子积常数
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 弱电解质的电离
- 水的离子积常数
定义:
在一定温度、浓度的条件下,弱电解质在溶液中电离成离子的速率与离子结合成分子的速率相等时,电离过程就到了电离平衡状态,叫弱电解质的电离平衡。

电离平衡的特征:
(1)等:
(2)动: 的动态平衡
的动态平衡
(3)定:条件一定,分子与离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。
在一定温度、浓度的条件下,弱电解质在溶液中电离成离子的速率与离子结合成分子的速率相等时,电离过程就到了电离平衡状态,叫弱电解质的电离平衡。

电离平衡的特征:
(1)等:

(2)动:
 的动态平衡
的动态平衡(3)定:条件一定,分子与离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。
水的电离:
水是一种极弱的电解质,它能微弱地电离:
实验测得:25℃时,1L纯水中只有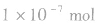 的水分子发生电离,故25℃时纯水中
的水分子发生电离,故25℃时纯水中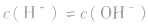

水的离子积:
在一定温度下,水电离出的c(H+)与c(OH-)的乘积是一个常数,称为水的离子积常数,简称水的离子积,用符号 表示,即
表示,即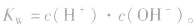
(1)在一定温度下,水的离子积都是一个常数,在25℃时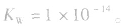
(2)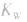 随温度的变化而变化,温度升高,
随温度的变化而变化,温度升高,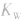 增大。
增大。
(3)水的离子积常数揭示了在任何水溶液中均存在水的电离平衡,都有 存在。在酸性或碱性的稀溶液中,当温度为25℃时,
存在。在酸性或碱性的稀溶液中,当温度为25℃时,
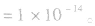
(4)在酸或碱的稀溶液中,由水电离出的c(H+)和c(OH-)总相等.即 如25℃时
如25℃时 或NaOH溶液中,
或NaOH溶液中,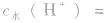
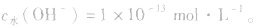
溶液中c(H+)或c(OH-)的计算:
常温下,稀溶液中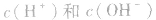 的乘积总是
的乘积总是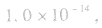 知道
知道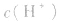 就可以计算出
就可以计算出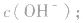 反之亦然
反之亦然
1.酸溶液
当在水中加入酸后,将使水的电离平衡向左移动 (抑制水的电离)。在酸的水溶液中,H+主要由酸电离产生,即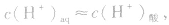 而OH-是由水电离产生的:
而OH-是由水电离产生的: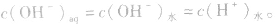
2.碱溶液
同理,在碱的水溶液中,OH-主要由碱电离产生,即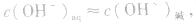 而H+是由水电离产生的:
而H+是由水电离产生的: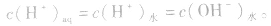
3.盐溶液
在盐的水溶液中,H+和OH-全部来自水的电离,且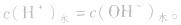
(1)若单一水解的盐的水溶液呈酸性,c(H+)> c(OH-),即弱碱阳离子水解


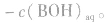
(2)若单一水解的盐的水溶液呈碱性,c(OH一)> c(H+),即弱酸阴离子水解
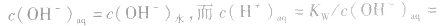
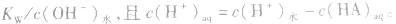
说明:由以上分析可以看出,在常温下(25℃):
酸(或碱)的溶液中,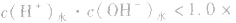
 发生水解的盐溶液中
发生水解的盐溶液中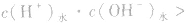
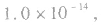 但
但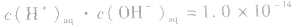 总成立。
总成立。
发现相似题
与“常温下,0.1mol/L某一元酸(HA)溶液中,下列叙述正确是[ ]A...”考查相似的试题有:
- 对于常温下pH=3的乙酸溶液,下列说法正确的是( )A.C(H+)=c(CH3COO-)+c(OH-)B.加水稀释到原体积的10倍后溶液pH变为4...
- 25°C时某些弱酸的电离平衡常数如下表,下列说法正确的是( )化学式CH3COOHHClOH2CO3KaKa=1.8×10-5Ka=3.0×10-8Ka1=4.1×10-7Ka2=...
- 0.1mol·L-1HF溶液的pH=2,则该溶液中有关浓度关系式不正确的是( )A.c(H+)>c(F-)B.c(H+)>c(HF)C.c(OH-)<c(HF)D...
- 下列事实能证明HNO2是弱电解质的是( )A.用HNO2溶液做导电性试验灯光较暗B.HNO2是共价化合物C.常温下,0.1 mol/L HNO2溶...
- 石油开采过程中广泛采用CO2驱油,即向油井注入CO2,当CO2到达储层后,CO2溶解于水中生成碳酸溶液腐蚀岩石,使岩石的渗透率得...
- 甲酸是一种一元有机酸。下列性质可以证明它是弱电解质的是[ ]A.甲酸能与水以任意比互溶B.1 mol/L甲酸溶液的pH约为2C.10 mL...
- 室温下,下列关于pH均为9、体积均为10ml的NaOH溶液和CH3COONa溶液比较的说法,正确的是( )A.两种溶液中的c(Na+)相等B....
- 用标准氢氧化钠溶液滴定未知浓度的盐酸,用酚酞作指示剂,下列操作会导致实验结果偏高的是A.配制标准溶液的氢氧化钠中混有碳...
- 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂。请填写下列空白:(1)用标准...
- 用稀盐酸预处理强酸型阳离子交换树脂,使之变为HR,再用蒸馏水洗涤至中性,然后用该树脂软化100mL含0.001molMg2+的中性溶液,...