本试题 “根据你所学的知识,判断下列推断正确的是( )A.若X是金属晶体,Y是分子晶体,则熔点高低为:X>YB.若R2-与M2+的电子层结构相同,则原子序数大小为:R>MC...” 主要考查您对氧化性、还原性强弱的比较
物质性质的研究
盐类水解的定义
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化性、还原性强弱的比较
- 物质性质的研究
- 盐类水解的定义
研究对象:
物质的物理性质、化学性质物质性质。
研究方法:
观察与问题、假设与预测、实验与事实、解释与结论、表达与交流、扩展与迁移。
盐类水解:
1.定义:在水溶液中盐电离出来的离子跟水电离出来的H+或OH-结合生成弱电解质的反应,叫做盐类水解。
2.实质:生成弱电解质,使水的电离平衡被破坏而建立新的平衡。
3.条件:盐中必须有弱酸根离子或弱碱阳离子,盐溶于水。
4.特点:可逆性,写水解离子方程式时要用“ ” 水解是吸热过程,是中和反应的逆过程。一般,水解的程度较小,写离子方程式时,不能用“↑”或“↓”符号。多元弱酸根分步水解,以第一步为主。多元弱碱阳离子一步水解。
” 水解是吸热过程,是中和反应的逆过程。一般,水解的程度较小,写离子方程式时,不能用“↑”或“↓”符号。多元弱酸根分步水解,以第一步为主。多元弱碱阳离子一步水解。
5.规律:有弱才水解,无弱不水解。谁弱谁水解,谁强显谁性。越弱越水解,都弱都水解。例如:25℃时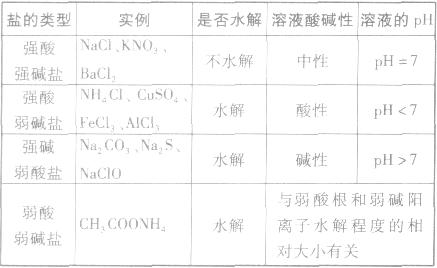
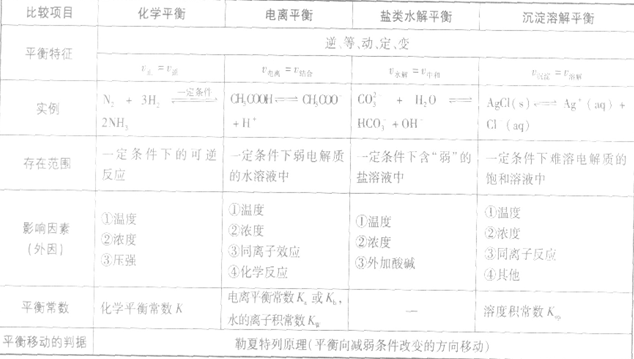
四种重要的动态平衡的比较:
发现相似题
与“根据你所学的知识,判断下列推断正确的是( )A.若X是金属晶...”考查相似的试题有:
- 回答下列有关氧化还原反应的问题:(1)在下列反应中:A.2F2+2H2O=4HF+O2↑;B.2Na+2H2O=2NaOH+H2↑;C.CaO+H2O=Ca(OH)2;...
- 三氟化氮(NF3)是无色无味的气体,它可由氨气和氟气反应得到,反应的化学方程式为:4NH3+3F2==NF3+3NH4F。下列有关NF3的叙述...
- A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C两元素的族序数之和是A元素族序数的2倍;则A、B、C分别为( )A...
- (10分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题...
- A、B、C、D、E、F、G七种元素,它们的原子序数依次增大,除G外均为前20号元素。A原子基态时p能级原子轨道上电子数等于次外能...
- 下表是部分短周期元素的原子半径及主要化合价:元素代号WRXYZQM原子半径/nm0.0370.1860.0740.0750.0770.1100.160主要化合价+1...
- 根据元素F、S、Cl在周期表中的位置,关于F、S、Cl的说法正确的是( )A.非金属性:F>S>ClB.原子半径:Cl>S>FC.稳定性...
- 则下列有关NH4Cl溶液里存在的微粒的叙述,不正确的是A.存在NH3·H2O,其结构式为B.存在NH4+,其电子式为C.存在H3O+,其结构...
- 下列说法正确的是( )A.溶液的pH值越小,其中含有的氢离子就越多B.物质的水溶液浓度越高,密度越大C.单质的化学活动性越...
- 在氯化铁溶液中存在平衡:FeCl3+3H2OFe(OH)3+3HCl △H>0。(1)加热FeCl3溶液,溶液的颜色会加深,可得到一种红褐色透明...