本试题 “请你根据不同的实验内容,回答对应的问题:(1)仪器a的名称是______.用带火星的木条检验a中的气体,观察到木条复燃,该气体是______.(2)将白色纸花用紫...” 主要考查您对电解水实验
燃烧与燃烧的条件
二氧化碳的性质
一氧化碳的性质和用途
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电解水实验
- 燃烧与燃烧的条件
- 二氧化碳的性质
- 一氧化碳的性质和用途
电解就是将两根金属或碳棒(即电极)放在要分解的物质(电解质)中,然后接上电源,使电流通过液体。化合物的阳离子移到带负电的电极(阴极),阴离子移到带正电的电极(阳极),化合物分为二极。
电解过程
用电使化合物分解的过程就叫电解过程。
水(H2O)被电解生成电解水。电流通过水(H2O)时,氢气在阴极形成,氧气则在阳极形成。带正电荷的离子向阴极移动,溶于水中的矿物质钙、镁、钾、钠……带正电荷的离子,便在阴极形成,就是我们所喝的碱性水;而带负电的离子,在阴极生成。
电解水实验:
1.实验装置图:
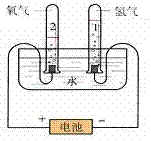
2.表达式:
水
 氢气+氧气
氢气+氧气2H2O
 2H2↑+O2↑
2H2↑+O2↑3.实验现象:
(1)通电后两电极上都有气泡产生;
(2)与电源正极相连接的一端产生的气体比连接负极一端产生的气体少,
接负极一端玻璃管中气体的体积是接正极一端玻璃管内气体体积的2倍。
4.产物检验
(1)正极一端的气体能使带火星的木条复燃,证明气体是氧气。
(2)负极一端的气体能燃烧,并看到微弱的淡蓝色火焰(或听到爆鸣声),
证明气体是氢气。
5.实验结论:
(1)水是由氢元素和氧元素组成的。
(2)1个水分子由2个氢原子和1个氧原子构成。
(3)化学变化中,分子可以再分,原子不可以再分。
6.注意事项:
(1)实验前在水中加入少量的氢氧化钠或者稀硫酸,可增强水的导电性,
加快反应速率。
(2)实验开始时产生的氧气和氢气的体积会小于1:2,是因为氢气难溶于水,
氧气不易溶于水,开始产生的氧气有一部分溶于水,实验时间越长,
其比值越接近1:2。
电解水记忆口诀:
水中通入直流电,正氧负氢会出现;氢二氧一体积比,任何时候都不变。
概念:
燃烧是指可燃物与氧气发生的一种发光放热的剧烈的氧化反应。
燃烧的三个条件:
物质具有可燃性,可燃物与氧气接触,温度达到可燃物的着火点
促进物质燃烧的方法:
(1)增大氧气的浓度
(2)增大可燃物与氧气的接触面积
对燃烧概念的理解:
通常所说的燃烧是一种可燃物与空气中的氧气发生的一种发光、发热的剧烈的氧化反应。但实际上燃烧并不一定有氧气参加,任何发光、发热的剧烈化学反应都可称之为“燃烧”。
如2Mg+CO2
 2MgO+C;2Na+Cl2
2MgO+C;2Na+Cl2 2NaCl
2NaCl燃烧与发光,放热,火焰之间的关系:
(1)燃烧与发光,放热的关系
燃烧一定发光,放热,但发光,放热的变化不一定是化学变化,因而不一定是燃烧,如原子弹,氢弹的爆炸。
(2)燃烧与火焰的关系
火焰是气体物质燃烧所特有的现象、液体物质的燃烧主要是其蒸气的燃烧,因而产生火馅。若固体物质的沸点较高.燃烧时无蒸气逸出,则无火焰,如铁勺燃烧:若固体物质的沸点较低,燃烧时有蒸气逸出,就有火馅,如钠、硫的燃烧。
(3)发光与放热的关系
化学反应瞬间放出热量较多时.就以光的形式出现,反之则不发光,因此,发光一定收热,放热不一定发光。燃烧反应是既发光又放热的反应,单一的发光或放热反应不一定是燃烧。
影响物质着火点的因素:
着火点不是同定不变的。对同体燃料来说,着火点的高低跟表面积的大小、材料的粗细、导热系数的大小有关系。颗粒越细,表而积越大.导热系数越小,着火点越低,所以块状的木材难点燃,向木材的刨花很好点燃。对于液体燃料和气体燃料来说,火焰接触它们的情况和外界压强的大小有关系,所以测定物质的着火点对外界条件有一定标准。
(1)内在因素
可燃物的性质,不同种物质燃烧的现象不同。例如,硫在空气中燃烧发出淡监色火焰,细铁丝在空气中却不能燃烧。
(2)外部因素
①与氧气的接触面积越大,燃烧越剧烈,如煤的燃烧经历了煤块→煤球→蜂窝煤的过程,蜂窝煤能使煤更充分燃烧的原因是与空气的接触面积增大;如俗语说“人要实,火要虚”。
②氧气的浓度越大,燃烧就越剧烈。如硫在空气燃烧发出淡蓝色火焰,而在氧气中燃烧发出蓝紫色火焰。可燃物在纯氧中比在空气中燃烧会更剧烈。
燃烧的利与弊
燃烧会放出入量,人类需要的大部分能量来源于化石燃料的燃烧.人类利用燃烧放出的热量,可以做饭、取暖、发电、冶烁金属等,但燃蛲也有不利的地方,燃料燃烧不充分时,不仅产生的热量少,浪费资源,而且还会产生CO等物质,污染环境
二氧化碳是空气中常见的化合物,其分子式为CO?,由两个氧原子与一个碳原子通过共价键连接而成,常温下是一种无色无味气体,密度比空气略大,能溶于水,与水反应生成碳酸。固态二氧化碳俗称干冰。二氧化碳被认为是造成温室效应的主要来源。
物理性质:
常温下,二氧化碳是一种无色无味的气体,密度比空气大,能溶于水。
固态的二氧化碳叫做干冰。
化学性质:
(1)一般情况下,二氧化碳不能燃烧,也不支持燃烧,不供给呼吸,因此当我们进入
干枯的深井,深洞或久未开启的菜窖时,应先做一个灯火实验,以防止二氧化碳浓度
过高而造成危险
(2)二氧化碳和水反应生成碳酸,使紫色石蕊试液变红:CO2 + H2O===H2CO3,
碳酸不稳定,很容易分解成水和二氧化碳,所以红色石蕊试液又变回紫色:
H2CO3===H2O + CO2↑
(3)二氧化碳和石灰水反应:Ca(OH)2 + CO2====CaCO3↓+ H2O
(4)二氧化碳可促进植物的光合作用:6CO2+6H2O
 C6H12O6+6O2
C6H12O6+6O2 一氧化碳和二氧化碳性质的比较:
|
|
|
一氧化碳 |
二氧化碳 |
|
物理性质 |
状态 |
无色,无味气体 |
无色,无味气体 |
|
密度 |
1.250g/l(略小于空气) |
1.977g/l(大于空气) | |
|
溶解性 |
1体积水中约溶解0.02体积 |
1体积中约溶解1体积 | |
|
化学性质 |
可燃性 |
有可燃性 |
一般情况下,既不能燃烧,也不能支持燃烧 |
|
还原性 |
有还原性: |
没有还原性 | |
|
跟水反应 |
不能 |
能:CO2+H2O==H2CO3 | |
|
跟澄清石灰水反应 |
不能 |
CO2+Ca(OH)2==CaCO3↓+H2O | |
|
毒性 |
有毒 |
无毒 | |
|
主要用途 |
作气体燃料,用于高炉炼铁 |
灭火,人工降雨,干冰制冷剂等,作化工原料和温室肥料 | |
|
相互转化 |
C+O2 CO2 CO2C+CO2  2CO 2CO | ||
干冰:
一定条件下,二氧化碳气体会变成固体,固体二氧化碳叫“干冰”。干冰升华时,吸收大量的热,因此可作制冷剂。如果用飞机向云层中撤干冰,由于干冰升华吸热,空气中的水蒸气迅速冷凝变成水滴,就可以形成降雨。
二氧化碳不一定能灭火:
二氧化碳一般不支持燃烧,但在一定条件下,某些物质也可以在二氧化碳中燃烧,如将点燃的镁条伸入盛有二氧化碳的集气瓶中,镁条能继续燃烧,反应的化学方程式为:2Mg+CO2
 2MgO+C,所以活泼金属着火不能用二氧化碳来灭火
2MgO+C,所以活泼金属着火不能用二氧化碳来灭火 二氧化碳与一氧化碳的鉴别方法:
(1)澄清石灰水:将气体分别通入澄清石灰水中,能使澄清石灰水变浑浊的是二氧化碳,无明显现象的是一氧化碳。
(2)燃着的木条:将气体分别在空气中点燃,能燃烧的是一氧化碳,不能燃烧的是二氧化碳。
(3)紫色石蕊试液:将气体分别通入紫色石蕊试液中,能使石蕊试液变红的是二氧化碳,无明显现象的是一氧化碳。
(4)还原金属氧化物:将气体分别通过灼热的氧化铜,出现黑色粉末变红这一现象的是一氧化碳,没有明显现象的是二氧化碳。
二氧化碳与一氧化碳的除杂方法:
1.CO(CO2)(括号内的物质为杂质):通常将气体通人过量的碱溶液(一般用氢氧化钠溶液而不用澄清石灰水)中,二氧化碳与碱溶液反应,从而达到除杂的目的。
2.CO2(CO)(括号内的物质为杂质):通常将气体通过灼热的氧化铜,一氧化碳与氧化铜反应生成铜和二氧化碳,从而达到除杂的目的。不能用点燃的方法,因为CO2不支持燃烧,也不能燃烧。
二氧化碳与石灰石的应用:
二氧化碳与石灰水反应出现白色沉淀,反应的方程式为:CO2+Ca(OH)2==CaCO3↓+H2O。
该反应及现象有以下儿方面的应用:
(1)检验二氧化碳气体;
(2)鉴别NaOH溶液和澄清石灰水:将CO2气体通入待测溶液中,生成白色沉淀的溶液为澄清石灰水,无明显现象的为NaOH溶液;
(3)除去某些气体中的杂质:如除去CO中的CO2 气体,可将混合气体通过澄清石灰水;
(4)解释澄清石灰水为什么要密封保存:敞口放置的澄清石灰水会吸收空气中的CO2而使澄清石灰水表面生成一层白膜或变浑浊,其成分是CaCO3;
(5)用石灰砂浆砌砖抹墙不久后变白变硬:石灰砂浆的主要成分是Ca(OH)2,吸收空气中的CO2发生反应Ca(OH)2声称白色固体CaCO3固体。
(6)保存鸡蛋:将鸡蛋浸泡在澄清石灰水中,取出来后CO2与石灰水反应封闭鸡蛋壳上的小孔,可以延长鸡蛋的保存时间。
二氧化碳肥料:
二氧化碳是光合作用的原料之一,因而现在在温室大棚内种植蔬菜水果时,经常人为提高温室内CO2 浓度,以增加农作物产员,增大CO2浓度的方法通常有以下几种:
(1)在温室内放置干冰,干冰升华增大CO2浓度。
(2)在温室内放置通过化学反应产生CO2气体的物质,如在塑料大棚顶部的容器内放置石灰石和稀盐酸。
灯火实验:
(1)二氧化碳本身无毒,但它不供给呼吸,当空气中二氧化碳含量超过常量时,也会对人体健康产生不良影响。
| 空气中二氧化碳的体积分数/% | 对人体健康的影响 |
| 1 | 感到气闷,头昏,心悸 |
| 4—5 | 气喘,头痛,眩晕 |
| 10 | 神志不清,呼吸停止,死亡 |
一氧化碳(CO)纯品为无色、无臭、无刺激性的气体。分子量28.01,密度1.250g/l,冰点为-207℃,沸点-190℃。在水中的溶解度甚低。空气混合爆炸极限为12.5%~74%。一氧化碳进入人体之后会和血液中的血红蛋白结合,进而使血红蛋白不能与氧气结合,从而引起机体组织出现缺氧,导致人体窒息死亡。因此一氧化碳具有毒性。一氧化碳是无色、无臭、无味的气体,故易于忽略而致中毒。常见于家庭居室通风差的情况下,煤炉产生的煤气或液化气管道漏气或工业生产煤气以及矿井中的一氧化碳吸入而致中毒。
物理性质:
通常状况下,是一种没有颜色,气味的气体,比空气略轻难溶于水。
化学性质:
(1)可燃性:2CO + O2
 2CO2
2CO2 (2)还原性:
一氧化碳还原氧化铜:CO+ CuO
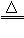 Cu + CO2
Cu + CO2 一氧化碳还原氧化铁:3CO+ Fe2O3
 2Fe + 3CO2
2Fe + 3CO2 一氧化碳还原四氧化三铁:4CO+ Fe3O4
 3Fe + 4CO2
3Fe + 4CO2 (3)毒性:
CO极易和血液中的血红蛋白结合,从而使血红蛋白不能很好地与氧气结合,造成生物体内缺氧,严重时危及生命。CO有剧毒,人在CO的体积分数达到 0.02%的空气中持续停留2—3h即出现中毒症状,因此我们使用煤、燃气热水器时要装烟囱,注意室内通风。
用途:
用作燃料,冶炼金属。
一氧化碳和氢气的比较
| 颜色状态 | 无色,无味气体 | 无色,无味气体 |
| 密度 | 1.250g/l(略小于空气) | 0.089g/l(最轻的气体) |
| 可燃性 | 有可燃性 2CO+O2  2CO2 2CO2 |
有可燃性 2H2+O2  2H2O 2H2O |
| 还原性 | 有还原性 CO+CuO 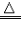 Cu+CO2 Cu+CO2 |
有还原性 H2+CuO  Cu+H2O Cu+H2O |
| 毒性 | 剧毒 | 无毒 |
| 鉴别方法 | 根据燃烧产物的不同鉴别 | |
H2、CO、C的比较
| H2 | C | CO | ||
| 可燃性 | 化学方程式 | 2H2+O2 2H2O 2H2O |
C+O2 CO2; CO2;2C+O2  2CO 2CO |
2CO+O2 2CO2 2CO2 |
| 反应现象 | 淡蓝色火焰,放热,生成 无色液体 |
发光,放热 | 蓝色火焰,放热, 生成的无色气体 能使澄清石灰水 变浑浊 | |
| 还原性 | 方程式 | 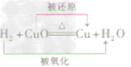 |
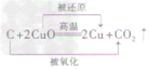 |
 |
| 反应现象 | 黑色固体变红,生成无色液体,管口有水珠 | 黑色固体变红,生成的无色气体能使澄清石灰水变洪浑浊 | 黑色固体变红,生成的无色气体能使澄清石灰水变浑浊 | |
| 装置图 |  |
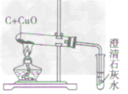 |
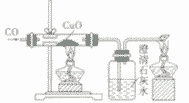 | |
| 装置要点 | 试管口略向下倾斜,导管贴试管上臂至药品上方,试管口没有橡皮塞 | 试管口略向下倾斜,导管刚过橡皮塞 | 多余的CO要进行尾气处理(如点燃) | |
| 主要步骤 | 通H2→加热→停止加热→停止通H2 | 反应结束后,先将导管从液体中取出,再停止加热 | 通CO→加热→停止加热→停止通CO | |
| 优点 | 反应条件低,生成物是水,不污染环境 | 原料便宜,操作简便 | 反应条件低 | |
| 缺点 | 不安全,操作复杂 | 反应条件高,生成物不易提纯 | 不安全,操作复杂,有毒 | |
| 用途 | 作工业原料,作高能燃料,冶炼金属 | 作燃料,冶炼金属, | 作燃料,冶炼金属, | |
(1)三种物质燃烧的现象有所不同,但不能根据火焰去鉴别CO和H2
(2)在还原CuO的实验中,必须对多余的CO进行处理
与“请你根据不同的实验内容,回答对应的问题:(1)仪器a的名称...”考查相似的试题有:
- 下列关于电解水的说法中,不正确的是( )A.电解水是分解反应B.电解时,水分子被破坏C.电解前后氢、氧原子的种类和数目都...
- 如图表示通电分解水的简易装置。(1)与电源 ____ 极相连的试管内收集到的气体具有可燃性,与电源的另一极相连的试管内收集到...
- 重庆是火锅的“故乡”,最近纸火锅在一些地方悄然兴起。纸火锅的材料是普通的纸,使用时不会被点燃的原因是[ ]A.纸火锅里的汤...
- 为探究燃烧的条件,某同学进行了如图所示的实验,有关的说法正确的是( )A.现象①②说明物质燃烧需要温度B.现象②③说明物质燃...
- 生产、生活中处处有化学.(1)在硫酸钾、碳酸氢铵、明矾三种物质中,可用作净水剂的是______;可用作氮肥的是______.(2)...
- 小明一家三口到火锅店吃火锅。(1)火锅常用的燃料有木炭、天然气、酒精(固体酒精)等。天然气中的主要成分在空气中燃烧的化...
- 下列有关人体生理活动的叙述,错误的是[ ]A.代谢产生的CO2,如不能及时排出,会使血液的pH增大B.无机盐和水虽不能提供能量,...
- 气体的制取和性质等一系列问题的研究历来是中学化学的重要内容.I.有下列仪器装置、实验示意图(1)写出实验室制取CO2的化学...
- 现有“氧气、二氧化碳、氢气、氮气、稀有气体、明矾、活性炭”等物质,填写下列空格:(1)为防止膨化食品易碎和延长保质期而充...
- 下列图象关系正确的是( )A.表示CO还原CuO的实验中,试管内的固体质量与时间的关系图B.表示向一定量的稀硫酸中加入过量Ba...
 2CO2
2CO2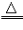 Cu+CO2
Cu+CO2