本试题 “根据碘与氢气反应的热化学方程式 (i) I2(g)+ H2(g)2HI(g) △H=-9.48 kJ/mol(ii) I2(s)+H2(g)2HI(g) △H=+26.48 kJ/mol 下列判断正确的是[ ]A.254g I2(g)中通入...” 主要考查您对焓变、反应热
盖斯定律
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 焓变、反应热
- 盖斯定律
反应热,焓变:
化学能可以转化为热能、电能和光能等,化学反应中的能量变化,通常主要表现为热量的变化。
1.定义:在化学反应过程中,当生成物和反应物具有相同温度时所放出或吸收的热量,通常叫做化学反应的反应热。在恒温、恒压条件下,化学反应过程中吸收或放出的热量称为反应的焓变。
2.符号:△Ⅳ
3.单位:kJ·mol-1
4.产生原因:化学反应过程中旧键断裂吸收的总能量与新键形成释放的总能量不相等,故化学反应均伴随着能量变化——吸热或放热。
5.表示方法:放热反应的△H<0,吸热反应的△H>0.
化学能可以转化为热能、电能和光能等,化学反应中的能量变化,通常主要表现为热量的变化。
1.定义:在化学反应过程中,当生成物和反应物具有相同温度时所放出或吸收的热量,通常叫做化学反应的反应热。在恒温、恒压条件下,化学反应过程中吸收或放出的热量称为反应的焓变。
2.符号:△Ⅳ
3.单位:kJ·mol-1
4.产生原因:化学反应过程中旧键断裂吸收的总能量与新键形成释放的总能量不相等,故化学反应均伴随着能量变化——吸热或放热。
5.表示方法:放热反应的△H<0,吸热反应的△H>0.
盖斯定律的内容:
不管化学反应是一步完成还是分几步完成,其反应热是相同的。换句话说,化学反应的反应热只与反应的始态和终态有关,而与反应进行的途径无关。如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一一步完成时的反应热是相同的,这就是盖斯定律。
盖斯定律的意义:
利用盖斯定律可以间接计算某些不能直接测得的反应的反应热。例如: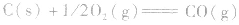 的△H无法直接测得,可以结合下面两个反应的△H,利用盖斯定律进行计算。
的△H无法直接测得,可以结合下面两个反应的△H,利用盖斯定律进行计算。
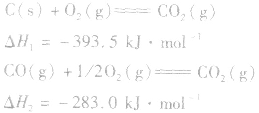
根据盖斯定律,就可以计算出所给反应的△H。分析上述两个反应的关系,即知
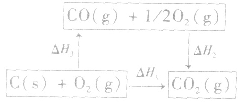
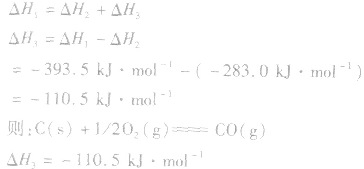
盖斯定律在反应热大小比较中的应用:
1.同一反应生成物状态不同时
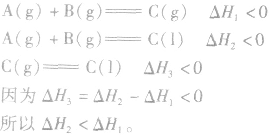
若按以下思路分析:
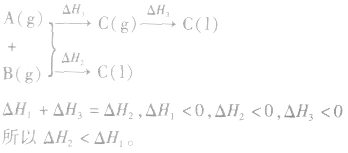
2.同一反应物状态不同时
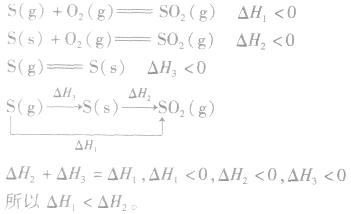
3.两个有联系的不同反应相比
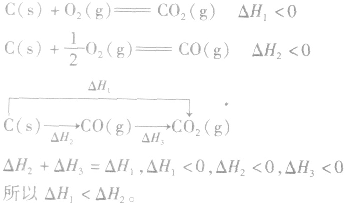
并且据此可写出下面的热化学方程式:

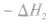
不管化学反应是一步完成还是分几步完成,其反应热是相同的。换句话说,化学反应的反应热只与反应的始态和终态有关,而与反应进行的途径无关。如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一一步完成时的反应热是相同的,这就是盖斯定律。
盖斯定律的意义:
利用盖斯定律可以间接计算某些不能直接测得的反应的反应热。例如:
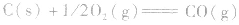 的△H无法直接测得,可以结合下面两个反应的△H,利用盖斯定律进行计算。
的△H无法直接测得,可以结合下面两个反应的△H,利用盖斯定律进行计算。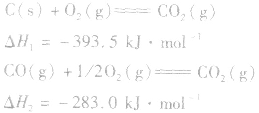
根据盖斯定律,就可以计算出所给反应的△H。分析上述两个反应的关系,即知
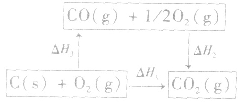
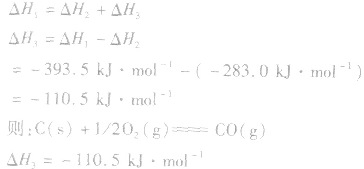
盖斯定律在反应热大小比较中的应用:
1.同一反应生成物状态不同时
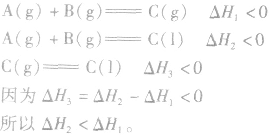
若按以下思路分析:
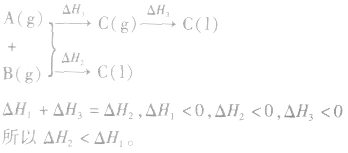
2.同一反应物状态不同时
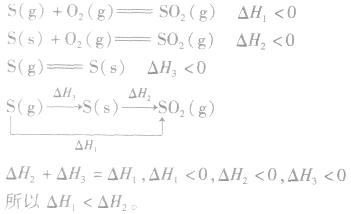
3.两个有联系的不同反应相比
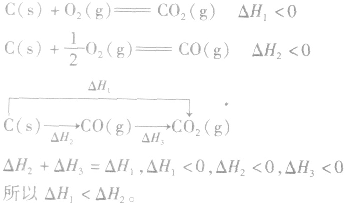
并且据此可写出下面的热化学方程式:

发现相似题
与“根据碘与氢气反应的热化学方程式 (i) I2(g)+ H2(g)2HI(g) △H=...”考查相似的试题有:
- (1)已知红磷比白磷稳定,又知:4P(白磷,s)+5O2(g)=2P2O5(s) △H1;4P(红磷,s)+5O2(g)=2P2O5(s) △H2,则ΔH1和...
- 下列各项与反应热的大小无关的是[ ]A.反应物和生成物的状态B.反应物量的多少C.反应物的性质D.反应的快慢
- 下列关于反应能量的说法正确的是( )A.Zn(s)+CuSO4(aq)===ZnSO4(aq)+Cu(s)ΔH=-216 kJ·mol-1,E反应物
- 下列说法中,正确的是( )A.放热反应不需要加热就可以发生B.化学反应除了生成新物质外,还伴随着能量的变化C.反应条件为...
- 已知298K时,2SO2(g) + O2(g)2SO3(g);△H =—Q1kJ/mol,在相同温度下,向密闭容器中通入4molSO2和1molO2,达到平衡时放出热量Q...
- 钛(Ti )被称为继铁、铝之后的第三金属.如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污...
- 已知:C(s,金刚石)=C(s,石墨)△H=-1.9KJ/molC(s,金刚石)+O2(g)=CO2(g) △H1C(s,石墨)+O2(g)=CO2(g) △H2根据已述反应...
- 在常温常压下,已知:4Fe(s)+3O2(g)=2Fe2O3(s)△H14Al(s)+3O2(g)=2Al2O3(s)△H22Al(s)+Fe2O3(s)=Al2O3(s)+2F...
- 已知:(1)Zn(s)+12O2(g)═ZnO(s),△H=-348.3kJ•mol-1,(2)2Ag(s)+12O2(g)═Ag2O(s),△H=-31.0kJ•mol-1,则Zn(...
- 已知热化学方程式:C(金刚石,s)+O2(g)=CO2(g)△H1C(石墨,s)+O2(g)=CO2(g)△H2C(石墨,s)=C(金刚石,s)△H3=1....