本试题 “38.4gCu跟适量的浓HNO3反应,Cu全部作用后,在标准状况下收集到气体22.4L,求消耗的HNO3的物质的量是多少?” 主要考查您对金属、非金属的有关计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 金属、非金属的有关计算
包括金属及化合物、金属与非金属化合物、非金属化合物之间的反应的计算,解此类题的关键是正确的写出反应方程式,明确物质间的等量关系。明确物质之间的反应,正确写出方程式,此类题可迎刃而解。
AlCl3与NaOH反应的相关计算:
1、求Al(OH)3沉淀的量
2、求反应物碱的量
铝与酸、碱反应的计算规律:
铝分别与盐酸、氢氧化钠溶液反应的原理: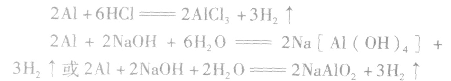
(1)等量铝分别与足量盐酸和氢氧化钠溶液反应,产生氢气的体积比为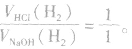
(2)足量的锅分别与等物质的量的盐酸和氢氧化钠溶液反应,产生氢气的体积比为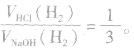
(3)一定量的铝分别和一定量的盐酸和氢氧化钠溶液反应,若产生氢气的体积比为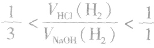 ,则必定是:
,则必定是:
①铝与盐酸反应时,铝过量而盐酸不足;
②铝与氢氧化钠溶液反应时,铝不足而氢氧化钠过量。
解有关硝酸与金属反应的计算题的技巧:
1.灵活运用得失电子守恒、原子守恒及溶液中的电荷守恒关系例如Cu与HNO3反应中就有以下等量关系:
(1)N原子守恒:反应前所有的N只存在于HNO3中;反应后含N的物质有HNO3的还原产物(假设此处有NO3、NO)和Cu(NO3)3,若HNO3过量,则过量HNO3中也含一部分N,则有:n(N)=n(NO2)+ n(NO)+2n[Cu(NO3)3]+n剩(HNO3)。
(2)得失电子守恒:在反应中失去电子的是参加反应的Cu, ;得到电子的是被还原的HNO3(假设还原产物为NO2、NO),NO3-+e→ NO2、NO3-+3e→NO。根据得失电子守恒,则有:
;得到电子的是被还原的HNO3(假设还原产物为NO2、NO),NO3-+e→ NO2、NO3-+3e→NO。根据得失电子守恒,则有: 
(3)溶液中的电荷守恒:在任何溶液中,阴离子所带负电荷总数与阳离子所带正电荷总数在数值上是相等的。在Cu与HNO3反应后的溶液中,若HNO3不过量,阳离子只有Cu2+,阴离子只有NO3-(此类计算不考虑H2O电离出的极少量的H+、OH-);若HNO3过量,溶液中阳离子有Cu2+和H+,阴离子只有NO3-。则有:
①若HNO3不过量: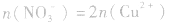
②若HNO3过量: 
2.铁与稀HNO3的反应规律 

(2)上述反应可以认为先发生反应①,若Fe有剩余则发生 ①×2+ ③即得反应②,所以,无论是反应①还是反应②,被还原的HNO3皆占参加反应的HNO3的
①×2+ ③即得反应②,所以,无论是反应①还是反应②,被还原的HNO3皆占参加反应的HNO3的 。
。
有关镁、铝的图像集锦:
Al(OH)3与Al3+、AlO2-之间的转化,是建立在 Al(OH)3两性基础上的,有关相互转化的配比和沉淀Al(OH)3的质量变化,见下表:
与“38.4gCu跟适量的浓HNO3反应,Cu全部作用后,在标准状况下收集...”考查相似的试题有:
- 在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除氧化膜,并用针刺一些小孔的铝箔包好,然后放人盛水且倒置于水...
- 将2.3 g Na和2.7 g Al同时加入到足量的水中充分反应,将反应后的溶液稀释、定容为500 mL。 下列说法正确的是 [ ]A.反应中放...
- 将等体积的AlCl3溶液和NaOH溶液混合后,沉淀物中含铝元素的质量与溶液中含铝元素的质量相等,则原AlCl3溶液与NaOH溶液的物质...
- 烟气脱硫是控制二氧化硫污染的主要技术手段。(1)利用海水脱硫是一种有效的方法,其工艺流程如下图所示: 某研究小组为探究提...
- 12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中NO2的体积是[ ]A.10.8mLB.2.4mL...
- Cu与一定浓度的硝酸反应时,其方程式可表示为 Cu+HNO3—Cu(NO3)2+NO↑+NO2↑+H2O(1)硝酸在反应中的性质是 _______________。(...
- 把铝粉和氧化亚铁粉末配成铝热剂,分成两等份。一份在高温下恰好完全反应后,再与足量盐酸起反应;另一份与足量的烧碱溶液中...
- 用足量的CO还原32.0克某种氧化物,将生成的气体通入足量澄清石灰水中,得60克沉淀,则该氧化物是[ ]A. MgOB. Fe2O3C. CaOD. Cu2O
- 某溶液中除H+、OH-外,还含有大量的Mg2+、Fe3+、Cl-,且这三种离子的物质的量浓度之比为1:1:6。下列有关该溶液的判断正确的...
- 将0.4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质...