本试题 “I、(1)NaHCO3是一种______(填“强”或“弱”)电解质;(2)写出HCO3-水解的离子方程式:______;(3)常温下,0.1mol•L-1NaHCO3溶液的pH大于8,则溶液中Na+、...” 主要考查您对盐类水解的定义
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 盐类水解的定义
盐类水解:
1.定义:在水溶液中盐电离出来的离子跟水电离出来的H+或OH-结合生成弱电解质的反应,叫做盐类水解。
2.实质:生成弱电解质,使水的电离平衡被破坏而建立新的平衡。
3.条件:盐中必须有弱酸根离子或弱碱阳离子,盐溶于水。
4.特点:可逆性,写水解离子方程式时要用“ ” 水解是吸热过程,是中和反应的逆过程。一般,水解的程度较小,写离子方程式时,不能用“↑”或“↓”符号。多元弱酸根分步水解,以第一步为主。多元弱碱阳离子一步水解。
” 水解是吸热过程,是中和反应的逆过程。一般,水解的程度较小,写离子方程式时,不能用“↑”或“↓”符号。多元弱酸根分步水解,以第一步为主。多元弱碱阳离子一步水解。
5.规律:有弱才水解,无弱不水解。谁弱谁水解,谁强显谁性。越弱越水解,都弱都水解。例如:25℃时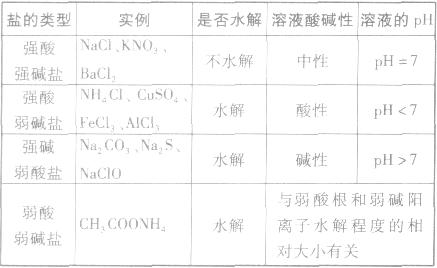
四种重要的动态平衡的比较:
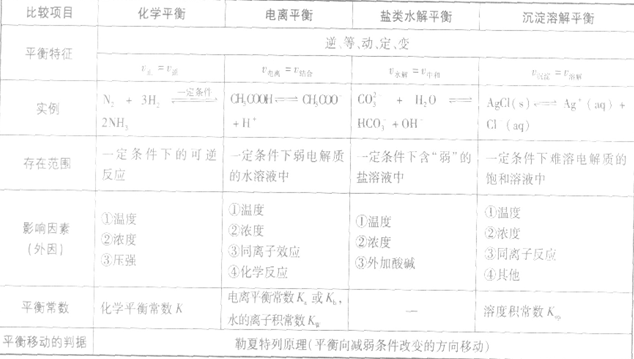
发现相似题
与“I、(1)NaHCO3是一种______(填“强”或“弱”)电解质;(2)写...”考查相似的试题有:
- 氯化钠是一种重要的生活、生产必需品.下列叙述中正确的是( )A.锌粒与盐酸反应时,若加入适量氯化钠晶体,可加快反应速率B...
- 下列离子方程式正确的是( )A.硫化钠水解 S2-+2H2OH2S+2OH-B.硫氢化钠的水解 HS-+H2OH3O++S2-C.不断加热煮沸氯化铁溶液 F...
- 下列溶液中有关微粒的物质的量浓度关系正确的是 ( )
- CuSO4溶液是中学化学及工农业生产中常见的一种试剂。(1)某同学配制CuSO4溶液时,向盛有一定量硫酸铜晶体的烧杯中加入适量的蒸...
- 物质的量浓度均为0.1mol/L的下列溶液:①KNO3、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH、⑦Ba(OH)2、⑧NH4Cl,pH由大到小的...
- 下列离子组中因相互促进水解而不能共存的离子组是:( )A.H2PO4-、Na+、Cl-、OH-B.Al3+、Na+、HCO3-、SO42-C.H+、Fe2+、N...
- 下列能正确表示水解的离子方程式是A.CH3COOH + H2OCH3COO-+ H3O+B.Br-+ H2OHBr + OH-C.CO32-+ 2H2OH2CO3+ 2OH-D.NH4++ H2...
- 物质A~E都是由下表中的离子组成的,常温下将各物质的溶液从1 mL稀释到1 000 mL,pH的变化关系如图甲所示,其中A与D反应得到E...
- (12分)在生产生活和科学研究中,人们常常根据需要促进或抑制盐的水解。试回答下列问题:(1)FeCl2溶液呈 (填“酸”、“中”、...
- 下列各溶液中,微粒的物质的量浓度关系正确的是( )A.常温下,在pH=8的NaA溶液中:c(Na+)-c(A-)=9.9×10-7mol/LB.由10m...