本试题 “下列与处理方法对应的反应方程式不正确的是[ ]A.用Na2S去除废水中的Hg2+:Hg2++S2-=HgS↓B.用催化法处理汽车尾气中的CO和NO:CO+NOC+NO2C.向污水中投放明矾...” 主要考查您对离子方程式
有机反应方程式
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 离子方程式
- 有机反应方程式
用实际参加反应的离子符号表示离子反应的式子。
离子方程式书写规则:
①写:写出化学反应方程式
②拆:把易溶于水、易电离的物质写成离子形式,难容难电离的物质及气体等仍用化学式表示
③删:删去方程式两边不参加反应的离子
④查:检查离子方程式两边各元素的原子个数和电荷总数是否相等
离子方程式书写及正误的判断方法:
①判断反应是否在水溶液中进行
因为电解质在水溶液中可以电离为自由移动的离子,在这种条件下才能发生离子反应。
②判断反应能否发生。
如果反应不能发生,当然也就没有离子方程式可言。
③判断反应物、生成物是否正确。
④判断质量和电荷是否守恒。
离子方程式不仅要质量守恒,而且反应前后各离子所带电荷总数必须相等。
⑤判断氧化物、难溶物、气体、单质、难电离的弱酸、弱碱、水是否写成了分子形式,而易电离的物质是否写成离子形式。
⑥判断连接符号“=”和“
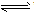 ”及状态符号“↑”和“↓”运用是否正确。
”及状态符号“↑”和“↓”运用是否正确。 强电解质的电离、不可逆反应、双水解反应用“=”;弱电解质电离、可逆反应、水解反应用“
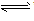 ”。复分解反应、水解反应生成的难溶物用“↓”,气体用“↑”;单水解反应生成的难溶物不用“↓”,气体不用“↑”。
”。复分解反应、水解反应生成的难溶物用“↓”,气体用“↑”;单水解反应生成的难溶物不用“↓”,气体不用“↑”。 ⑦判断微溶物的处理是否正确。
微溶物做反应物时,一般用离子形式,做生成物时一般用分子式。
⑧判断反应物的滴加顺序与方程式中生成物是否一致。
如:把碳酸钠溶液滴加到盐酸溶液中,和把盐酸滴加到碳酸钠溶液中反应产物是不同的。
⑨判断反应物的相对量与产物是否一致。
有些反应因反应物的量不同会生成不同的产物。如:CO2、SO2、H2S等气体与碱溶液反应时,若气体少量,则生成正盐;若气体过量,则生成酸式盐。
⑩判断电解质在写成离子形式时阴阳离子个数比是否合理。
如Ba(OH)2溶液和稀H2SO4反应的离子方程式往往错误写成:
 ,正确为:
,正确为: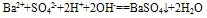
书写与量有关的离子方程式:
基本方法是:把物质的量少的物质的系数定为1,其他物质按最大量消耗。
1.因滴加顺序不同造成连续反应
- HCl与Na2CO3
向Na2CO3溶液中滴入盐酸溶液至过量,其离子反应分步写 (1)CO32-+H+==HCO3- (2)HCO3-+H+==CO2↑+H2O
若向盐酸溶液中滴入Na2CO3溶液至不再产生气体,其离子反应一步完成 CO32-+2H+==CO2↑+H2O
若向足量Na2CO3溶液中加入少量的盐酸溶液,其离子方程式为: CO32-+H+==HCO3-
- HCl与NaAlO2
向Na2CO3溶液中滴入盐酸溶液至过量,其离子反应分步写 (1)CO32-+H+==HCO3- (2)HCO3-+H+==CO2↑+H2O
若向盐酸溶液中滴入Na2CO3溶液至不再产生气体,其离子反应一步完成 CO32-+2H+==CO2↑+H2O
若向足量Na2CO3溶液中加入少量的盐酸溶液,其离子方程式为: CO32-+H+==HCO3-
- AlCl3与NaOH
向AlCl3溶液中滴入NaOH溶液至过量,其离子反应分步写 (1)Al3++3OH-==Al(OH)3↓ (2)Al(OH)3+OH-==AlO2-+2H2O
若向NaOH溶液中加入少量AlCl3溶液,其离子反应一步完成 Al3++4OH-==AlO2-+2H2O
若向足量Al2(SO4)3溶液中加入少量的NaOH溶液,其离子方程式为: Al3++3OH-==Al(OH)3↓
- AgNO3与NH3·H2O
向AgNO3溶液中滴入稀NH3·H2O至过量,其离子反应分步写(1) Ag++NH3·H2O==AgOH↓+NH4+ (2)AgOH+2NH3·H2O==Ag(NH3)2++OH-+2H2O
若向NH3·H2O溶液中加入少量AgNO3,其离子反应一步完成 Ag++3NH3·H2O==Ag(NH3)2++OH-+NH4++2H2O
若向足量AgNO3溶液中滴入少量NH3·H2O,其离子方程式为:Ag++NH3·H2O==AgOH↓+NH4+
- CO2与NaOH
向NaOH溶液中通人CO2气体至过量,其离子反应分步写 (1)2OH-+CO2==CO32-+H2O (2)CO32-+CO2+H2O==2HCO3-
若向足量NaOH溶液中通人少量CO2气体,其离子方程式为: 2OH-+CO2==CO32-+H2O
若向NaOH溶液中通人过量CO2气体,其离子反应一步完成 OH-+CO2==HCO3-
2.过量型:
向足量的Ca(HCO3)2溶液中逐渐滴入NaOH溶液 OH-+Ca2++HCO3-==H2O+CaCO3↓
向足量的NaOH溶液中逐渐滴入Ca(HCO3)2溶液 Ca2++2HCO3-+2OH-==2H2O+CaCO3↓+CO32-
Fe与HNO3 :铁过量时:Fe+4HNO3==Fe(NO3)3+NO↑+2H2O
铁不足时:3Fe+8HNO3==3Fe(NO3)2+2NO↑+4H2O
3.定量型:
因还原性I->Fe2+>Br-,所以在FeI2或者FeBr2中通入一定量的Cl2,发生不同的离子反应,依次为:
(1)2I-+Cl2==2Cl-+I2(2)2Fe2++Cl2==2Fe3++2Cl-(3)2Br-+Cl2==2Cl-+Br2
4.目标型
向明矾溶液逐滴滴加Ba(OH)2溶液至硫酸根离子刚好沉淀完全 Al3++SO42-+Ba2++4OH-==AlO2-+2BaSO4↓+2H2O
向明矾溶液逐滴滴加Ba(OH)2溶液至铝离子刚好沉淀完全 Al3+SO42-+Ba2++3OH-==Al(OH)3↓+2BaSO4↓
(1)有机反应方程式中有机物写结构简式。
在书写有机物结构简式时,注意:碳只能形成四个共价键,不能少写或多写氢。
例新戊烷(CH3)4C,不能写成(CH2)4C或(CH3)4CH2。
(2)一些基团的连接方式要即正确又合乎习惯,不产生歧义。
例醛基-CHO,不能写成CHO-也不能写成-COH(写成此种形式,可能会误认为碳原子和氧原子之间是单键)。另外常见官能团-C6H5、-OH、-NO、-NH2、-COOH等不能写成C6H5-、OH-、NO2-、NH2-、COOH-等,尤其注意官能团写在物质左侧的。
(3)注意有机反应的条件,反应物和产物中间用“→”连接。
有机反应方程式举例:
一、烷烃、烯烃、炔烃
1. 甲烷的实验室制法C2H5OH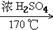 CH2=CH2↑+H2O
CH2=CH2↑+H2O
2. 甲烷燃烧CH4+2O2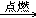 CO2+2H2O
CO2+2H2O
3. 甲烷与氯气CH4+Cl2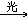 CH3Cl+HCl
CH3Cl+HCl
CH3Cl+Cl2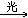 CH2Cl2+HCl
CH2Cl2+HCl
CH2Cl2+Cl2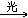 CHCl3+HCl
CHCl3+HCl
CHCl3+Cl2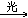 CCl4+HCl
CCl4+HCl
4. 甲烷隔绝空气时高温分解CH4 C+2H2
C+2H2
5. 丁烷的裂解(两个方程式)C4H10 CH4+C3H6
CH4+C3H6
C4H10 C2H4+C2H6
C2H4+C2H6
6. 乙烯的实验室制法CH3CH2OH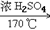 CH2=CH2↑+H2O
CH2=CH2↑+H2O
7. 乙烯燃烧C2H4+3O2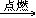 2CO2+2H2O
2CO2+2H2O
8. 乙烯使溴水褪色CH2=CH2+Br2→CH2Br─CH2Br
9. 乙烯与水在催化剂下反应CH2=CH2+H2O C2H5OH
C2H5OH
12. 乙烯的加聚
13. 乙烯与丙烯1:1加聚
14. 异戊二烯聚合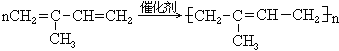
15. 苯乙烯与异戊二烯1:1加聚
16. 乙炔的实验室制法CaC2+2H2O→CH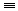 CH↑+Ca(OH)2
CH↑+Ca(OH)2
17. 乙炔与足量氢气反应CH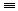 CH+2H2
CH+2H2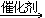 CH3-CH3
CH3-CH3
18. 乙炔的聚合
19. 由乙炔制备聚氯乙烯CH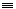 CH+HCl
CH+HCl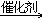 CH2=CHCl
CH2=CHCl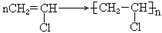
二、苯及其同系物
20. 苯燃烧2C6H6+15O2 12CO2+6H2O
12CO2+6H2O
21. 苯与液溴反应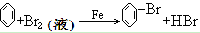
22. 甲苯的硝化反应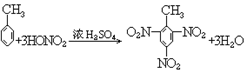
23. 苯与氢气反应
25. 甲苯与浓硝酸、浓硫酸反应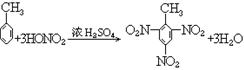
三、卤代烃的性质
26. 溴乙烷的消去反应CH3CH2Br+NaOH CH2=CH2↑+NaBr+H2O
CH2=CH2↑+NaBr+H2O
27. 溴乙烷的水解反应CH3-CH2-Br+NaOH CH3-CH2-OH+NaBr
CH3-CH2-OH+NaBr
28. 氯苯与氢氧化钠水溶液反应
四、醇的性质
29. 乙醇燃烧C2H5OH+3O2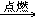 2CO2+3H2O
2CO2+3H2O
30. 乙醇与钠反应2C2H5OH+2Na→2C2H5ONa+H2↑
31. 乙醇的催化氧化2C2H5OH+O2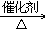 2CH3CHO+2H2O
2CH3CHO+2H2O
32. 乙醇与浓硫酸反应(两个方程式)CH3CH2OH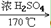 CH2=CH2↑+H2O
CH2=CH2↑+H2O
2CH3CH2OH CH3─CH2─O─CH2─CH3+H2O
CH3─CH2─O─CH2─CH3+H2O
33. 乙醇与乙酸反应C2H5OH+CH3COOH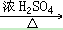 CH3COOC2H5+H2O
CH3COOC2H5+H2O
34. 乙二醇与钠反应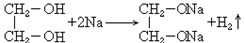
35. 甘油与硝酸反应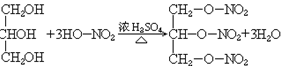
五、酚的性质
36. 苯酚与钠反应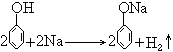
37. 苯酚与氢氧化钠反应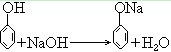
38. 苯酚与浓溴水反应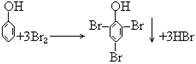
39. 苯酚钠与二氧化碳反应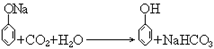
40. 苯酚与甲醛缩聚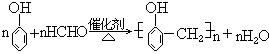
与“下列与处理方法对应的反应方程式不正确的是[ ]A.用Na2S去除...”考查相似的试题有:
- 下列离子方程式书写正确的是( )A.在FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-B.向CaCl2溶液中通入二氧...
- 写出下列反应的离子方程式(1)过氧化钠与水______;(2)金属铝与稀硫酸溶液______;(3)向Na2CO3与NaHCO3混和溶液加入CaCl...
- 下列反应的离子方程式正确的是A 硫酸铜溶液与氢氧化钡溶液反应: Ba2++SO42-= BaSO4↓B 向三氯化铝溶液中加入过量氨水:Al3+...
- 下列离子方程式正确的是[ ]A.用铂电极电解氯化镁溶液:2Cl-+ 2H2O2OH-+ Cl2↑+H2↑B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+===...
- 能正确解释下列反应原理的离子方程式[ ]A.AlCl3溶液中通入过量的NH3:Al3++4NH3·H2O=AlO2-+4NH4+B.淀粉碘化钾试纸上滴稀硝...
- 下列实验设计及其对应的离子方程式均正确的是( )A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+= Cu2++ 2Fe2+B.Na2O2与H2O反应...
- 已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3══3Cu(NO3)2+2NO↑+4H2O(1)用单线桥法分析上述反应。____...
- X、Y、Z三种物质有如图所示转化关系(1)根据上述转化关系,写出下列物质的化学式:X 、Y 、Z 试剂甲 ,试剂乙 (每空1分)。...
- 下列反应的离子方程式正确的是A.碳酸钙跟盐酸反应: CO32-+2H+=CO2↑+H2OB.氨水跟盐酸反应: OH-+ H+= H2OC.氢氧...
- 下列各组离子反应可用H++OH—= H2O表示的是 ( ) A.氢氧化钡和硫酸B.氢氧化铜和盐酸C.硝酸和氢氧化钠D.硫酸和氢氧化镁