本试题 “(1)用化学符号填空:①一个氮分子______;②两个铁原子______;③硫酸铜溶液中的金属离子______;④标出氧化铁中铁元素的化合价______;(2)硫在空气中燃烧的...” 主要考查您对化学反应方程式的书写
文字表达式
化合价的写法和意义
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应方程式的书写
- 文字表达式
- 化合价的写法和意义
化学方程式的书写原则遵循两个原则:
一是必须以客观事实为基础,绝不能凭空设想、主观臆造事实上不存在的物质和化学反应;
二是遵循质量守恒定律,即方程式两边各种原子的种类和数目必须相等。
书写化学方程式的具体步骤:
(1)写:根据实验事实写出反应物和生成物的化学式。反应物在左,生成物在右,中间用横线连接,如: H2+O2——H2O,H2O——H2+O2。
(2)配:根据反应前后原子的种类和数目不变的原则,在反应物和生成物的化学式前配上适当的化学计量数,使各种元素的原子个数在反应前后相等,然后将横线变成等号。配平后,化学式前的化学计量数之比应是最简整数比,如:2H2+O2=2H2O,2H2O= 2H2+O2。
(3)注:注明反应条件【如点燃、加热(常用“△”表示)、光照、通电等〕和生成物的状态(气体用“↑”。沉淀用“↓”。)。如:2H2+O2 2H2O,2H2O
2H2O,2H2O 2H2↑+O2↑。
2H2↑+O2↑。
化学计量数:
化学计量数指配平化学方程式后,化学式前面的数字。在化学方程式中,各化学式前的化学计量数之比应是最简整数比,计数量为1时,一般不写出。
书学化学方程式的常见错误:
书写化学方程式时条件和气体、沉淀符号的使用:
(1).“△”的使用
①“△”是表示加热的符号,它所表示的温度一般泛指用酒精灯加热的温度。
②如果一个反应在酒精灯加热的条件下能发生,书写化学方程式时就用“△”,如:2KMnO4 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
③如果一个反应需要的温度高于用酒精灯加热的温度,一般用“高温”表示;如:CaCO3 CaO+ CO2↑
CaO+ CO2↑
(2)“↑”的使用
①“↑”表示生成物是气态,只能出现在等号的右边。
②当反应物为固体、液体,且生成的气体能从反应体系中逸出来,气体化学式后应该加“↑”。如Fe+ 2HCl==FeCl2+H2↑。
③当反应物是溶液时,生成的气体容易溶于水而不能从反应体系中逸出来,则不用“↑”,如:H2SO4+ BaCl2==FeCl2+2HCl
④只有生成物在该反应的温度下为气态,才能使用“↑”。
⑤若反应物中有气态物质,则生成的气体不用标 “↑”。如:C+O2 CO2
CO2
(3)“↓”使用
①“↓”表示难溶性固体生成物,只能出现在等号的右边
②当反应在溶液中进行,有沉淀生成时,用 “↓”,如:AgNO3+HCl==AgCl↓+HNO3
③当反应不在溶液中进行,尽管生成物有不溶性固体,也不用标“↓”,如:2Cu+O2 2CuO
2CuO
④反应在溶液中进行,若反应物中有难溶性物质,生成物中的难溶性物质后面也不用标“↓”。如:Fe +CuSO4==FeSO4+Cu.
化学方程式中“↑”和“↓”的应用:
①“↑”或“↓”是生成物状态符号,无论反应物是气体还是固体,都不能标“↑”或“↓”;
②若反应在溶液中进行且生成物中有沉淀,则使用“↓”;若不在溶液中进行,无论生成物中是否有固体或难溶物,都不使用“↓”;
③常温下,若反应物中无气体,生成物中有气体.
提取信息书写化学方程式的方法:
书写信息型化学方程式是中考热点,题目涉及社会、生产、生活、科技等各个领域,充分体现了化学学科的重要性,并考查了同学们接受信息、分析问题和解决问题的能力。解答这类题日的关键是掌握好化学方程式的书写步骤,可按两步进行:首先正确书写反应物和生成物的化学式,并注明反应条件及生成物状态;第二步就是化学方程式的配平。
一是必须以客观事实为基础,绝不能凭空设想、主观臆造事实上不存在的物质和化学反应;
二是遵循质量守恒定律,即方程式两边各种原子的种类和数目必须相等。
书写化学方程式的具体步骤:
(1)写:根据实验事实写出反应物和生成物的化学式。反应物在左,生成物在右,中间用横线连接,如: H2+O2——H2O,H2O——H2+O2。
(2)配:根据反应前后原子的种类和数目不变的原则,在反应物和生成物的化学式前配上适当的化学计量数,使各种元素的原子个数在反应前后相等,然后将横线变成等号。配平后,化学式前的化学计量数之比应是最简整数比,如:2H2+O2=2H2O,2H2O= 2H2+O2。
(3)注:注明反应条件【如点燃、加热(常用“△”表示)、光照、通电等〕和生成物的状态(气体用“↑”。沉淀用“↓”。)。如:2H2+O2
 2H2O,2H2O
2H2O,2H2O 2H2↑+O2↑。
2H2↑+O2↑。 化学计量数:
化学计量数指配平化学方程式后,化学式前面的数字。在化学方程式中,各化学式前的化学计量数之比应是最简整数比,计数量为1时,一般不写出。
书学化学方程式的常见错误:
| 常见错误 | 违背规律 |
| 写错物质的化学式 | 客观事实 |
| 臆造生成物或事实上不存在的化学反应 | |
| 写错或漏泄反应条件 | |
| 化学方程式没有配平 | 质量守恒 |
| 漏标多标“↑”、“↓”符号 | —— |
书写化学方程式时条件和气体、沉淀符号的使用:
(1).“△”的使用
①“△”是表示加热的符号,它所表示的温度一般泛指用酒精灯加热的温度。
②如果一个反应在酒精灯加热的条件下能发生,书写化学方程式时就用“△”,如:2KMnO4
 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。 ③如果一个反应需要的温度高于用酒精灯加热的温度,一般用“高温”表示;如:CaCO3
 CaO+ CO2↑
CaO+ CO2↑(2)“↑”的使用
①“↑”表示生成物是气态,只能出现在等号的右边。
②当反应物为固体、液体,且生成的气体能从反应体系中逸出来,气体化学式后应该加“↑”。如Fe+ 2HCl==FeCl2+H2↑。
③当反应物是溶液时,生成的气体容易溶于水而不能从反应体系中逸出来,则不用“↑”,如:H2SO4+ BaCl2==FeCl2+2HCl
④只有生成物在该反应的温度下为气态,才能使用“↑”。
⑤若反应物中有气态物质,则生成的气体不用标 “↑”。如:C+O2
 CO2
CO2 (3)“↓”使用
①“↓”表示难溶性固体生成物,只能出现在等号的右边
②当反应在溶液中进行,有沉淀生成时,用 “↓”,如:AgNO3+HCl==AgCl↓+HNO3
③当反应不在溶液中进行,尽管生成物有不溶性固体,也不用标“↓”,如:2Cu+O2
 2CuO
2CuO ④反应在溶液中进行,若反应物中有难溶性物质,生成物中的难溶性物质后面也不用标“↓”。如:Fe +CuSO4==FeSO4+Cu.
化学方程式中“↑”和“↓”的应用:
①“↑”或“↓”是生成物状态符号,无论反应物是气体还是固体,都不能标“↑”或“↓”;
②若反应在溶液中进行且生成物中有沉淀,则使用“↓”;若不在溶液中进行,无论生成物中是否有固体或难溶物,都不使用“↓”;
③常温下,若反应物中无气体,生成物中有气体.
提取信息书写化学方程式的方法:
书写信息型化学方程式是中考热点,题目涉及社会、生产、生活、科技等各个领域,充分体现了化学学科的重要性,并考查了同学们接受信息、分析问题和解决问题的能力。解答这类题日的关键是掌握好化学方程式的书写步骤,可按两步进行:首先正确书写反应物和生成物的化学式,并注明反应条件及生成物状态;第二步就是化学方程式的配平。
概念:用文字表示化学反应的式子
文字表达式的书写步骤:
(1)写:根据反应事实写出反应物和生成物
(2)注:注明反应条件:[点燃,加热,光照,通电等]
文字表达式的书写步骤:
(1)写:根据反应事实写出反应物和生成物
(2)注:注明反应条件:[点燃,加热,光照,通电等]
化合价的定义:
一种元素一定数目的原子跟其他元素一定数目的原子相化合的性质,叫做这种元素的化合价。化合价有正价、负价之分,如在H2O中,氢原子与氧原子的个数比为2:1,H为+1价,0为-2价;在MgCl2中,镁原子与氯原子的个数比为1:2,Mg为+2价,Cl为-1价。
化合价的意义:
化合价反映元素的原子之间相互化合时的数日,是元素的一种性质。因此,强调化合价时,一定要指明元素。
化合价的表示方法:
通常在元素符一号或原子团的正上方用+n或-n表示,“+”“-”在前,数值在后。“1”不能省略。例如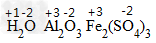 .
.
化合价的一般规律:
(1)化合价有正价和负价;
(2)金属元素跟非金属元素化合时,金属元素显正价,非金属元素显负价,如MgCl2中Mg为+2价,Cl为-1价;非金属元素和氧元素形成化合物时,非金属元素通常显正价,氧元素通常显-2价,如SO2中S为+4价,O为-2价;
(3)一些元素在不同物质中可显不同的化合价,如KMnO4、K2MnO4中锰元素的化合价分别为+7,+6价;
(4)化合物中,各元素正、负化合价代数和为0;
(5)因为化合价是元素的原子在形成化合物时才表现出来的一种性质,所以单质中元素的化合价为0;
(6)原子团不能独立存在,只是化合物的一个组成部分,所以原子团的化合价由各元素的正、负化合价的代数和算出,原子团的化合价一定不为0。
化合价与最外层电子数的关系:
(1)金属元素的化合价数值一般等于它的最外层电子数。
(2)非金属元素的最高正价数值等于它的最外层电子数(O、F除外),最低负价数值等于8减去最外层电子数。
化合价符号与离子符号的比较
一些常见元素和根的化合价:
记忆口诀:
常见元素的化合价口诀
(1)一价钾、钠、银、氢、氟,二价钙、镁、钡和锌,铝价正三氧负二,以上价态要记真。铜一二来铁二三,碳硅二四要记全,硫显负二正四六,负三正五氮和磷,氯价最常显负一,还有正价一五七,锰显正价二四六,最高价数也是七。
(2)常见原子团的化合价口诀
一价铵根氢氧根,另有硝酸氯酸根。二价硫酸碳酸根,勿忘一个锰酸根。三价只有磷酸根。除了铵根皆为负,常写常用能记住。
一种元素一定数目的原子跟其他元素一定数目的原子相化合的性质,叫做这种元素的化合价。化合价有正价、负价之分,如在H2O中,氢原子与氧原子的个数比为2:1,H为+1价,0为-2价;在MgCl2中,镁原子与氯原子的个数比为1:2,Mg为+2价,Cl为-1价。
化合价的意义:
化合价反映元素的原子之间相互化合时的数日,是元素的一种性质。因此,强调化合价时,一定要指明元素。
化合价的表示方法:
通常在元素符一号或原子团的正上方用+n或-n表示,“+”“-”在前,数值在后。“1”不能省略。例如
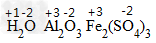 .
.化合价的一般规律:
(1)化合价有正价和负价;
(2)金属元素跟非金属元素化合时,金属元素显正价,非金属元素显负价,如MgCl2中Mg为+2价,Cl为-1价;非金属元素和氧元素形成化合物时,非金属元素通常显正价,氧元素通常显-2价,如SO2中S为+4价,O为-2价;
(3)一些元素在不同物质中可显不同的化合价,如KMnO4、K2MnO4中锰元素的化合价分别为+7,+6价;
(4)化合物中,各元素正、负化合价代数和为0;
(5)因为化合价是元素的原子在形成化合物时才表现出来的一种性质,所以单质中元素的化合价为0;
(6)原子团不能独立存在,只是化合物的一个组成部分,所以原子团的化合价由各元素的正、负化合价的代数和算出,原子团的化合价一定不为0。
化合价与最外层电子数的关系:
(1)金属元素的化合价数值一般等于它的最外层电子数。
(2)非金属元素的最高正价数值等于它的最外层电子数(O、F除外),最低负价数值等于8减去最外层电子数。
化合价符号与离子符号的比较
| 元素化合价的符号 | 离子符号 | |
| 概念不同 | 表示元素原子所显化合价的数值和正负的符号 | 表示带电原子(或原子团)所带电荷的电性核电荷量的符号 |
| 位置不同 | 化合价写在元素符号或原子团的正上方 | 所带电荷写在元素符合(或原子团)的右上角。 |
| 前后不同 | 正负号在前,数字在后 | 数字在前,正负号在后 |
| 省略不同 | 化合价为+1或-1价时,数字1不能省略 | 带一个单位正电荷或负电荷时,“1”不能省略不写 |
一些常见元素和根的化合价:
| 元素和根的名称 | 元素和根的符号 | 常见的化合价 | 元素和根的名称 | 元素和根的符号 | 常见的化合价 |
| 钾 | K | +1 | 氯 | Cl | -1、+1、+5、+7 |
| 钠 | Na | +1 | 溴 | Br | -1 |
| 银 | Ag | +1 | 氧 | O | -2 |
| 钙 | Ca | +2 | 硫 | S | -2、+4、+6 |
| 镁 | Mg | +2 | 碳 | C | +2、+4 |
| 钡 | Ba | +2 | 硅 | Si | +4 |
| 铜 | Cu | +1、+2 | 氮 | N | -3、+2、+3、+4、+5 |
| 铁 | Fe | +2、+3 | 磷 | P | -3、+3、+5 |
| 铝 | Al | +3 | 氢氧根 | OH- | -1 |
| 锰 | Mn | +2、+4、+6、+7 | 硝酸根 | NO3- | -1 |
| 锌 | Zn | +2 | 硫酸根 | SO42- | -2 |
| 氢 | H | +1 | 碳酸根 | CO32- | -2 |
| 氟 | F | -1 | 铵根 | NH4+ | +1 |
记忆口诀:
常见元素的化合价口诀
(1)一价钾、钠、银、氢、氟,二价钙、镁、钡和锌,铝价正三氧负二,以上价态要记真。铜一二来铁二三,碳硅二四要记全,硫显负二正四六,负三正五氮和磷,氯价最常显负一,还有正价一五七,锰显正价二四六,最高价数也是七。
(2)常见原子团的化合价口诀
一价铵根氢氧根,另有硝酸氯酸根。二价硫酸碳酸根,勿忘一个锰酸根。三价只有磷酸根。除了铵根皆为负,常写常用能记住。
发现相似题
与“(1)用化学符号填空:①一个氮分子______;②两个铁原子______...”考查相似的试题有:
- 小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体...
- 小明在实验室里,向盛有一种固态物质的试管中加入一种无色溶液,有气泡产生.试根据学过的知识,推测生成气体可能是哪几种?...
- 按要求填空:(1)下列是某同学书写的错误化学式,请加以改正。锰(MN)改为 ;硫酸钾(KSO4)改为 。(2)用化学符号表示:2个...
- 晓宇同学设计一套制取的氧气的装置(如图所示):回答下列问题:(1)试管中的药品为______.发生反应的化学方程式为______....
- 化学和我们的日常生活息息相关,化学科学的发展促进了人类社会文明的进步,提高了人们的生活质量。 通过化学学习,我们已经认...
- (10分)下表是元素周期表中1—18号元素的排列情况。根据此表我对它进行探究:(1)第16号元素的名称是(10)。通过对元素周期...
- 大海是取之不尽的化工原料宝库,从海水中可提取各项化工原料,下图是工业对海水进行几项综合利用的示意图,根据图示填空:(1...
- 下列物质的化学式书写正确的是( )A.氧化铁[FeO]B.氯化银[AgCl2]C.硫酸钠[NaSO4]D.氢氧化铜[Cu(OH)2]
- 下列示意图形象地表示了A()与B()反应生成C()其反应前后分子及数目的变化,则该反应的化学方程式中,A、B、C的化学计量...
- 根据要求完成下列化学方程式,并在括号中注明基本反应类型.(1)实验室用一种暗紫色固体制取氧气______,(______);(2)...