本试题 “在某温度时,测得纯水中的C(H+)=2.4×10-7mol•L-1,则C(OH-)为( ) A.10-7mol•L-1 B.2.4×10-7mol•L-1 C.1×10-7mol•L-1 D.C(OH-)无法确定” 主要考查您对水电离的影响因素
水的电离平衡
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 水电离的影响因素
- 水的电离平衡
影响水电离平衡的因素:
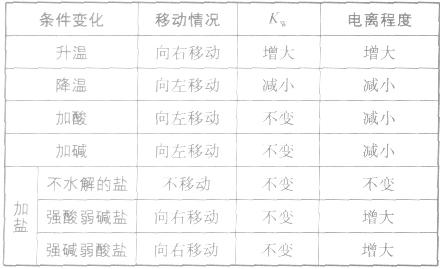
水的电离:
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O
 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L 注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
发现相似题
与“在某温度时,测得纯水中的C(H+)=2.4×10-7mol•L-1,则C(OH-...”考查相似的试题有:
- 100 mL pH=2的两种一元酸x和y,稀释过程中pH与溶液体积的关系如图所示。下列说法正确的是A.稀释前x、y的物质的量浓度相等B...
- 现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。已知:①A、B两溶液呈碱性;C、D、E溶液呈...
- 下列说法正确的是A.根据丁达尔现象可以区分食盐水和硫酸铜溶液B.某离子被沉淀完全是指该离子在溶液中的浓度等于0C.在任何...
- 下列液体均处于25℃,有关叙述正确的是A.无色溶液中:NH、Ag+、PO、Cl—能大量共存B.pH= 4.5的番茄汁中c(H+)是pH= 6.5的牛...
- 向盛有一定量氢氧化钠溶液的烧杯中通入标准状况下448mL氮气和二氧化碳的混合气体后得到溶液A,在溶液A中逐滴加入0.1 mol/L的...
- 纯水在80℃时的pH A.等于7B.大于7C.小于7D.无法确定
- 下图为室温下0.2 mol/L CH3COOH溶液逐滴滴加到25.00 mL 0.1mol/L NaOH溶液中pH的变化曲线,下列说法正确的是:A.若选用甲基...
- 柠檬水中的c (OH-) =10-11mol/L,则其PH是 ( )A. 11B. 7C. 5D. 3
- (1)A、B两种物质都是由H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸性,请找出A、B可能的两...
- 常温下,某溶液中由水电离出的c(OH-) = 1×10-5mol/L,则该溶液中的溶质是A.CH3COONaB.NaOHC.NH3·H2OD.KI