本试题 “下列有关水的叙述正确的是[ ]A.水是一种非电解质B.纯水中c(H+)随着温度的升高而降低C.由液态水结成冰的过程是一个熵增的过程D.25℃,pH相同的氢氧化钠溶液...” 主要考查您对化学反应进行的方向
电解质、非电解质
水电离的影响因素
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应进行的方向
- 电解质、非电解质
- 水电离的影响因素
化学反应的方向与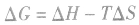 :
:
1.化学反应进行方向的判据
(1)由稳定性弱的物质向稳定性强的物质转变
如 ,稳定性
,稳定性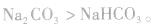
(2)离子反应总是向着使反应体系中某些离子浓度减小的方向进行
①溶解度大的物质向溶解度小的物质转变,如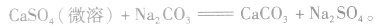
②由相对强酸(碱)向相对弱酸(碱)转变,如 ,
,  所以酸性强弱:
所以酸性强弱: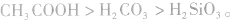
(3)由难挥发性物质向易挥发性物质转变
如 所以沸点:
所以沸点: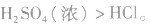
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质转变
如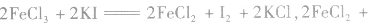
 ,则氧化性:
,则氧化性: 。
。
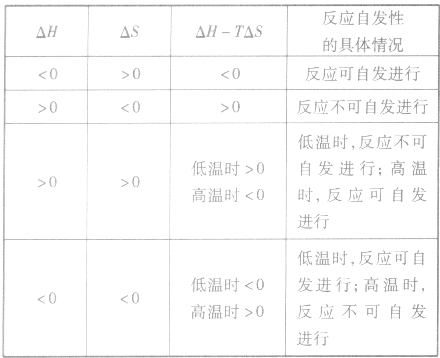
2.焓变和熵变共同判断反应的方向:
在温度、压强一定的条件下,自发反应总是向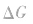
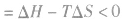 的方向进行,直至达到平衡状态;
的方向进行,直至达到平衡状态;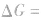
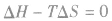 表明反应已达到平衡状态;
表明反应已达到平衡状态;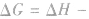
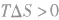 表明反应不能自发进行。
表明反应不能自发进行。
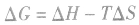 :
:1.化学反应进行方向的判据
(1)由稳定性弱的物质向稳定性强的物质转变
如
 ,稳定性
,稳定性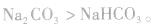
(2)离子反应总是向着使反应体系中某些离子浓度减小的方向进行
①溶解度大的物质向溶解度小的物质转变,如
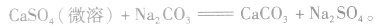
②由相对强酸(碱)向相对弱酸(碱)转变,如
 ,
,  所以酸性强弱:
所以酸性强弱: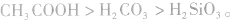
(3)由难挥发性物质向易挥发性物质转变
如
 所以沸点:
所以沸点: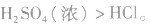
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质转变
如
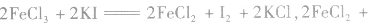
 ,则氧化性:
,则氧化性: 。
。 2.焓变和熵变共同判断反应的方向:
在温度、压强一定的条件下,自发反应总是向
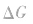
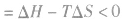 的方向进行,直至达到平衡状态;
的方向进行,直至达到平衡状态;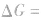
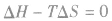 表明反应已达到平衡状态;
表明反应已达到平衡状态;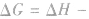
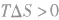 表明反应不能自发进行。
表明反应不能自发进行。
电解质和非电解质:
1.电解质和非电解质在水溶液里或熔融状态下能导电的化合物,叫做电解质。在水溶液里和熔融状态下都不导电的化合物,叫做非电解质。
2.电解质和非电解质的比较

说明(1)电解质、非电解质均是化合物。
(2)电解质导电必须有外界条件:水溶液或熔融状态。
(3)电解质是一定条件下本身电离而导电的化合物。CO2、SO2、SO3、NH3溶于水后也导电,但是与水反应生成的新物质电离而导电的,不是本身电离而导电的,故属于非电解质。
(4)电解质的强弱由物质的内部结构决定,与其溶解度无关。某些难溶于水的化合物,如BaSO4、AgCl,虽然溶解度很小,但溶解的部分是完全电离的,所以是强电解质。
(5)电解质不一定导电,非电解质一定不导电;导电的物质不一定是电解质,不导电的物质不一定是非电解质。
1.电解质和非电解质在水溶液里或熔融状态下能导电的化合物,叫做电解质。在水溶液里和熔融状态下都不导电的化合物,叫做非电解质。
2.电解质和非电解质的比较

说明(1)电解质、非电解质均是化合物。
(2)电解质导电必须有外界条件:水溶液或熔融状态。
(3)电解质是一定条件下本身电离而导电的化合物。CO2、SO2、SO3、NH3溶于水后也导电,但是与水反应生成的新物质电离而导电的,不是本身电离而导电的,故属于非电解质。
(4)电解质的强弱由物质的内部结构决定,与其溶解度无关。某些难溶于水的化合物,如BaSO4、AgCl,虽然溶解度很小,但溶解的部分是完全电离的,所以是强电解质。
(5)电解质不一定导电,非电解质一定不导电;导电的物质不一定是电解质,不导电的物质不一定是非电解质。
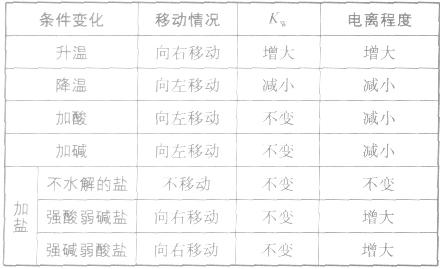
影响水电离平衡的因素:
发现相似题
与“下列有关水的叙述正确的是[ ]A.水是一种非电解质B.纯水中c(...”考查相似的试题有:
- 硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发达水平的一种标志.目前的重要生产方法是“接触法”,有关接触...
- 中学化学教材中有大量数据,下面是某同学对数据的利用情况,其中不正确的是A.利用焓变和熵变的数据可以确定一定温度、压强下...
- 下列说法正确的是[ ]A.食物在常温下腐败是自发进行的B.凡是放热反应都是自发的C.自发反应都是熵增大的反应D.电解池的反应...
- 把0.05mol NaOH固体分别加入到下列100mL液体中,溶液导电性基本不变,该液体为A.自来水B.0.5mol/L HClC.0.5mol/L HAcD....
- 下列物质中:①NaCl ②Na2O ③CH3COOH ④CO2 ⑤NaHCO3 ⑥NH3·H2O ⑦Fe ⑧金刚石 ⑨Cl2 ⑩澄清石灰水 ⑪NaOH 属于强电解质的有 ...
- 向纯水中加入少量的硫酸氢钠(溶液温度不变),则溶液的( )A.pH值升高B.酸性增强C.水的离子积增大D.c(OH-)不变
- 常温下,用0.10 mol·L-1KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混...
- 某学生用0.10 mol/L标准NaOH溶液滴定某浓度的盐酸。记录数据如下:实验序号待测液体积(mL)所消耗NaOH标准液的体积(mL)滴...
- 下列叙述正确的是[ ]A.室温下,pH=9的氨水和pH=9的NaF溶液中,水的电离程度相同B.2SO2(g)+O2(g)2SO3(g)的正、逆反应的平衡...
- 下列说法中不正确的是( ) A.将纯水加热至高温度,水的离子积变大,pH减小,呈中性 B.氨水和盐酸混合后溶液呈酸性,溶液中...