本试题 “下列物质中不能通过置换反应生成的是[ ]A.F2B.COC.Fe3O4D.S” 主要考查您对置换反应
四氧化三铁
单质硫
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 置换反应
- 四氧化三铁
- 单质硫
置换反应:
单质与化合物反应生成另外的单质和化合物的化学反应
发生置换反应的原理:
必须是活动性强的金属置换活动性弱的金属或H+溶液
根据元素性质分类:
1.金属单质置换金属单质:2Al+Fe2O3=高温=Al2O3+2Fe(铝热反应。Al还可与V2O5、CrO3、WO3、MnO2等发生置换);Fe+CuSO4=FeSO4+Cu
2.金属单质置换非金属单质:Zn+2HCl=H2↑+ZnCl2 ;2Na+2H2O=2NaOH+H2↑;2Mg+CO2=点燃=2MgO+C;3Fe+4H2O(g)=高温=Fe3O4+4H2
3.非金属单质置换金属单质:H2+CuO=Δ=Cu+H2O ;C+FeO=Δ=Fe+CO↑
4.非金属单质置换非金属单质:2F2+2H2O=4HF+O2 ;2C+SiO2=Si+2CO↑ ;C+H2O=高温=CO+H2 ;2H2+SiCl4=Si+4HCl ;Cl2+2NaBr=Br2+2NaCl
置换反应与氧化还原反应的关系:
置换反应一定属于氧化还原反应。
四氧化三铁:
又称磁性氧化铁,具有磁性的黑色晶体,不溶于水,具有优良的导电性。
四氧化三铁的性质:
(1)色态:具有磁性的黑色晶体
(2)别名:磁性氧化铁、氧化铁黑、磁铁、磁石、吸铁石、偏铁酸亚铁
(3)矿物:磁铁矿
(4)溶解性:不溶于水,与酸反应生成+2、+3铁盐
(5)稳定性:稳定
(6)还原性:在高温下,易氧化成三氧化二铁。4Fe3O4+O2 6Fe2O3
6Fe2O3
(7)氧化性:在高温下可与还原剂H2、CO、Al、C等反应。 


铁的氧化物:
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗称 | —— | 铁红 | 磁性氧化铁 |
| 色态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 铁的价态 | +2 | +3 | +2、+3 |
| 水溶性 | 不溶 | 不溶 | 不溶 |
| 与酸反应 | FeO+2H+==Fe2++H2O | Fe2O3+6H+==2Fe3++3H2O | Fe3O4+8H+==Fe2++2Fe3++4H2O |
| 用途 | 玻璃色料 | 油漆、颜料 | 做颜料和抛光剂 |
| 氧化性 | 高温时都能与C、CO、H2反应,被还原生成Fe单质 | ||
硫:
硫是一种非金属元素,化学符号是S,原子序数是16。单质硫是一种非常常见的无臭无味的非金属,纯的硫是黄色的晶体,又称作硫磺。
分子结构:硫元素有多种同素异形体 (由同一种元素形成的性质不同的单质)。若将硫的分子式设为 Sx,则x=1,2,3,4,5,6,7,8,9,10,12,18。Sx的分子结构可用如图表示。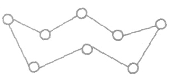
硫的物理性质和化学性质:
(1)物理性质:硫为黄色晶体,俗称硫黄,质脆,易研成粉末。硫的密度比水大,不溶于水,微溶于酒精,易溶于CS。
(2)化学性质:硫位于第3周期ⅥA族,最外层有6个电子,在反应中易得到2个电子而呈-2价;硫的最高正价为+6价;单质硫的化合价为0,处于中间价态,故单质硫既有氧化性又有还原性,在反应中既可作氧化剂又可作还原剂。
如;
①弱氧化性
在加热的条件下,硫黄能被H:和绝大多数的金属单质还原。南于硫的氧化性比较弱,与变价金属反应时往往生成低价态的金属硫化物。例如: 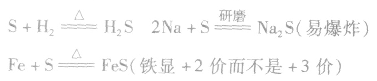

②弱还原性
在一定条件下,硫黄可被F2、O2、Cl2等非金属单质以及一些具有氧化性的化合物氧化,例如:

③硫黄在强碱溶液里加热可发生歧化反应。 (可用热碱液除去试管中残留的硫) 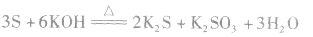
④特性:Hg、Ag在常温下不跟O2反应,但易跟S 反应。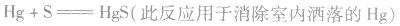
存在与用途:
存在:游离态的硫存在于火山喷口附近或地壳的岩层里,火山喷出物中含有大量含硫化合物,如H2S、 SO2、SO3等。化合态的硫主要以硫化物和硫酸盐的形式存在,如硫铁矿(FeS2)、石膏(CaSO4·2H2O)等。
用途:制H2SO4、黑火药、农药、医药和硫化橡胶。
与“下列物质中不能通过置换反应生成的是[ ]A.F2B.COC.Fe3O4D.S”考查相似的试题有:
- 把某表面被氧化的钢铁样品,加入过量稀H2SO4中,过滤,除去杂质,在滤中滴加KSCN溶液无血红色,继续向滤液中加入适量硝酸后,...
- 某兴趣小组设计如下图实验装置进行实验。Ⅰ、探究大气污染物SO2的性质(1)为了实现绿色环保的目标,能否用上图A2代替A1装置 ...
- 下列说法中正确的是A.漂白粉的有效成分是Ca(CIO)2,应密封保存B.紫色石蕊试液中通入过量二氧化硫气体,溶液将先变红后褪色C...
- 硫与热强碱溶液可生成S2-和SO32-;生成物继续与硫作用得S22-和S2O32-。过滤后除去过量硫,向滤液中加入一定量的强碱后,再适...
- 某研究性学习小组做铜与浓硫酸反应实验时,发现试管底部有白色固体并夹杂有少量黑色物质。倒去试管中的浓硫酸,将剩余固体(含...
- 强热条件下,硫酸亚铁固体发生分解:2FeSO4=Fe2O3+SO2↑+SO3↑,如将此反应生成的气体通入BaCl2溶液中,则( )A.析出BaSO3...
- 50 mL18 mol·L-1硫酸溶液中,加入足量的铜片并加热,被还原的硫酸的物质的量 ( )A.等于0.90 molB.等于0.45 molC.小于0.45...
- A、B、C、D均为中学常见物质且均含有同一种元素,它们之间的部分转化关系如下图所示(反应条件已经略去):。以下推断不正确的...
- 下列叙述正确的是( )A.可用浓硝酸除去铝制品表面的铜镀层B.用催化法处理汽车尾气中的CO和NO:CO+NOC+NO2C.浓硫酸具有吸...
- 在自然界中,化合态的硫存在于下列哪些物质中( )①硫酸盐 ②硫化物 ③火山喷出的气体 ④温泉 ⑤蛋白质A.①②B.①②③C.①②③④D.全部