本试题 “(8分)甲醇是一种可再生能源,具有广泛的开发和应用前景。(1) 工业上一般采用下列两种反应合成甲醇:反应Ⅰ:CO (g)+2H2(g)CH3OH(g) ΔH1反应Ⅱ:CO2(g)+3H2...” 主要考查您对化学反应速率的定义、公式
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应速率的定义、公式
化学反应速率:
1.定义:化学反应速率是用来衡量化学反应进行的快慢程度的物理量。
2.表示方法:在容积不变的反应器中,通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。即: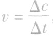
3.单位:mol·L-1·s-1或mol·L-1·min-1等。
4.注意:
(1)化学反应速率是指一段时间内的平均速率,而不是瞬时速率;通常前一段时间的平均反应速率要快于后一段时间的平均反应速率,反应速率均取正值,即v>0。
(2)在一定温度下,固体和纯液体物质单位体积的物质的量保持不变,即物质的量浓度为常数,因此在表示化学反应速率时,不代入固体或纯液体物质的浓度。浓度是指气体或溶液的浓度。
(3)同一个化学反应在相同的条件下、在同一段时间内,用不同物质表示反应速率时,数值可能相同也可能不同,但表达的意义都相同,即反应的快慢程度是一样的。
(4)在同一反应巾用不同的物质来表示反应速率时,其数值之比等于化学方程式中各物质的化学计量数之比.
如化学反应: ,
,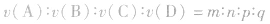 ,所以
,所以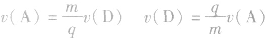
发现相似题
与“(8分)甲醇是一种可再生能源,具有广泛的开发和应用前景。(1...”考查相似的试题有:
- 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:(1)该反应的化学方程式为:______(2...
- (6分)在50mLH2O2水溶液中加入2g二氧化锰,在标准状况下放出气体的体积与时间的关系如右图所示(1)该反应的化学方程式为 。...
- 在2L容器中发生反应N2+3H2⇌2NH3,经一段时间后NH3的物质的量增加了2.4mol,这段时间内用氢气表示的反应速率为0.6mol•L-1•s-1...
- 1913年德国化学家哈伯发明了以低成本制造大量氨的方法,下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是A.①②③B....
- 在2A+B3C+4D反应中,表示该反应速率最快的是 A.υ(A)= 0.5 mol /(L·s) B. υ(B)= 0.3 mol /(L·min)C.υ(C)= 0.8 mol /(L...
- 在25℃时,密闭容器中X、Y、Z三种气体的浓度变化情况如图:下列说法错误的是( )A.反应可表示为3X+Y2ZB.从反应开始到0.4s时...
- (7分)将气体A、B置于容积为2L的密闭容器中,发生如下反应:3A(g) +B(g) 2C(g)+2D(g),反应进行到10s末,测得A的物质的量...
- 对于可逆反应N2+3H2⇌2NH3下列各项所表示的反应速率最快的是( )A.V(N2)=0.01mol/(L•S)B.V(H2)=0.2mol/(L•S)C.V(...
- 甲、乙两个容器内都在进行A→B的反应,甲中每分钟减少4 mol A,乙中每分钟减少2 mol A,则两容器中的反应速率A.甲快B.乙快C...
- 某温度时,在2 L容器中,某一反应中A、B的物质的量随时间变化的曲线如下图所示,由图中数据分析得:(1)在4 min末时,A、B的物质的...