本试题 “铜及铜的化合物有多种应用.请回答下面相关问题:(1)下列两种方法均可以制备CuSO4①2Cu+O2 △ . 2CuO CuO+H2SO4=CuSO4+H2O ②Cu+2H2SO4(浓) △ . CuSO4+SO2↑+...” 主要考查您对氧化还原反应的配平
单质铜
氧化亚铜
氧化铜
氢氧化铜
盖斯定律
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化还原反应的配平
- 单质铜
- 氧化亚铜
- 氧化铜
- 氢氧化铜
- 盖斯定律
配平简介:
化学反应方程式严格遵守质量守恒定律,书写化学反应方程式写出反应物和生成物后,往往左右两边各原子数目不相等,不满足质量守恒定律,这就需要通过配平来解决。
配平原则:
(1)电子守恒原则:反应中还原剂失去电子的总数与氧化剂得到电子的总数相等
(2)电荷守恒原则:若为离子反应,反应前后离子所带正负电荷总数相等
(3)质量守恒原则:反应前后各元素的原子个数相等
配平步骤:
(1)一标:标明反应前后化合价有变化的元素的化合价
(2)二等:通过求最小公倍数使化合价升降总值相等
(3)三定:确定氧化剂与还原剂的化学计量数
氧化剂(还原剂)化学计量数=降(升)价的最小公倍数÷1mol氧化剂(还原剂)降(升)价总数
(4)四平:用观察法配平其他物质的化学计量数
(5)五查:检查质量与电荷、电子是否分别守恒
配平技巧:
(1)逆向配平法:部分氧化还原反应、自身氧化还原反应等可用逆向配平法,即选择氧化产物、还原产物为基准物来配平(一般从反应物很难配平时,可选用逆向配平法)
例:
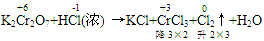
通过表明氧化产物、还原产物化合价的升降,确定CrCl3、Cl2的计量数为2和3,然后再用观察法配平。
(2)设“1”配平法:设某一反应物或生成物(一般选用组成元素较多的物质作基准物)的化学计量数为1,其余各物质的化学计量数可根据原子守恒原理列方程求得。
例:P4O+Cl2→POCl3+P2Cl6
可令P4O前的系数为1,Cl2的系数为x,则
1P4O+xCl2→POCl3+3/2P2Cl6 ,再由Cl原子守恒得2x=3+3/2×6 得x=6 即可配平
(3)零价配平法:先令无法用常规方法确定化合价的物质中各元素均为零价,然后计算出各元素化合价的升降值,并使元素化合价升降总数相等,最后用观察法配平其他物质的化学计量数。
例:Fe3C+HNO3=Fe(NO3)3+CO2↑+NO2↑+H2O
复杂化合物Fe3C按照常规方法分析,无法确定其Fe和C的具体化合价,此时可令组成物质的各元素化合价为零价,根据化合价升降法配平。
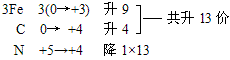
再用观察法确定物质的化学计量数。
(4)整体标价法:当某元素的原子在某化合物中有数个时,可将它作为一个整体对待,根据化合物中元素化合价代数和为零原则予以整体标价。
例:S+Ca(OH)2→CaSx+Ca2S2O3+H2O
生成物CaSx、Ca2S2O3中的Sx、S2作为一个整体标价为-2、+4价,则化合价升降关系为:
Sx 0→-2 降2×2
S2 0→+4 升4×1
即可配平。
(5)缺项配平法:一般先确定氧化剂、还原剂、氧化产物、还原产物的化学计量系数,再通过比较反应物与生成物,确定缺项(一般为H2O、H+或OH-),最后观察配平。
(6)有机氧化还原反应的配平:有机物中元素的化合价一般来讲,氢元素显+1价,氧元素显-2价,然后再根据化合价的代数和为零求酸碳元素的平均化合价。
氧化还原反应方程式配平的一般方法与步骤:
- 一般方法:从左向右配。
- 步骤:标变价,找变化,求总数,配系数。
- 标出元素化合价变化的始态和终态
- 求升价元素或降价元素化合价的变化数
- 求化合价变化数的最小公倍数,分别作为氧化剂或还原剂的系数
- 配平变价元素
- 用观察法配平其他元素
- 检查配平后的方程式是否符合质量守恒定律(离子方程式还要看电荷是否守恒)
如: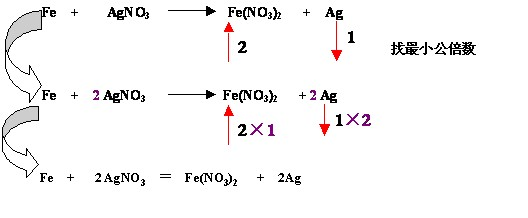
特殊技巧:
配平时若同一物质内既有元素的化合价上升又有元素的化合价下降,若从左向右配平较困难,可以采用从右向左配平,成为逆向配平法。
铜元素:
在元素周期表中的位置:铜的原子序数29,位于周期表中第四周期,第IB族。
(1)物理性质:有金属光泽,紫红色固体,密度较大,导电导热性能很好,具有很好的延展性,铜属于重金属、有色金属、常见金属,不能被磁铁吸引。
(2)化学性质: 铜常见的化合价为+1价和+2价
①在加热条件下,铜可与多种非金属单质反应。一般来说,遇到氧化性较弱的非金属,铜显较低化合价;遇到氧化性较强的非金属,铜显较高化合价。例如:与强氧化剂反应(如Cl2 Br2等)生成+2价铜的化合物。如:
Cu+Cl2 CuCl2 2Cu+O2
CuCl2 2Cu+O2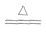 2CuO
2CuO
②铜与酸反应:铜只能被氧化性酸中的中心元素氧化。例如: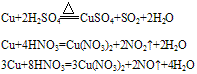
③铜与盐溶液反应:
Cu+2AgCl CuCl2+2Ag
CuCl2+2Ag
铜与铁的对比:
从金属活性顺序表:K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au可知,金属铁的金属活性比铜强,所以单质Fe可以从Cu的溶液中还原出单质来,例如: Fe+CuCl2 FeCl2+Cu
FeCl2+Cu
即Fe的还原性强于Cu
铜与浓硫酸和稀硫酸的反应:
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
2Cu+O2+2H2SO4(稀) 2CuSO4+2H2O
2CuSO4+2H2O
注意:从金属活性顺序表:K Ca Na Mg Al Zn Fe Sn Pb (H)Cu Hg Ag Pt Au 可知,铜不能与稀硫酸发生反应,但是在有氧气和加热的条件下可以反应
铜与铜的化合物之间的转换图: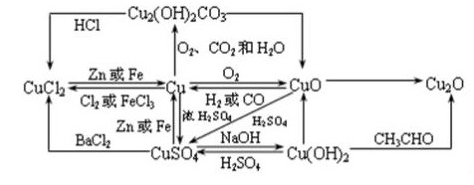
铜的制备和精炼:
(1)工业炼铜法:CuO+CO Cu+CO2
Cu+CO2
(2)湿法炼铜:Fe+CuSO4 FeSO4+Cu
FeSO4+Cu
(3)高温炼铜:工业上用高温冶炼黄铜矿的方法获得铜(粗铜):
2CuFeS2+4O2 Cu2S+3SO2+2FeO(炉渣)
Cu2S+3SO2+2FeO(炉渣)
2Cu2S+3O2 2Cu2O+2SO2
2Cu2O+2SO2
2Cu2O+Cu2S 6Cu+SO2↑
6Cu+SO2↑
备注:粗铜中铜的的含量为99.5%-99.7%,主要含有Ag、Zn、Au等杂质,粗铜通过电解精炼可得到纯度达99.95%-99.98%的铜,原理为用粗铜作阳极,失去电子变为Cu2+,用纯铜棒作阴极即可得精铜。
氧化亚铜:
氧化亚铜为红色或砖红色八面立方晶系结晶性粉末。相对密度6.0,熔点1235℃。在1800℃失去氧。不溶于水和醇,溶于盐酸、氯化铵、氨水,微溶于硝酸。
氧化亚铜的化学性质:
(1)溶于盐酸生成白色氯化亚铜结晶粉末。遇稀硫酸和稀硝酸生成铜盐。在空气中会迅速变蓝。能溶于浓碱、三氯化铁等溶液中。在湿空气中逐渐氧化成黑色氧化铜。
(2)不溶于水及有机溶剂,但可溶于浓氨溶液形成无色配合物[Cu(NH3)2]+,其在空气中被氧化为蓝色的[Cu(NH3)4(H2O)2]2+。氢卤酸反应,因生成络合物,不岐化成二价铜和铜,氧化亚铜氧化亚铜可溶于盐酸生成H[CuCl2](氯化亚铜的配合物),也可溶于硫酸及硝酸分别形成硫酸铜及硝酸铜。
知识点拨:
在酸性溶液中岐化为二价铜,说明在溶液中,二价铜离子的稳定性大于一价铜离子,例如氧化亚铜和硫酸反应,生成硫酸铜和铜。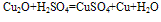
知识扩展:
氧化亚铜有剧毒,氧化亚铜粉尘在空气中含量达到0.22~14mg/m3时,工作1~2h后会引起急性中毒,表现为头痛、无力、咽和结膜发红、恶心、肌肉痛、有时呕吐和腹泻、疲乏、体温升高。一天以后体温可恢复正常,但仍无力,头痛,眩晕,脉数加快,淋巴细胞增多。氧化亚铜的慢性中毒表现为:接触铜化合物的工人的局部皮肤、头发及眼结膜有时变成浅黄色或黑绿色,齿龈上有暗红色或绛红色边。对皮肤有刺激作用,粉尘刺激眼睛,并引起角膜溃疡。对急性中毒者用一定浓度的K4[Fe(CN)6]溶液洗胃,服牛奶等措施。空气中最高容许浓度为0.1mg/m3。可戴口罩、防尘眼镜,穿防护工作服,工作后要洗淋浴。
氧化铜:
(1)物理性质:氧化铜是不溶于水的黑色固体(粉末),能溶于烯酸中,主要用于制造人造丝、陶瓷、釉、电池、杀虫剂,也用于制氢,做催化剂使用。
(2)化学性质:①氧化铜有金属氧化物的性质,常温下能与烯酸反应:CuO+2H+ Cu2++H2O
Cu2++H2O
②氧化铜具有氧化性,加热条件下可以与还原剂发生氧化还原反应:H2+CuO Cu+H2O
Cu+H2O
③氧化铜在高温下可发生分解反应:4CuO 2Cu2O+O2↑
2Cu2O+O2↑
(3)冶炼:一般通过加热分解Cu(OH)2的方式得到CuO,化学方程式为:Cu(OH)2 CuO+H2O
CuO+H2O
注意: 溶液中的Cu2+常为蓝色(浓CuCl2溶液呈绿色,稀CuCl2溶液呈蓝色),其颜色可作为Cu2+的判断依据。Cu2+与碱发生反应生成蓝色沉淀Cu(OH)2,其溶于氨水形成蓝色溶液。
氧化铜的特性:
| 气味 | 无味 |
| 颜色 | 黑色或者棕黑色 |
| 外观 | 无定形或结晶性粉末 |
| 性状 | 稍有吸湿性 |
| 相对质量 | 79.55 |
| 溶解性(水) | 不可溶 |
| 溶解度 | 不溶于水和乙醇,溶于酸、氯化铵及氰化钾溶液,氨溶液中缓慢溶解 |
| 稳定性 | 稳定 |
| 储存 | 密封干燥保存 |
| 用途 | 做有机反应的催化剂,制作人造丝和其他铜化合物等 |
氧化铜和氢氧化铜的性质比较:
名称
氧化铜
氢氧化铜
化学式
CuO
Cu(OH)2
物理性质
不溶水的黑色固体(粉末)
不溶于水的蓝色固体
化学性质
CuO+2H+
 Cu2++H2O
Cu2++H2O
CuO+H2 Cu+H2O
Cu+H2O
CuO+CO Cu+CO2
Cu+CO2Cu(OH)2+2H+  Cu2++2H2O
Cu2++2H2O
Cu(OH)2 CuO+H2O
CuO+H2O
Cu(OH)2+4NH3·H2O Cu(NH3)4(OH)2+4H2O
Cu(NH3)4(OH)2+4H2O
制法
Cu(OH)2
 CuO+H2O
CuO+H2OCu2++2OH-  Cu(OH)2↓
Cu(OH)2↓
例题:铜在自然界存在于多种矿石中,如:黄铜矿(CuFeS2)、斑铜矿(Cu5FeS4)、辉铜矿(Cu2S)、孔雀石(CuCO3·Cu(OH)2
请回答下列问题:
(1)、上表所列铜化合物中,铜的质量百分含量最高的是__Cu2S
)、工业上以黄铜矿为原料。采用火法熔炼工艺生产铜。改工艺的中间过程会发生反应:
2Cu2O+Cu2S 6Cu+SO2↑,反应的氧化剂是Cu2S和Cu2O
6Cu+SO2↑,反应的氧化剂是Cu2S和Cu2O
(3)、二氧化硫尾气直接排放到大气中造成环境污染的后果是形成酸雨,会对植物和建筑物等造成严重危害;该尾气可得到有价值的化学品,写出其中1中酸和1中盐的名称硫酸、硫酸钠。
(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需要进一步采用电解法精制。请简述粗铜电解得到精铜的大批量:以硫酸铜-硫酸溶液为电解质。电解时,粗铜(阳极)中的铜以及比铜活泼的金属失去电子进入溶液,不如铜活泼的金属沉入电解槽形成“阳极泥”;溶液中的Cu2+得到电子沉积在纯铜(阴极)上。
氧化铜与铜化合物之间的转换图:
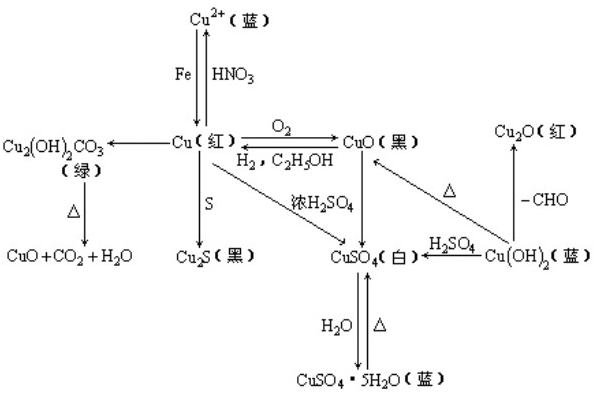
需要记住这些单质、化合物的颜色和状态,可以做为实验题的切入点。
知识扩展:
溶液中的Cu2+常为蓝色(浓CuCl2溶液呈绿色,稀CuCl2溶液呈蓝色),其颜色可作为Cu2+的判断依据。Cu2+与碱发生反应生成蓝色沉淀Cu(OH)2,其溶于氨水形成蓝色溶液。
反应方程为:CuCl2+2NaOH Cu(OH)2↓+2NaCl;Cu(OH)2+4NH3·H2O
Cu(OH)2↓+2NaCl;Cu(OH)2+4NH3·H2O Cu(NH3)4(OH)2+4H2O
Cu(NH3)4(OH)2+4H2O
氢氧化铜:
化学式Cu(OH)2,淡蓝色粉末状晶体,密度3.368g/cm3。难溶于水。受热易分解为氧化铜和水。微显两性,既溶于酸又溶于氨水和浓碱溶液。
氢氧化铜的物理性质和化学性质:
1.物理性质:不溶于水的蓝色固体
2.化学性质:Cu(OH)2+2H+==Cu2++2H2O;Cu(OH)2 CuO+H2O;Cu(OH)2+4NH3·H2O==Cu(NH3)4(OH)2+4H2O
CuO+H2O;Cu(OH)2+4NH3·H2O==Cu(NH3)4(OH)2+4H2O
知识点拨:
溶液中的Cu2+常为蓝色(浓CuCl2溶液呈绿色,稀CuCl2溶液呈蓝色),其颜色可作为Cu2+的判定依据。Cu2+与碱反应生成蓝色沉淀Cu(OH)2, Cu(OH)2溶于氨水形成深蓝色溶液。
不管化学反应是一步完成还是分几步完成,其反应热是相同的。换句话说,化学反应的反应热只与反应的始态和终态有关,而与反应进行的途径无关。如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一一步完成时的反应热是相同的,这就是盖斯定律。
盖斯定律的意义:
利用盖斯定律可以间接计算某些不能直接测得的反应的反应热。例如:
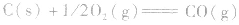 的△H无法直接测得,可以结合下面两个反应的△H,利用盖斯定律进行计算。
的△H无法直接测得,可以结合下面两个反应的△H,利用盖斯定律进行计算。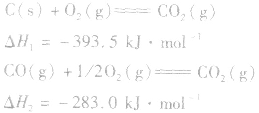
根据盖斯定律,就可以计算出所给反应的△H。分析上述两个反应的关系,即知
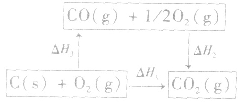
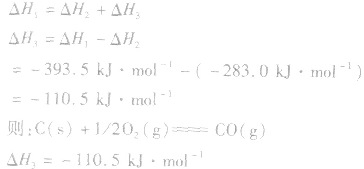
盖斯定律在反应热大小比较中的应用:
1.同一反应生成物状态不同时
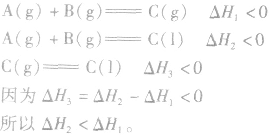
若按以下思路分析:
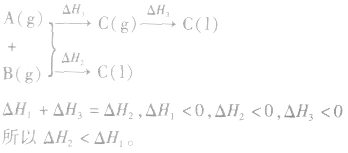
2.同一反应物状态不同时
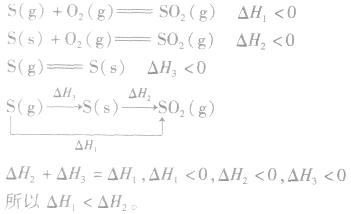
3.两个有联系的不同反应相比
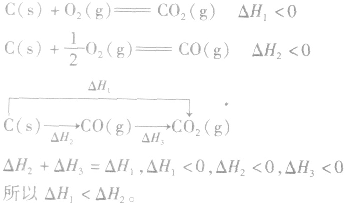
并且据此可写出下面的热化学方程式:

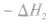
与“铜及铜的化合物有多种应用.请回答下面相关问题:(1)下列两...”考查相似的试题有:
- 若(NH4)2SO4加强热分解的产物是SO2、N2、NH3和H2O,则对该反应的下列说法中正确的是( )A.化学方程式中产物分子的化学计量数...
- 下列反应中,属于有水参加的氧化还原反应,且水只作氧化剂的是( )A.SO2+H2O====H2SO3B.Cl2+H2O====HCl+HClOC.2H2O2H2↑+O...
- 新型无机非金属材料氮化硅是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特点,工业上可用下列方法制取:3SiO2+6C+...
- 已知某混合金属粉末,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合金属粉末中铁、...
- 把以下左栏列举的金属的用途与右栏列举的有关金属的性质用线连起来。①金属可制成比纸还薄的金箔 a.导电性好②生活中用铁锅做...
- 将6g纯铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中充分反应后得到200mL0.5mol/L的FeSO4溶液和5.2g固体,求:(1)反应后生成...
- 根据下列框图分析,下列说法正确的是( )A.E3+的氧化性比M2+的氧化性弱B.在反应①中硫酸既表现了酸性、又表现了氧化性C.反应④...
- 为了除去镀在铝表面的铜镀层,可选用的试剂是( )A.稀硝酸B.浓硝酸C.浓硫酸D.浓盐酸
- 下列各组物质相互反应后,再向得到的溶液中滴入KSCN试剂,溶液变成红色的是A.氯水和氯化亚铁溶液B.铁屑和氯化铜溶液C.铁屑和...
- 将一定量的FeO、Fe2O3、Fe3O4混合粉末与一定量铝粉均匀配成铝热剂并分成两份,第一份在高温下恰好完全反应生成氧化铝和铁,然...