本试题 “t℃时,在两个相同的密闭容器(等容)中分别进行SO2和SO3相互转化的实验,反应的化学方程式为2SO2(g)+O2(g)⇌2SO3(g),实验Ⅰ和实验Ⅱ情况分别为图Ⅰ和图Ⅱ所...” 主要考查您对勒夏特列原理
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 勒夏特列原理
原理内容:
如果改变影响平衡的一个条件(如浓度、压强、温度),平衡将向着能够减弱这种改变的方向移动。勒夏特列原理又叫平衡移动原理。
适用范围:
平衡移动原理适用于化学平衡、溶解平衡、电离平衡、水解平衡等动态平衡。
注意事项:
(1)平衡向“减弱”外界条件变化的方向移动,但不能“抵消”外界条件的变化。
(2)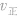 增大并不意味着平衡一定向正反应方向移动,只有
增大并不意味着平衡一定向正反应方向移动,只有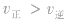 时才可以肯定平衡向正反应方向移动。
时才可以肯定平衡向正反应方向移动。
(3)当平衡向正反应方向移动时,反应物的转化率并不一定提高,生成物的体积分数也并不一定增大(因为反应物或反应混合物的总量增大了),增大一种反应物的浓度会提高另一种反应物的转化率。
(4)存在平衡且平衡发生移动时才能应用平衡移动原理。
分析思路:
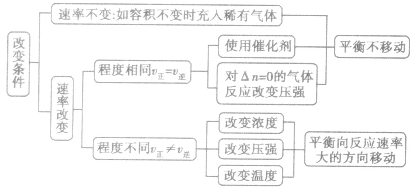
如果改变影响平衡的一个条件(如浓度、压强、温度),平衡将向着能够减弱这种改变的方向移动。勒夏特列原理又叫平衡移动原理。
适用范围:
平衡移动原理适用于化学平衡、溶解平衡、电离平衡、水解平衡等动态平衡。
注意事项:
(1)平衡向“减弱”外界条件变化的方向移动,但不能“抵消”外界条件的变化。
(2)
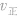 增大并不意味着平衡一定向正反应方向移动,只有
增大并不意味着平衡一定向正反应方向移动,只有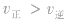 时才可以肯定平衡向正反应方向移动。
时才可以肯定平衡向正反应方向移动。 (3)当平衡向正反应方向移动时,反应物的转化率并不一定提高,生成物的体积分数也并不一定增大(因为反应物或反应混合物的总量增大了),增大一种反应物的浓度会提高另一种反应物的转化率。
(4)存在平衡且平衡发生移动时才能应用平衡移动原理。
分析思路:

发现相似题
与“t℃时,在两个相同的密闭容器(等容)中分别进行SO2和SO3相互...”考查相似的试题有:
- 在一定条件下,使NO和O2在一密闭容器中进行反应,下列说法中正确的是( )A.随着反应的进行,正反应速率逐渐减小,最后不变B...
- 下列表格中的各种情况,可以用下面的图象曲线表示的是( )反应纵坐标甲乙A相同质量的氨,在同一容器中2NH3⇌N2+3H2氨气的转化...
- 对于可逆反应N2(g)+3H2(g)⇌2NH3(g);△H<0,仅改变单一条件后,下列的选项和图示相符的是( ) A.压强对反应的影响 B...
- 我国有丰富的天然气资源.以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):(1)“造合成气”发...
- 同时符合下列两个图象的反应是(温度T1>T2)( )A.N2O3(g)⇌NO2(g)+NO(g);△H>0B.H2(g)+I2(g)⇌2HI(g);△H>0...
- 下列事实不能用勒夏特列原理解释的是[ ]A.氯化铁溶液加热蒸干最终得不到氯化铁固体B.铁在潮湿的空气中容易生锈C.实验室可用排...
- 在200℃时,将amolH2(g)和bmolBr2(g)充入到体积为1L的密闭容器中,发生反应:Br2(g)+H2(g)⇌2HBr(g).(1)反应刚开...
- 下列事实中,不能用勒夏特列原理解释的是[ ]A.对熟石灰的悬浊液加热,悬浊液中固体质量增加B.实验室中常用排饱和食盐水的方...
- 下列事实中,不能用勒夏特列原理解释的是[ ]A.对熟石灰的悬浊液加热,悬浊液中固体质量增加B.实验室中常用排饱和食盐水的方...
- 有关下列图象的说法正确的是( )A.曲线图①可以表示对某化学平衡体系改变温度后反应速率随时间的变化B.根据图②判断,物质A...