本试题 “以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸钠和氧化铁红颜料,原料的综合利用率较高。其主要流程如下(1)反应I前需在溶液中加入_________...” 主要考查您对硫酸盐
工业生产其他物质(工业制备碳酸锂,硫酸钡等化工原理)
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 硫酸盐
- 工业生产其他物质(工业制备碳酸锂,硫酸钡等化工原理)
几种重要的硫酸盐:

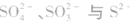 的检验:
的检验:
1.SO42-的检验
(1)原理:利用 ,
,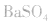 具有不溶于盐酸、硝酸的特性。
具有不溶于盐酸、硝酸的特性。
(2)试剂:可溶性钡盐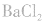 溶液或
溶液或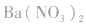 溶液,盐酸和稀硝酸。
溶液,盐酸和稀硝酸。
(3)易出现的错误:
①只加可溶性钡盐,不酸化。误将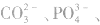 、
、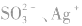 等判成SO42-,此时上述离子会分别产生
等判成SO42-,此时上述离子会分别产生 等白色沉淀.
等白色沉淀.
②先加可溶性盐,后酸化。误将 等判成SO42-,如向待测液中先滴加
等判成SO42-,如向待测液中先滴加 溶液,再加盐酸有白色沉淀生成便断定含SO42-。其错误之处是未注意溶液中不含SO42-而含Ag+或
溶液,再加盐酸有白色沉淀生成便断定含SO42-。其错误之处是未注意溶液中不含SO42-而含Ag+或 也会有同样现象,因为
也会有同样现象,因为
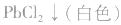
③试剂选择错误。误将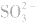 判成
判成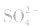 ,如向待测液中滴加盐酸酸化的
,如向待测液中滴加盐酸酸化的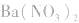 溶液,或滴加硝酸酸化的
溶液,或滴加硝酸酸化的 溶液,生成白色沉淀,使误以为有
溶液,生成白色沉淀,使误以为有 ,错在未注意
,错在未注意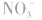 在酸性条件下具有强氧化性,可将
在酸性条件下具有强氧化性,可将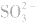 氧化成
氧化成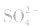 。
。
(4)检验的关键:既要注意试刹的选择,义耍注意操作顺序的优化,全面考虑,综合分析,正确推导,方能排除干扰离子。
(5)最佳检验方法:
2.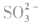 的检验常用气体法:
的检验常用气体法: (不能用硝酸等强氧化性酸),生成能使品红溶液褪色的无色有刺激性气味的气体。
(不能用硝酸等强氧化性酸),生成能使品红溶液褪色的无色有刺激性气味的气体。
3. 的检验
的检验
(1)气体法: ,所用酸必须是非强氧化性酸,可用稀盐酸或稀硫酸,生成能使湿润的醋酸铅试纸变黑的气体。
,所用酸必须是非强氧化性酸,可用稀盐酸或稀硫酸,生成能使湿润的醋酸铅试纸变黑的气体。
(2)沉淀法: ,生成黑色沉淀;或
,生成黑色沉淀;或 ,生成乳白色或黄色沉淀(溶液中)。
,生成乳白色或黄色沉淀(溶液中)。
亚硫酸及亚硫酸盐:
1.亚硫酸溶液中的微粒
SO2与水反应生成亚硫酸,亚硫酸不稳定,易分储成SO2和H2O,因此SO2与H2O的反应是一个可逆反应,用“ ”表示。
”表示。 
在亚硫酸溶液中存在的微粒有(三分子、四离子):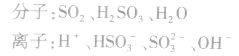
2.亚硫酸的性质
(1)亚硫酸的热稳定性
H2SO3极其不稳定,只能存在于稀的水溶液中。 H2SO3易分解生成SO2和H2O。 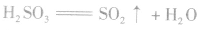
(2)亚硫酸的氧化性和还原性
H2SO3遇到比它更强的氧化剂时,表现还原性。如:
H2SO3遇到比它更强的还原剂时,表现氧化性。如:
(3)亚硫酸的酸性
H2SO3是中强酸,在水溶液中分两步电离: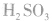
 。
。
由亚硫酸的组成和电离可知,亚硫酸对应的盐有正盐和酸式盐两种,如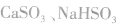 。
。
3.亚硫酸盐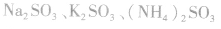 等亚硫酸盐易溶于水、易电离。
等亚硫酸盐易溶于水、易电离。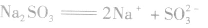

1.确定化工生产的最佳过程
确定化工生产反应原理与过程的一般方法:对于某一具体的化工产品,研究生产过程要从产品的化学组成和性质考虑,来确定原料和生产路线。
①分析产品的化学组成,据此确定生产产品的主要原料;
②分析产品与生产原料之间关键元素的性质,确定主要生产步骤;
③分析生产原料的性质.确定反应原理。
2.选择化工生产的最佳原料
选择原料首先要考虑化学反应原理,此外还要考虑厂址选择、原料供应、能源供应、工业用水供应、产品存储、产品运输、产品预处理成本、环境保护等。
3.控制最佳化学反应条件
控制反应条件是取得化工生产最佳综合效益的重要环节之一。控制反应条件要应用化学反应速率理论和化学平衡原理,结合具体化学反应的特点以及生产技术和设备条件、能源消耗等,控制最佳化学反应速率和反应物的平衡转化率。
4.科学治理工业“三废”
“三废”主要是指废气、废液和废渣。治理“三废” 首先要从设计生产工艺与选择原料做起,即从源头上解决问题;其次是把好排放关,对排出的“三废”的处理,要尽最大努力使其资源化,最低要求是无害化。
5.充分利用“废热”
通过热交换或其他方式利用化学反应所放出的热量。
硫代硫酸钠的工业制法:
(1)亚硫酸钠
将纯碱溶解后,与(硫磺燃烧生成的)二氧化硫作用生成亚硫酸钠,再加入硫磺沸腾反应,经过滤、浓缩、结晶,制得硫代硫酸钠。
Na2CO3+SO2==Na2SO3+CO2 Na2SO3+S+5H2O==Na2S2O3·5H2O
(2)硫化碱法
利用硫化碱蒸发残渣、硫化钡废水中的碳酸钠和硫化钠与硫磺废气中的二氧化硫反应,经吸硫、蒸发、结晶,制得硫代硫酸钠。
2Na2S+Na2CO3+4SO2==3Na2S2O3+CO2
(3)氧化、亚硫酸钠和重结晶法
由含硫化钠、亚硫酸钠和烧碱的液体经加硫、氧化;亚硫酸氢钠经加硫及粗制硫代硫酸钠重结晶三者所得硫代硫酸钠混合、浓缩、结晶,制得硫代硫酸钠。
2Na2S+2S+3O2==2Na2S2O3 Na2SO3+S==Na2S2O3
(4)重结晶法
将粗制硫代硫酸钠晶体溶解(或用粗制硫代硫酸钠溶液),经除杂,浓缩、结晶,制得硫代硫酸钠。
砷碱法净化气体副产 利用焦炉煤气砷碱法脱硫过程中的下脚(含Na2S2O3),经吸滤、浓缩、结晶后,制得硫代硫酸钠。
高锰酸钾的工业制法:
工业上利用二氧化锰制备高锰酸钾,其步骤是
(1)二氧化锰与氢氧化钾共熔并通入氧气:2MnO2+4KOH+O2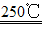 2K2MnO4+2H2O
2K2MnO4+2H2O
(2)电解锰酸钾溶液:2K2MnO4+2H2O 2KMnO4+H2↑+2KOH
2KMnO4+H2↑+2KOH
高锰酸钾常见的制备方法有以下两矿石中取得的二氧化锰和氢氧化钾在空气中或混合硝酸钾(提供氧气)加热,产生锰酸钾,再于碱性溶液中与氧化剂进行电解氧化得到高锰酸钾。 2MnO2+4KOH+O2→2K2MnO4+2H2O 2K2MnO4+Cl2→2KMnO4+2KCl
也可以用MnSO4在酸性环境中和二氧化铅(PbO2)或铋酸钠(NaBiO3)等强氧化剂反应产生。此反应也用于检验二价锰离子的存在,因为高锰酸钾的颜色明显种:
①法一:以MnO2(软锰矿)为原料制KMnO4
第一步:Mn(IV)→Mn(VI) 2MnO2+4KOH+O2====2K2MnO4+2H2O
第二步:CO2歧化K2MnO4 K2MnO4+2CO2====2KMnO4+MnO2+2K2CO3
这种制备方法的最高产率为66.7% 法
②电解法:阳极:2MnO42--2e-→2MnO4- 阴极:2H2O+2e-→H2↑+2OH- 总电解反应方程式为2K2MnO4+2H2O→2KMnO4+2KOH+H2↑
理论产率可达100%
纯硅的制取:
工业上在电炉内,用硅石和碳反应得粗硅和一氧化碳,然后用粗硅和氯气反应得四氯化硅,再用四氯化硅和氢气反应的纯硅和氯化氢,这样就完成硅的制造。(第一步完全相同,第二部有三种方法,工业上用的的是西门子的方法,其他两种不常见。)反应方程式
(1)石英制硅(冶金级),这一步是粗硅制取硅商业上是由高纯度的石英砂和木头,焦炭和煤使用碳棒电极在电弧炉中制得。在高于1900°C的温度下,依照下列方程式碳把石英砂还原成硅: SiO2+C→Si+CO2. SiO2+2C→Si+2CO. 这一过程所的硅称为冶金级硅。纯度为98%-99%。另外,硅制备办法还有熔盐电解法,即电解熔解的二氧化硅。
(2)高纯硅的制备在制备高纯硅之前,需要把粗硅转化成三氯化氢硅(300°C): Si+3HCl→HSiCl3+H2 接着,通过精馏使SiHCl3与其它氯化物分离,经过精馏的SiHCl3,其杂质水平可低于10-10%的电子级硅要求。然后,提纯后的SiHCl3通过CVD原理在1150°C下制备出多晶硅粉。2HSiCl3→Si+2HCl+SiCl4.
与“以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫...”考查相似的试题有:
- 近闻美国和日本正在研究用Na2SO3吸收法作为治理SO2污染的一种新方法。第一步是用Na2SO3溶液吸收SO2生成NaHSO3;第二步是加热...
- 碘化钠是实验室中常用的分析试剂,也常用于医疗和照相业。工业上用铁屑还原法制备NaI,其主要流程如下图,请回答下列问题:(...
- 以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如下:回答下列问题:(1)氧化步骤中发生的主...
- (1)工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体①在步骤a中,还需要通入氧气和水,其目的是_____________________。②...
- 高铁酸钾( K2FeO4)是一种集强氧化性、吸附、絮凝于一体的新型多功能水处理剂,生产工艺如下:已知:①温度较低时:2KOH+Cl2=KC...
- (三选一)【选修2:化学与技术】以磷肥厂排出的废渣磷石膏为原料制硫酸,同时生产水泥,制得的硫酸又用于生产磷肥。硫酸、磷...
- 工业上电解饱和食盐水能制取多种化工原料,其中部分原料可用于制备多晶硅。(1)上图是离子交换膜法电解饱和食盐水示意图,电...
- 高铁酸钾易溶于水,具有强氧化性,是一种新型水处理剂。工业上常用如下方法制备高铁酸钾:以铁丝网为阳极电解溶液,然后在阳...
- 钡盐行业生产中排出大量的钡泥[主要含有BaCO3、BaSiO3、BaSO3、 Ba( FeO2)2等]。某主要生产BaCl2、BaCO3、BaSO4的化工厂利用...
- 我国自行研制的优质磷酸二氢钾(KDP)晶体被应用于大功率固体激光器中。现以氯化钾和磷酸为原料制取磷酸二氢钾,反应方程式为...