本试题 “右图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答:(1)电解水时,将______能转化为化学能.(2)电解一段时间后...” 主要考查您对电解水实验
水的组成
化学反应中的能量变化
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电解水实验
- 水的组成
- 化学反应中的能量变化
电解原理
电解就是将两根金属或碳棒(即电极)放在要分解的物质(电解质)中,然后接上电源,使电流通过液体。化合物的阳离子移到带负电的电极(阴极),阴离子移到带正电的电极(阳极),化合物分为二极。
电解过程
用电使化合物分解的过程就叫电解过程。
水(H2O)被电解生成电解水。电流通过水(H2O)时,氢气在阴极形成,氧气则在阳极形成。带正电荷的离子向阴极移动,溶于水中的矿物质钙、镁、钾、钠……带正电荷的离子,便在阴极形成,就是我们所喝的碱性水;而带负电的离子,在阴极生成。
电解水实验:
1.实验装置图:
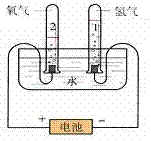
2.表达式:
水 氢气+氧气
氢气+氧气
2H2O 2H2↑+O2↑
2H2↑+O2↑
3.实验现象:
(1)通电后两电极上都有气泡产生;
(2)与电源正极相连接的一端产生的气体比连接负极一端产生的气体少,
接负极一端玻璃管中气体的体积是接正极一端玻璃管内气体体积的2倍。
4.产物检验
(1)正极一端的气体能使带火星的木条复燃,证明气体是氧气。
(2)负极一端的气体能燃烧,并看到微弱的淡蓝色火焰(或听到爆鸣声),
证明气体是氢气。
5.实验结论:
(1)水是由氢元素和氧元素组成的。
(2)1个水分子由2个氢原子和1个氧原子构成。
(3)化学变化中,分子可以再分,原子不可以再分。
6.注意事项:
(1)实验前在水中加入少量的氢氧化钠或者稀硫酸,可增强水的导电性,
加快反应速率。
(2)实验开始时产生的氧气和氢气的体积会小于1:2,是因为氢气难溶于水,
氧气不易溶于水,开始产生的氧气有一部分溶于水,实验时间越长,
其比值越接近1:2。
电解水记忆口诀:
水中通入直流电,正氧负氢会出现;氢二氧一体积比,任何时候都不变。
电解就是将两根金属或碳棒(即电极)放在要分解的物质(电解质)中,然后接上电源,使电流通过液体。化合物的阳离子移到带负电的电极(阴极),阴离子移到带正电的电极(阳极),化合物分为二极。
电解过程
用电使化合物分解的过程就叫电解过程。
水(H2O)被电解生成电解水。电流通过水(H2O)时,氢气在阴极形成,氧气则在阳极形成。带正电荷的离子向阴极移动,溶于水中的矿物质钙、镁、钾、钠……带正电荷的离子,便在阴极形成,就是我们所喝的碱性水;而带负电的离子,在阴极生成。
电解水实验:
1.实验装置图:

2.表达式:
水
 氢气+氧气
氢气+氧气2H2O
 2H2↑+O2↑
2H2↑+O2↑3.实验现象:
(1)通电后两电极上都有气泡产生;
(2)与电源正极相连接的一端产生的气体比连接负极一端产生的气体少,
接负极一端玻璃管中气体的体积是接正极一端玻璃管内气体体积的2倍。
4.产物检验
(1)正极一端的气体能使带火星的木条复燃,证明气体是氧气。
(2)负极一端的气体能燃烧,并看到微弱的淡蓝色火焰(或听到爆鸣声),
证明气体是氢气。
5.实验结论:
(1)水是由氢元素和氧元素组成的。
(2)1个水分子由2个氢原子和1个氧原子构成。
(3)化学变化中,分子可以再分,原子不可以再分。
6.注意事项:
(1)实验前在水中加入少量的氢氧化钠或者稀硫酸,可增强水的导电性,
加快反应速率。
(2)实验开始时产生的氧气和氢气的体积会小于1:2,是因为氢气难溶于水,
氧气不易溶于水,开始产生的氧气有一部分溶于水,实验时间越长,
其比值越接近1:2。
电解水记忆口诀:
水中通入直流电,正氧负氢会出现;氢二氧一体积比,任何时候都不变。
水由氢元素和氧元素组成,电解水实验验证了水的组成;一个水分子由两个氢原子和一个氧原子构成。
定义:
化学反应不仅有物质的变化,还伴随着能量的变化,通常表现为热量变化。有些化学反应会放出热量(称为放热反应),如燃烧、镁和盐酸反应等;也有些反应会吸收热量(称为吸热反应),如碳与二氧化碳反应(C+CO2 2CO)。
2CO)。
常见的吸热反应:
化学上把最终表现为吸收热量的反应叫吸热反应,初中化学所涉及的吸热反应主要有以下几种:
①C+CO2 2CO
2CO
C+2CuO 2Cu+CO2↑
2Cu+CO2↑
CaCO3 CaO+CO2↑
CaO+CO2↑
3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
可见,一般反应条件为高温的反应是吸热反应。
常见的放热反应:
化学上把最终表现为放出热量的反应叫放热反应,初中化学所涉及的放热反应主要有以下几种:
①燃烧:所有燃烧均会放热,如CH4+2O2 CO2+2H2O,H2+Cl2
CO2+2H2O,H2+Cl2 2HCl;
2HCl;
②酸碱中和:酸与碱反应生成盐和水,同时放出热量,如H2SO4+2NaOH==Na2SO4+2H2O
③活拨金属与酸发生置换反应生成H2,同时放出热量,如Mg+2HCl==MgCl2+H2↑,Zn+H2SO4== ZnSO4+H2↑。
④缓慢氧化也是放热反应,如铁生锈、食物腐烂过程中均放出热量。
⑤其他:如双氧水分解是放热反应
人类生活对能量的利用:
①生活燃料的利用:做饭、取暖等;
②利用燃料烧烧产生的能量:发电、制陶瓷、冶炼金属和发射火箭;
③利用爆炸产生的巨大能量:开山炸石、拆除违规建筑;
④食物在体内发生缓慢氧化放出热量,维持体温
化学反应不仅有物质的变化,还伴随着能量的变化,通常表现为热量变化。有些化学反应会放出热量(称为放热反应),如燃烧、镁和盐酸反应等;也有些反应会吸收热量(称为吸热反应),如碳与二氧化碳反应(C+CO2
 2CO)。
2CO)。 常见的吸热反应:
化学上把最终表现为吸收热量的反应叫吸热反应,初中化学所涉及的吸热反应主要有以下几种:
①C+CO2
 2CO
2CO C+2CuO
 2Cu+CO2↑
2Cu+CO2↑ CaCO3
 CaO+CO2↑
CaO+CO2↑ 3CO+Fe2O3
 2Fe+3CO2
2Fe+3CO2 可见,一般反应条件为高温的反应是吸热反应。
常见的放热反应:
化学上把最终表现为放出热量的反应叫放热反应,初中化学所涉及的放热反应主要有以下几种:
①燃烧:所有燃烧均会放热,如CH4+2O2
 CO2+2H2O,H2+Cl2
CO2+2H2O,H2+Cl2 2HCl;
2HCl;②酸碱中和:酸与碱反应生成盐和水,同时放出热量,如H2SO4+2NaOH==Na2SO4+2H2O
③活拨金属与酸发生置换反应生成H2,同时放出热量,如Mg+2HCl==MgCl2+H2↑,Zn+H2SO4== ZnSO4+H2↑。
④缓慢氧化也是放热反应,如铁生锈、食物腐烂过程中均放出热量。
⑤其他:如双氧水分解是放热反应
人类生活对能量的利用:
①生活燃料的利用:做饭、取暖等;
②利用燃料烧烧产生的能量:发电、制陶瓷、冶炼金属和发射火箭;
③利用爆炸产生的巨大能量:开山炸石、拆除违规建筑;
④食物在体内发生缓慢氧化放出热量,维持体温
发现相似题
与“右图所示的是电解水实验装置.通电一段时间后,在两个试管中...”考查相似的试题有:
- 在下列实验操作(或措施)与理由的关系中,正确的是( )A.做电解水实验时,向水中加入少量氢氧化钠溶液--反应加快,因氢氧...
- 下图是电解水的简易装置,下列有关该实验的说法错误的是[ ]A.甲试管内得到的气体是氧气,乙试管内得到的气体是氢气B.电池中...
- 3月22日是“世界水日”,2008年“世界水日”的主题是“涉水卫生”.(1)地球表面约有71%被水覆盖,但可供人类使用的淡水总量却不足...
- 给10%的硫酸溶液通电(实质为电解水,硫酸不发生化学变化)以测定水的组成,下面是小明他们各自实验后获得的数据,你认为其中...
- 地球是太阳系八大行星之中唯一被液态水所覆盖的星球.(1)自然界的水需要经过沉降、______、吸附、消毒等多步净化处理才能成...
- 有关水的实验装置如图所示。(1)图 A 为简易净水装置,其中活性炭的作用是___________ ; 小卵石、石英砂的作用是__________...
- (9分)我们生活在“水球”上,地球表面的70.8%被水覆盖。(1)降雨是自然界中水循环的一个环节。 、 或这些气体在空气中反应后...
- (6分)实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成。请根据电解水实验回答下列问题:(1)通电后电极上出...
- 下列变化过程中吸收热量的是( )A.硝酸铵固体溶于水B.浓硫酸溶于水C.镁与盐酸反应D.生石灰与水反应
- 沼气是当今农村已开发和使用的最洁净的气体燃料之一.(1)沼气的产生和应用过程中发生的能量转化是:生物能→______→热能或光...