本试题 “下列说法正确的是[ ]A.25℃水的电离常数是1.0×10-14B.中性溶液的c(H+)=C.纯水在100℃时,c(H+)>10-7mol·L-1,所以此时纯水中c(H+)>c(OH-)D.pH” 主要考查您对水的电离平衡
溶液的酸碱性
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 水的电离平衡
- 溶液的酸碱性
水的电离:
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O
 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L 注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
溶液的酸碱性:
(1)pH=-lg[c(H+)],在溶液的c(H+)很小时,用pH来表示溶液的酸度。
(2)pH越大,c(H+)越小,c(OH-)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
(3)pH的范围:0~14
(4)溶液酸碱性判断:
当c(H+)>c(OH-)时,溶液呈酸性;
当c(H+)>=c(OH-)时,溶液呈键性;
当c(H+)<c(OH-)时,溶液呈中性。
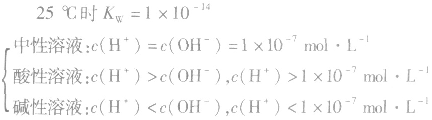
(5)关于pH相同的酸(含强酸和弱酸)
①溶液中c(H+)相等(填“相等”或“不等”)。
②溶液中溶质的物质的量的浓度:强酸<弱酸(填“>”或“<”)。
③耗碱规律:pH和溶液体积均相同的HCl、H2SO4、CH3COOH与碱完全反应时,消耗碱物质的量最多的是CH3COOH。
④稀释规律:分别加水稀释m倍时,溶液的物质的量的浓度均变为原来的1/m,强酸中c(H+)变为原来的1/m,但弱酸中c(H+)减小小于(填“大于”或“小于”)m倍,故稀释后弱酸酸性强于强酸。
(1)pH=-lg[c(H+)],在溶液的c(H+)很小时,用pH来表示溶液的酸度。
(2)pH越大,c(H+)越小,c(OH-)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
(3)pH的范围:0~14
(4)溶液酸碱性判断:
当c(H+)>c(OH-)时,溶液呈酸性;
当c(H+)>=c(OH-)时,溶液呈键性;
当c(H+)<c(OH-)时,溶液呈中性。
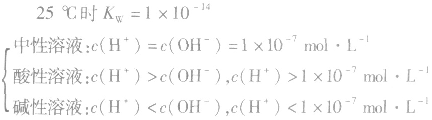
(5)关于pH相同的酸(含强酸和弱酸)
①溶液中c(H+)相等(填“相等”或“不等”)。
②溶液中溶质的物质的量的浓度:强酸<弱酸(填“>”或“<”)。
③耗碱规律:pH和溶液体积均相同的HCl、H2SO4、CH3COOH与碱完全反应时,消耗碱物质的量最多的是CH3COOH。
④稀释规律:分别加水稀释m倍时,溶液的物质的量的浓度均变为原来的1/m,强酸中c(H+)变为原来的1/m,但弱酸中c(H+)减小小于(填“大于”或“小于”)m倍,故稀释后弱酸酸性强于强酸。
溶液的pH:
1.定义:溶液里H+的物质的量浓度的负对数叫做pH。
2.表达式:
3.含义: pH越大,c(H+)越小,c(O-一)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
4.适用范围:
c(H+)很小时,用pH来表示溶液的酸碱度更方便。所以,pH适用于酸、碱的稀溶液
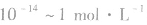 之间],pH取值范刚为0~14。
之间],pH取值范刚为0~14。
5.溶液的酸碱性和pH: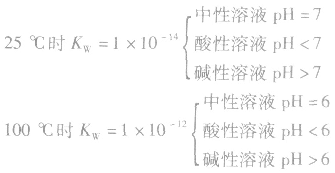
发现相似题
与“下列说法正确的是[ ]A.25℃水的电离常数是1.0×10-14B.中性...”考查相似的试题有:
- 下列关于电解质溶液的叙述正确的是A.常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为、c(Cl-)>c(NH4+)>c(H+)...
- 某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:A.在250mL容量瓶中定容成250mL烧碱溶液;...
- 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:(1)不考虑 其它组的实验...
- 甲溶液的pH是4,乙溶液的pH是5,则甲溶液与乙溶液的c(OH-)之比为A.4∶5B.1∶10C.10∶1D.1∶2
- 已知:常温下,A酸的溶液pH=a,B碱的溶液pH=b。(1)若A为盐酸,B为氢氧化钡,且a=3,b=11,两者等体积混合,溶液的pH为 。...
- 25℃时,KW=1.0×10-14;100℃时,KW=5.5×10-13。下列说法正确的是 ( )A.100℃时,pH=12的NaOH溶液和pH=2的H2SO4恰好中和,...
- 下列叙述正确的是( )A.95℃纯水的pH
- 下列水溶液一定呈中性的是( )A.c(NH4+)=c(Cl-)的NH4Cl溶液B.c(H+)=1.0×10-7mol·L-1的溶液C.pH=7的溶液D.室温下将p...
- pH值为4的FeCl3溶液和pH值为10的K2CO3溶液中,水的电离度分别为α1和α2,则它们的大小关系是( )A.α1>α2B.α1<α2C.α1=α2D...
- 常温下某强酸溶液pH=b,某强碱溶液的pH=a,已知a+b=12,酸碱溶液混合后pH=7,则酸溶液的体积V酸和碱溶液的体积V碱的正确关系...