本试题 “I、今有①CH3COOH、②HCl、③H2SO4三种溶液,选择序号填空:A.①>②>③ B.①<②<③ C.①=②=③ D.①=③>②E.①>②=③ F.①<②=③ G.①=②<③ H.①=②>③(1)当...” 主要考查您对强酸和弱酸的比较
水的电离平衡
溶液的酸碱性
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 强酸和弱酸的比较
- 水的电离平衡
- 溶液的酸碱性
强酸与弱酸(或强碱与弱碱)的比较:
1.强酸与弱酸(或强碱与弱碱)由于电离程度的不同,在很多方面表现出不同的性质 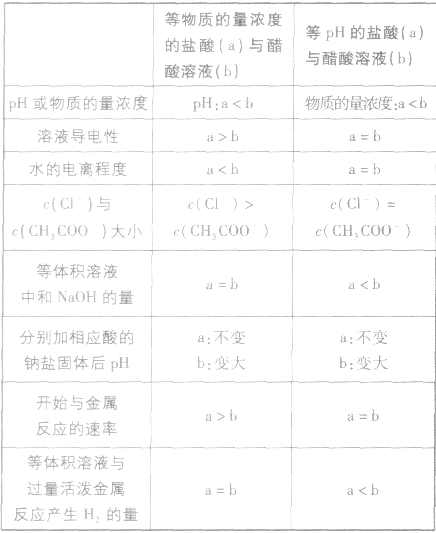
2.稀释时pH变化特点比较如下图:a、b分别为体积相等、pH相等的NaOH溶液和氨水的稀释曲线线;c、d分别为体积相等、pH相等的盐酸和醋酸溶液的稀释曲线,请体会图中的两层含义: 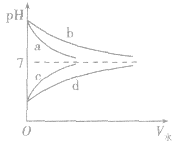
(1)加水稀释相同倍数后的pH大小:氨水>NaOH溶液,盐酸>醋酸溶液。若稀释10n倍,盐酸、Na0H溶液pH变化n个单位,而氨水与醋酸溶液pH变化小到 n个单位。
(2)稀释后的pH仍然相等,则加水量的大小:氨水 >NaOH溶液,醋酸溶液>盐酸。
水的电离:
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O
 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L 注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
溶液的酸碱性:
(1)pH=-lg[c(H+)],在溶液的c(H+)很小时,用pH来表示溶液的酸度。
(2)pH越大,c(H+)越小,c(OH-)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
(3)pH的范围:0~14
(4)溶液酸碱性判断:
当c(H+)>c(OH-)时,溶液呈酸性;
当c(H+)>=c(OH-)时,溶液呈键性;
当c(H+)<c(OH-)时,溶液呈中性。
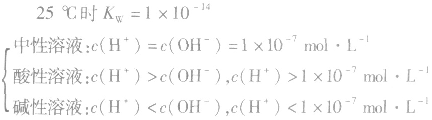
(5)关于pH相同的酸(含强酸和弱酸)
①溶液中c(H+)相等(填“相等”或“不等”)。
②溶液中溶质的物质的量的浓度:强酸<弱酸(填“>”或“<”)。
③耗碱规律:pH和溶液体积均相同的HCl、H2SO4、CH3COOH与碱完全反应时,消耗碱物质的量最多的是CH3COOH。
④稀释规律:分别加水稀释m倍时,溶液的物质的量的浓度均变为原来的1/m,强酸中c(H+)变为原来的1/m,但弱酸中c(H+)减小小于(填“大于”或“小于”)m倍,故稀释后弱酸酸性强于强酸。
(1)pH=-lg[c(H+)],在溶液的c(H+)很小时,用pH来表示溶液的酸度。
(2)pH越大,c(H+)越小,c(OH-)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
(3)pH的范围:0~14
(4)溶液酸碱性判断:
当c(H+)>c(OH-)时,溶液呈酸性;
当c(H+)>=c(OH-)时,溶液呈键性;
当c(H+)<c(OH-)时,溶液呈中性。
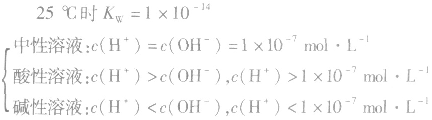
(5)关于pH相同的酸(含强酸和弱酸)
①溶液中c(H+)相等(填“相等”或“不等”)。
②溶液中溶质的物质的量的浓度:强酸<弱酸(填“>”或“<”)。
③耗碱规律:pH和溶液体积均相同的HCl、H2SO4、CH3COOH与碱完全反应时,消耗碱物质的量最多的是CH3COOH。
④稀释规律:分别加水稀释m倍时,溶液的物质的量的浓度均变为原来的1/m,强酸中c(H+)变为原来的1/m,但弱酸中c(H+)减小小于(填“大于”或“小于”)m倍,故稀释后弱酸酸性强于强酸。
溶液的pH:
1.定义:溶液里H+的物质的量浓度的负对数叫做pH。
2.表达式:
3.含义: pH越大,c(H+)越小,c(O-一)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
4.适用范围:
c(H+)很小时,用pH来表示溶液的酸碱度更方便。所以,pH适用于酸、碱的稀溶液
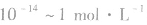 之间],pH取值范刚为0~14。
之间],pH取值范刚为0~14。
5.溶液的酸碱性和pH: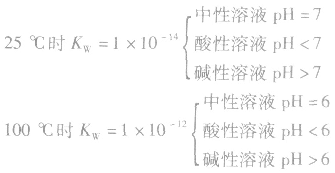
发现相似题
与“I、今有①CH3COOH、②HCl、③H2SO4三种溶液,选择序号填空:A.①...”考查相似的试题有:
- 某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA-H++A2-。现有下列四种溶液:① 0.01mol・L1的H2A溶液② 0.01mol・L1的NaHA...
- 将1mL pH值相同的醋酸和盐酸,分别用蒸馏水稀释到l00 mL,稀释后两溶液的pH 分别为m和n ( )A m>n B m=n C m<n D 不能确定
- 25 ℃时,下列各溶液中,粒子的物质的量浓度关系不正确的是( )A.0.1 mol/L NH4Cl溶液中加入NH3·H2O 至呈中性时:c(NH4+)=...
- 有甲、乙两种溶液,甲溶液的pH是乙溶液pH的2倍,则甲、乙两溶液中的C(H+)A 2:1 B 100:1 C 1:100 D 无法确定
- 下列说法正确的是( )A.水的电离方程式:H2OH++OH-B.升高温度,水的电离程度增大C.在NaOH溶液中没有H+D.在HCl溶液中没有OH-
- 等体积等浓度的MOH强碱溶液和HA弱酸溶液混和后,混和液中有关离子的浓度应满足的关系是A.c(M+)>c( OH―)> c(A-)>c(H+)B...
- 下列说法正确的是( )A.某盐的水溶液呈酸性,该盐一定是强酸弱碱盐B.强电解质溶液稀释后,溶液中各种离子浓度一定都减少C...
- pH=3的两种一元酸HX和HY溶液,分别取50mL加入足量的镁粉,充分反应后,收集到H2的体积分别为V(HX)和V(HY),若V(HX)>V...
- 关于下列各图的叙述,正确的是[ ]A.甲表示1mol H2(g)完全燃烧生成水蒸气吸收241.8 kJ热量B.甲表示2 mol H2(g)所具有的能量...
- 有人曾建议用AG表示溶液的酸度(acidity),AG的定义为AG=lg下列表述不正确的是[ ]A.在25℃时,若溶液呈中性,则pH=7,AG=1B...