本试题 “以黄铁矿为原料生产硫酸的工艺流程图如下(1)将燃烧黄铁矿的化学方程式补充完整4_______+11O22Fe2O3+8SO2(2)接触室中发生反应的化学方程式是_____________...” 主要考查您对二氧化硫
热化学方程式
工业制硫酸
金属、非金属的有关计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 二氧化硫
- 热化学方程式
- 工业制硫酸
- 金属、非金属的有关计算
①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:


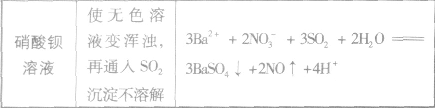
SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表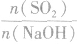 ,如下数轴所示:
,如下数轴所示: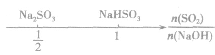
分析数轴可得:
(1)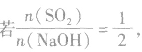 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2)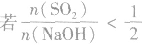 ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3)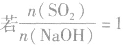 ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4)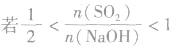 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5)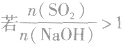 ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。
二氧化硫的制备:
工业制法:

实验室制法:
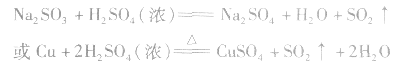
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

1.定义表示反应所放出或吸收热量的化学方程式,叫做热化学方程式。
2.表示意义不仅表明了化学反应中的物质变化,也表明厂化学反应中的能量变化。例如:
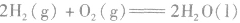 :
: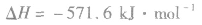 ,表示在25℃、101kPa下,2molH2(g)和1mol O2(g)完全反应生成2molH2O(l)时要释放571.6kJ 的能量。
,表示在25℃、101kPa下,2molH2(g)和1mol O2(g)完全反应生成2molH2O(l)时要释放571.6kJ 的能量。热化学反应方程式的书写:
热化学方程式与普通化学方程式相比,在书写时除厂要遵守书写化学方程式的要求外还应注意以下问题:
1.注意△H的符号和单位 △H只能写在标有反应物和生成物状态的化学方程式的右边。若为放热反应,△H为“-”;若为吸热反应,△H为“+”。△H的单位一般为kJ/moJ。
2.注意反应条件反衄热△H与测定条件(温度、压强等)有关。因此书写热化学方程式时应注明△H的测定条件。绝大多数△H是是25℃、101kPa下测定的,此条件下进行的反应可不注明温度和压强。
3.注意物质的聚集状态反应物和生成物的聚集状态不同,反应热△H不同。因此,必须注明物质的聚集状态才能完整地体现出热化学方程式的意义。气体用“g”,液体用:l“,固体用“s”,溶液用“aq”。
4.注意热化学方程式的化学计量数
(1)热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物质的量,并不表示物质的分子数或原子数,因此化学计量数可以是整数,也可以是分数。
(2)热化学方程式中的反应热表示反应已完成时的热量变化,由于△H与反应完成的量有关,所以方程式中化学式前面的化学计量数必须与△H相对应,如果化学计量数加倍,则△H也要加倍。当反应逆向进行时,其反应热与正反应的反应热数值相等,符号相反。
工业制硫酸的方法:
(1)硫铁矿制酸硫铁矿在沸腾焙烧炉内通空气燃烧产生SO2气体,经余热锅炉回收热量后,依次通过旋风除尘和电除尘进行干法除尘。随后,炉气再通过洗涤、冷却、除雾等一系列的净化操作进入干燥塔。干燥后的炉气用主鼓风机压送至一转一吸或两转两吸制酸装置内制取硫酸。其反应如下: 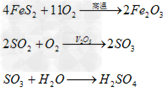
(2)硫磺制酸反应时生成的热传递给进入接触室的需要预热的浓和气体并冷却反应后生成的气体(即热交换过程)熔融硫磺在焚硫炉内用干燥空气燃烧产生SO2气体,经余热锅炉回收燃烧热后进入“一转一吸”或“两转两吸”制酸系统制取硫酸。其反应如下: 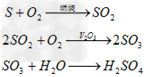
(3)冶炼烟气制酸主要利用有色金属铜、铅、锌、镍、钴等硫化矿在熔炼过程中产生的SO2烟气进行制酸。
其工艺流程除焙烧系统随有色金属硫化矿的焙烧工艺不同而有异外,其制酸工艺与沸腾炉炉气制酸相同。
硫酸的生产流程:
(1)原料工段原料处理能力要满足生产周转,与硫酸生产能力相匹配,能够满足焙烧工艺的进料工况条件结合矿源及工程,应着重考虑如下问题原料的卸车及转运方式、矿库的贮存能力(库容)、干燥及含尘尾气处理、块矿的破碎及筛分等。原料工段设置应尽量少进行固体物料的交叉,流程越简单越好。
(2)焙烧流程焙烧流程一般为:焙烧炉—废热锅炉—旋风除尘器—电除尘器,也可以不设旋风除尘器。这种流程非常紧凑,但电除尘器需专门设计且操作管理要求较高。为了尽可能使工艺技术和设备制造立足国内,增加装置操作的可靠性,使用国内的电除尘器,则倾向于设置旋风除尘器。一般采用增湿输送的干法排渣,有刮板输送机—冷却滚筒(增湿)一带式输送机流程和冷却滚筒+冷却滚筒(增湿)—带式输送机两种流程,目前设计倾向于使用后一种流程。
(3)净化流程大型硫酸装置选择酸洗净化流程。国内大型装置空塔流程居多,即空塔(增湿塔)—填料冷却塔(稀酸板式换热器)一两级电除雾器。近十多年来我国投产的硫铁矿制酸酸洗净化流程绝大多数使用此流程,亦是比较容易掌握的流程。近年来冶炼烟气制酸选择动力波洗涤器代替空塔居多,国内有关专家认为,动力波洗涤器特别适用于烟气量波动比较大的情况,效果较好,但压降较大,对气量均衡稳定的硫铁矿制酸并无明显优势。
(4)干吸流程干吸流程有塔槽一体化流程、三塔一槽流程、三塔两槽流程和三塔三槽流程。塔槽一体化即干燥塔、一吸塔、二吸塔均不设外部泵槽,由各塔的底部分别存液,循环泵设于塔外的管道上,国内比较典型的为贵州瓮福2×400kt/a硫铁矿制酸装置。塔槽一体化省去了泵槽和很多的管线,使得工艺流程简单、设备布置紧凑,有一定的优越性,但在设计时要考虑泵的密封,特别是一吸循环泵。目前,国内设计多采用三塔两槽流程,又以干燥塔一个循环槽.两吸收塔共用一个循环槽居多。干吸塔普遍使用不锈钢槽管式分酸器及大规格填料,可大幅增加分酸点,降低填料高度,优化塔的操作状况,提高塔的操作效率,塔的顶部装设高效除雾器。
(5)转化流程转化工序基本采用两转两吸流程,国内“2+2”,“3+2”,“3+1”几种流程都有,但目前采用较多的是,“3+1”流程,配套换热流程有ⅢⅠ—ⅣⅡ和ⅣⅠ—ⅢⅡ等,设计选择较多的ⅢⅠ—ⅣⅡ根据系统热平衡计算,可以考虑设置热管省煤器。转化系统的流程和设计参数的选择,实际上是系统的优化问题,需与所用催化剂和所用设备情况综合考虑,应尽量提高一转化的转化率,使尾气排放更容易达到日益严格的环保要求。
(6)生产硫酸流程图
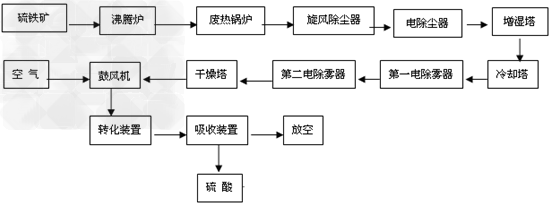
包括金属及化合物、金属与非金属化合物、非金属化合物之间的反应的计算,解此类题的关键是正确的写出反应方程式,明确物质间的等量关系。明确物质之间的反应,正确写出方程式,此类题可迎刃而解。
AlCl3与NaOH反应的相关计算:
1、求Al(OH)3沉淀的量
2、求反应物碱的量
铝与酸、碱反应的计算规律:
铝分别与盐酸、氢氧化钠溶液反应的原理: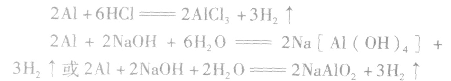
(1)等量铝分别与足量盐酸和氢氧化钠溶液反应,产生氢气的体积比为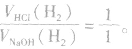
(2)足量的锅分别与等物质的量的盐酸和氢氧化钠溶液反应,产生氢气的体积比为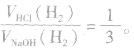
(3)一定量的铝分别和一定量的盐酸和氢氧化钠溶液反应,若产生氢气的体积比为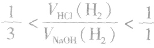 ,则必定是:
,则必定是:
①铝与盐酸反应时,铝过量而盐酸不足;
②铝与氢氧化钠溶液反应时,铝不足而氢氧化钠过量。
解有关硝酸与金属反应的计算题的技巧:
1.灵活运用得失电子守恒、原子守恒及溶液中的电荷守恒关系例如Cu与HNO3反应中就有以下等量关系:
(1)N原子守恒:反应前所有的N只存在于HNO3中;反应后含N的物质有HNO3的还原产物(假设此处有NO3、NO)和Cu(NO3)3,若HNO3过量,则过量HNO3中也含一部分N,则有:n(N)=n(NO2)+ n(NO)+2n[Cu(NO3)3]+n剩(HNO3)。
(2)得失电子守恒:在反应中失去电子的是参加反应的Cu, ;得到电子的是被还原的HNO3(假设还原产物为NO2、NO),NO3-+e→ NO2、NO3-+3e→NO。根据得失电子守恒,则有:
;得到电子的是被还原的HNO3(假设还原产物为NO2、NO),NO3-+e→ NO2、NO3-+3e→NO。根据得失电子守恒,则有: 
(3)溶液中的电荷守恒:在任何溶液中,阴离子所带负电荷总数与阳离子所带正电荷总数在数值上是相等的。在Cu与HNO3反应后的溶液中,若HNO3不过量,阳离子只有Cu2+,阴离子只有NO3-(此类计算不考虑H2O电离出的极少量的H+、OH-);若HNO3过量,溶液中阳离子有Cu2+和H+,阴离子只有NO3-。则有:
①若HNO3不过量: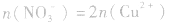
②若HNO3过量: 
2.铁与稀HNO3的反应规律 

(2)上述反应可以认为先发生反应①,若Fe有剩余则发生 ①×2+ ③即得反应②,所以,无论是反应①还是反应②,被还原的HNO3皆占参加反应的HNO3的
①×2+ ③即得反应②,所以,无论是反应①还是反应②,被还原的HNO3皆占参加反应的HNO3的 。
。
有关镁、铝的图像集锦:
Al(OH)3与Al3+、AlO2-之间的转化,是建立在 Al(OH)3两性基础上的,有关相互转化的配比和沉淀Al(OH)3的质量变化,见下表:
与“以黄铁矿为原料生产硫酸的工艺流程图如下(1)将燃烧黄铁矿的...”考查相似的试题有:
- 含有SiO2的黄铁矿(FeS2)试样1克,在O2中充分灼烧后残余固体为0.76克,则该黄铁矿的纯度为________%;用这种黄铁矿100吨可制...
- (17分)在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀。然后加入适...
- 下列有关说法,错误的是[ ]A.氮氧化物、二氧化硫都是形成酸雨的主要物质B.工业合成氨及用NH3制化肥(NH4)2SO4都属于氮的固定...
- 乙醇是一种重要的化工原料。(1)葡萄糖在酒化酶的作用下转化为乙醇的化学方程式是__________________。(2)常温常压下,23g乙醇...
- A、B、C、D和甲有以下转化关系。已知物质甲是短周期元素组成的盐,且是某种消毒液的有效成分,沉淀D可溶于酸。请回答下列问题...
- 将铁和氧化铁的混合物15g加入150mL稀硫酸中,在标准状况下放出氢气1.68L,同时铁和氧化铁均无剩余,向溶液中滴加硫氰化钾溶...
- 将铜片放入0.1mol/LFeCl3溶液中,反应一定时间后取出铜片,溶液中c(Fe3+):c(Fe2+)=2:3,则Cu2+与Fe3+的物质的量之比为[ ]A...
- 取两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,同温同压下放出相同体积的气体,则两份铝片的质量之比为[ ]A...
- 一定条件下磷与干燥氯气反应,若0.25g磷消耗掉314mL氯气(标准状况),则产物中PCl3与PCl5的物质的量之比接近于[ ]A.1:2B...
- 某金属的可溶性硫酸盐和碳酸盐2.48g,与过量氯化钡溶液反应,生成4.3g沉淀,将沉淀洗净后,放入过量稀硫酸中,除有无色气体产生外,...