本试题 “已知下面三个数据:7.2×10-4、4.6×10-4、4.9 ×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2===HCN+NaNO2NaCN+HF===HCN...” 主要考查您对电离平衡常数
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电离平衡常数
电离平衡常数:
1.概念在一定条件下,弱电解质的电离达到平衡时,溶液中电离所生成的各种离子浓度的乘积与溶液中未电离的分子浓度的比是一个常数,这个常数叫做电离平衡常数,简称电离常数。用K表示(酸用 表示,碱用
表示,碱用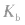 表示)。
表示)。
2.表示方法: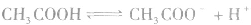
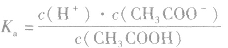
对于多元弱酸,其电离是分步进行的,每步各有电离常数,通常用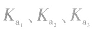 ,等分别表示,且
,等分别表示,且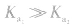
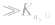
例如: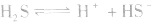
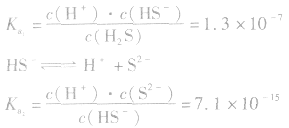
3.影响因素:温度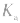 (或
(或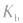 )只随温度变化而变化,不随浓度变化而变化。电离平衡常数,类似于化学平衡常数.
)只随温度变化而变化,不随浓度变化而变化。电离平衡常数,类似于化学平衡常数.
4.意义:反映弱酸,弱碱酸碱性的相对强弱在一定温度下, 越大(多元弱酸以
越大(多元弱酸以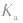 为依据),弱酸的电离程度就越大,浓度相同时c(H+)也越大,弱酸的酸性越强。
为依据),弱酸的电离程度就越大,浓度相同时c(H+)也越大,弱酸的酸性越强。
1.概念在一定条件下,弱电解质的电离达到平衡时,溶液中电离所生成的各种离子浓度的乘积与溶液中未电离的分子浓度的比是一个常数,这个常数叫做电离平衡常数,简称电离常数。用K表示(酸用
 表示,碱用
表示,碱用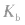 表示)。
表示)。 2.表示方法:
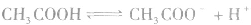
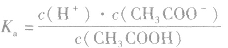
对于多元弱酸,其电离是分步进行的,每步各有电离常数,通常用
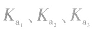 ,等分别表示,且
,等分别表示,且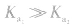
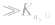
例如:
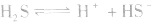
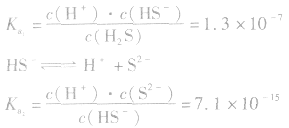
3.影响因素:温度
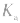 (或
(或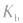 )只随温度变化而变化,不随浓度变化而变化。电离平衡常数,类似于化学平衡常数.
)只随温度变化而变化,不随浓度变化而变化。电离平衡常数,类似于化学平衡常数.4.意义:反映弱酸,弱碱酸碱性的相对强弱在一定温度下,
 越大(多元弱酸以
越大(多元弱酸以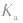 为依据),弱酸的电离程度就越大,浓度相同时c(H+)也越大,弱酸的酸性越强。
为依据),弱酸的电离程度就越大,浓度相同时c(H+)也越大,弱酸的酸性越强。 发现相似题
与“已知下面三个数据:7.2×10-4、4.6×10-4、4.9 ×10-10分别是...”考查相似的试题有:
- 已知:①25℃时弱电解质电离平衡数:Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Ksp(CaF2)=1.5×1...
- ⑴完全中和100mL PH=3的醋酸溶液和1L PH=4的醋酸溶液,需要等物质的量浓度的NaOH溶液的体积分别为V1和V2,则V1 V2。(填“>”、“
- 用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是[ ]A.B.C.c(H+)和c(OH-)的乘积D.OH-的物质的量
- 以水为溶剂进行中和滴定的原理是:H3O++OH-=2H2O。已知液态SO2和纯水的导电性相近,因为液态SO2也会发生自离解:SO2(l)+SO2(l...
- 运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。若在恒温、恒压条件下向平衡体系中通入氯气,平衡_________移...
- 常温下,将0.05mol/L盐酸溶液和未知浓度的NaOH溶液以1:2的体积比混合,所得溶液的pH=12。用上述NaOH溶液13 ml和pH=3的某一...
- 25℃时,有0.01 mol/L的醋酸溶液,醋酸的电离平衡常数表达式_______________________达平衡时,溶液中氢离子浓度是__________...
- 下列化学用语书写正确的是[ ]A.次氯酸的电离方程式:HClOH++ ClO-B.铝溶于烧碱溶液的离子方程式:Al+ 2OH-= AlO2-+H2↑C.电...
- 关于水的离子积常数Kw与水的电离平衡常数Kc的叙述中,正确的是[ ]A.Kw和Kc都随温度的升高而增大B.Kw和Kc数值不同,但单位相...
- 化学平衡常数(K)、电离常数( Ka)、溶度积常数(Ksp)是判断物质性质或变化的重要的常数。下列关于这些常数的说法中,正确的是[ ...