本试题 “现有浓度均为0.1 mol/L的下列溶液:①硫酸 ②醋酸 ③氢氧化钠④氯化铵 ⑤醋酸铵 ⑥硫酸铵 ⑦硫酸氢铵 ⑧氨水,请回答下列问题:(1)①②③④四种溶液中由水电离出的H+浓...” 主要考查您对水的离子积常数
水电离的影响因素
水的电离平衡
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 水的离子积常数
- 水电离的影响因素
- 水的电离平衡
水的电离:
水是一种极弱的电解质,它能微弱地电离:
实验测得:25℃时,1L纯水中只有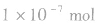 的水分子发生电离,故25℃时纯水中
的水分子发生电离,故25℃时纯水中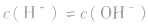

水的离子积:
在一定温度下,水电离出的c(H+)与c(OH-)的乘积是一个常数,称为水的离子积常数,简称水的离子积,用符号 表示,即
表示,即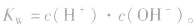
(1)在一定温度下,水的离子积都是一个常数,在25℃时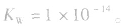
(2)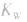 随温度的变化而变化,温度升高,
随温度的变化而变化,温度升高,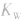 增大。
增大。
(3)水的离子积常数揭示了在任何水溶液中均存在水的电离平衡,都有 存在。在酸性或碱性的稀溶液中,当温度为25℃时,
存在。在酸性或碱性的稀溶液中,当温度为25℃时,
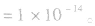
(4)在酸或碱的稀溶液中,由水电离出的c(H+)和c(OH-)总相等.即 如25℃时
如25℃时 或NaOH溶液中,
或NaOH溶液中,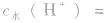
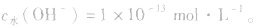
溶液中c(H+)或c(OH-)的计算:
常温下,稀溶液中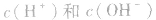 的乘积总是
的乘积总是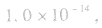 知道
知道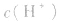 就可以计算出
就可以计算出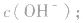 反之亦然
反之亦然
1.酸溶液
当在水中加入酸后,将使水的电离平衡向左移动 (抑制水的电离)。在酸的水溶液中,H+主要由酸电离产生,即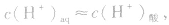 而OH-是由水电离产生的:
而OH-是由水电离产生的: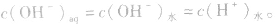
2.碱溶液
同理,在碱的水溶液中,OH-主要由碱电离产生,即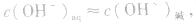 而H+是由水电离产生的:
而H+是由水电离产生的: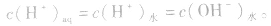
3.盐溶液
在盐的水溶液中,H+和OH-全部来自水的电离,且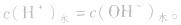
(1)若单一水解的盐的水溶液呈酸性,c(H+)> c(OH-),即弱碱阳离子水解


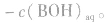
(2)若单一水解的盐的水溶液呈碱性,c(OH一)> c(H+),即弱酸阴离子水解
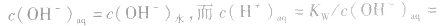
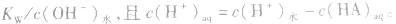
说明:由以上分析可以看出,在常温下(25℃):
酸(或碱)的溶液中,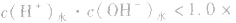
 发生水解的盐溶液中
发生水解的盐溶液中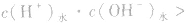
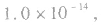 但
但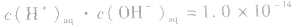 总成立。
总成立。
影响水电离平衡的因素:
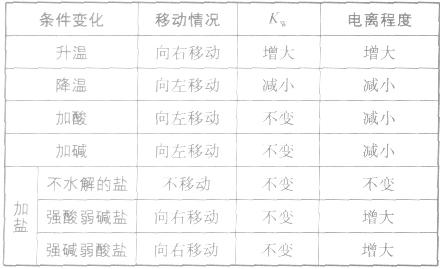
水的电离:
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O
 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L 注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
发现相似题
与“现有浓度均为0.1 mol/L的下列溶液:①硫酸 ②醋酸 ③氢氧化钠④...”考查相似的试题有:
- 下列有关说法正确的是 ( )A.25℃时,0.1mol·L-1的三种溶液的pH关系为:pH(NaHCO3) > pH(Na2CO3) >pH(CH3COONa)B.25℃时,p...
- (14分)已知醋酸是日常生活中常见的弱酸。(1)用pH试纸测定醋酸pH的操作是___________。(2)常温下在 pH =5的醋酸稀溶液中,醋...
- 把aL含(NH4)2SO4和NH4NO3的混和溶液分成两等份,一份加入b mol的烧碱并加热,恰好将全部NH4+转变成NH3放出;另一份需含c mol...
- 常温时,将V1mLclmol/L的氨水滴加到V2mL c2mol/L的盐酸中,下列结论正确的是A.若Vl=V2,cl=c2,则溶液中一定存在c(H+)=c(OH-...
- 已知水的电离方程式:H2O⇌H++OH-.下列叙述中,正确的是( )A.升高温度,KW增大,pH不变B.向水中加入氨水,平衡向逆反应方...
- 某学生用0.1mol/L的KOH标准溶液滴定未知浓度盐酸,其操作可分解为如下几步:A.移取20mL待测盐酸溶液注入洁净的锥形瓶,并加...
- 某温度下,水的离子积约为1×10-12,将VaL pH=2的硫酸溶液与VbL pH=11的NaOH溶液混合,若混合溶液的pH=10,体积是(Va+Vb)...
- 用惰性电极电解pH=6的CuSO4溶液500 mL,当电极上有16 mg铜析出时,溶液的pH约为(设电解前后溶液体积变化可忽略,阴极上无H2...
- 实验室用NaOH固体配制0.1 000mol·L-1NaOH溶液500mL. (1)用托盘天平称取NaOH固体________g.溶液配制过程用到下列玻璃仪器...
- 在常温下,0.1000mol·L-1Na2CO3溶液25mL 用0.1000mol·L-1盐酸滴定,其滴定曲线如图。对滴定过程中所得溶液中相关离子浓度间的...