本试题 “氮及其化合物在工农业生产中具有重要作用.(1)某小组进行工业合成氨N2(g)+3H2(g)⇌2NH3(g)△H<0的模拟研究,在1L密闭容器中,分别加入0.1molN2和0.3mo...” 主要考查您对一氧化氮
二氧化氮
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 一氧化氮
- 二氧化氮
氮的氧化物:
氮元素有+1、+2、+3、+4、+5五种正价,五种正价对应六种氧化物N2O(俗称“笑气”,具有麻醉作用)、 NO、N2O4(暗蓝色气体)、NO2、N2O4、N2O5(白色固体)。其中N2O3和N2O5分别是HNO2和HNO3的酸酐,它们都是空气污染物,空气中的NO2是造成光化学污染的主要因素。另外,在思考某些问题时,要注意:2NO2 N2O4。对气体体积及平均相对分子质量的影响:
N2O4。对气体体积及平均相对分子质量的影响:
氮元素有+1、+2、+3、+4、+5五种正价,五种正价对应六种氧化物N2O(俗称“笑气”,具有麻醉作用)、 NO、N2O4(暗蓝色气体)、NO2、N2O4、N2O5(白色固体)。其中N2O3和N2O5分别是HNO2和HNO3的酸酐,它们都是空气污染物,空气中的NO2是造成光化学污染的主要因素。另外,在思考某些问题时,要注意:2NO2
 N2O4。对气体体积及平均相对分子质量的影响:
N2O4。对气体体积及平均相对分子质量的影响:一氧化氮的物理性质和化学性质:
(1)物理性质:无色、不溶于水、有毒的气体,密度比空气稍重。
(2)化学性质:
①极易被空气中的O2氧化: 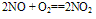
②NO中的氮为+2价,处于中间价态,既有氧化性又有还原性。
二氧化氮的物理性质和化学性质:
(1)物理性质:红棕色、有刺激性气味、有毒的气体,易溶于水、易液化,比空气重。
(2)化学性质:
与H2O反应: 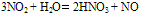
(工业制HNO3原理,在此反应中,NO2同时作氧化剂和还原剂)
NO、NO2的性质、实验室制法的比较:
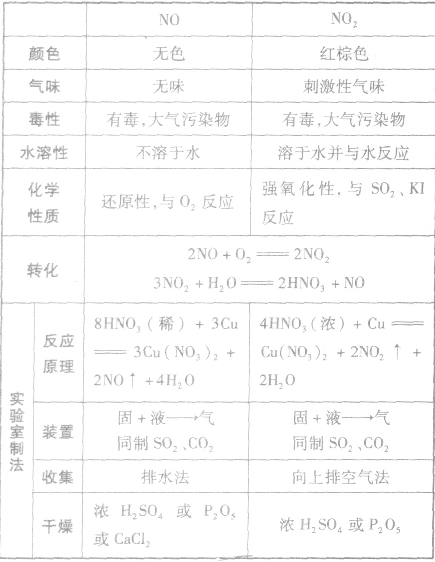
隐含反应: 的应用:
的应用:
通常“纯净”的NO2或N2O4并不纯,因为在常温、常压下能发生反应 ,由于此平衡的存在,导致一些物理量的理论值与实验值有一定的误差。例如:
,由于此平衡的存在,导致一些物理量的理论值与实验值有一定的误差。例如:
1.收集到的1mo1NO2在标准状况下的体积应小于22.4L
2.标准状况下22.4LNO2的质量大于46g。
3.NO与O2混合后,所得物质的相对分子质量应大于按体积比求得的数值。
4.温度影响“ ”平衡体系,其他条件不变,体系颜色随温度改变而改变。升高温度,气体颜色变深;降低温度,气体颜色变浅。
”平衡体系,其他条件不变,体系颜色随温度改变而改变。升高温度,气体颜色变深;降低温度,气体颜色变浅。
5.恒容时,在“ ”平衡体系中增加 N01,相当于增大压强。
”平衡体系中增加 N01,相当于增大压强。
有关混合气体NO、NO2、O2溶于水的计算:
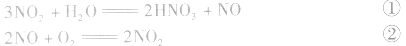
①×2+②得NO2、O2与水反应生成HN3,的化学方程式为: 
①×2+②×3得NO、O2与水反应生成HNO3的化学方程式为: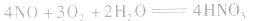
一般NO、NO2、O2与水反应,可归纳成四种情况:
1.NO和NO2混合 剩余气体为NO
剩余气体为NO
2.NO2和O2混合
3.NO和O2混合 
4.NO2、NO、O2的混合
当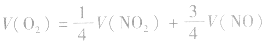 时,反应后无气体剩余
时,反应后无气体剩余
特例:当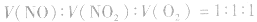 时,无气体剩余。
时,无气体剩余。
发现相似题
与“氮及其化合物在工农业生产中具有重要作用.(1)某小组进行工...”考查相似的试题有:
- 以下四组气体分别与对应的试纸接触,均能使试纸变蓝的是( ) 选项 湿润的淀粉-KI试纸 湿润红色石蕊试纸 A SO2 NH3 B H2S HCl...
- 实验室收集NO、NO2两种气体( ) A.均可用排水法 B.均可用向上排空气法 C.NO用向上排空气法、NO2用排水法 D.NO用排水法、...
- 下列说法中,不正确的是( )A.少量白磷可以保存在煤油中B.少量金属钠可以保存在煤油中C.浓硝酸应保存在棕色试剂瓶中D.漂...
- 使用单质铜制硝酸铜,耗用原料最经济,而且对环境几乎没有污染的是( )
- 在标准状况下,250 mL烧瓶充满氨气后,倒置于水槽中,假设溶解后的溶质不向烧瓶外扩散,则烧瓶中氨水的物质的量浓度接近于( ...
- 某研究性学习小组设计实验方案来研究稀硝酸与铜反应生成NO。(1)补充完成下列实验步骤:①_________________________________...
- 下列有关说法,错误的是[ ]A.氮氧化物、二氧化硫都是形成酸雨的主要物质B.工业合成氨及用NH3制化肥(NH4)2SO4都属于氮的固定...
- 1.92gCu片与一定量的浓HNO3作用,当收集到NO2和NO气体共1.12L时(标准状况),金属铜恰好全部作用。则:(1)反应中消耗HNO...
- 有a、b、c、d、e五种气体,进行下列实验:(1)a和b混合气体变红棕色(2)c和d混合产生白烟 (3)c和e分别通入少量溴水中溴水...
- (12)氨是重要的无机化工原料,也是合成氮肥的主要原料,因此合成氨在国民经济中占有重要地位。⑴工业合成氨反应的化学方程式为...