本试题 “下面是一些原子的电子排布式,其中不是激发态原子的是[ ]A.1s22s22p2B.1s22s23s1C.1s22s24d1D.1s22s22p23s1” 主要考查您对电子排布式
基态与激发态、光谱
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电子排布式
- 基态与激发态、光谱
电子排布式:
①简化电子排布式
为了避免电子排布式书写过于繁琐,把内层电子达到稀有气体元素原子结构的部分以相应稀有气体的冗素符号外加方括号表示,即为简化电子排布式,如K 的简化电子排布式为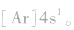
②特殊电子排布式
有个别元素的基态原子的电子排布对于构造原理有1个电子的反常。因为能量相同的原子轨道在全充满( )、半充满(
)、半充满(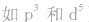 )和全空(
)和全空(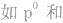
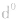 )状态时,体系的能量较低,原子较稳定。
)状态时,体系的能量较低,原子较稳定。 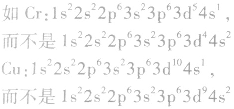
(2)电子排布图:用方框表示一个原子轨道,用箭头“↑”或“↓”来区别自旋状态不同的电子。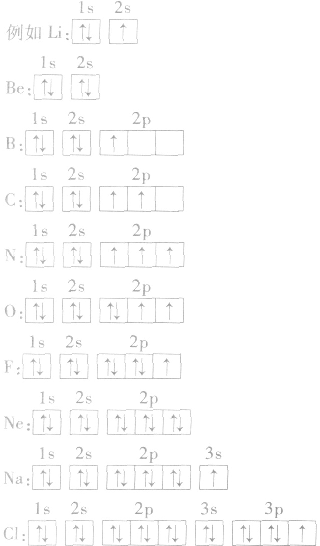
构造原理:
多电子原子的核外电子排布总是按照能量最低原理,由低能级逐步填充到高能级。绝大多数元素的原子核外电子的排布遵循下图所示的排布顺序,这种排布顺序被称为构造原理。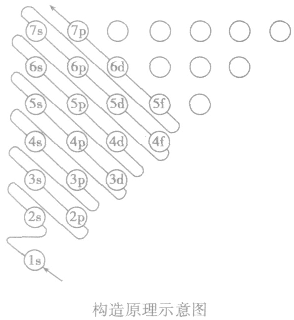
点拨:构造原理中的排布顺序,其实质是各能级的能量高低顺序,可由下列公式得出ns<(n一2)f< (n一1)d<np(n表示能层序数)。常用的重要的能级交错顺序有: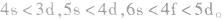
核外电子排布式一构造原理的应用:
根据构造原理,按照能级顺序,用能级符号右上角的数字表示该能级上电子数的式子,叫做电子排布式。例如,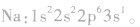
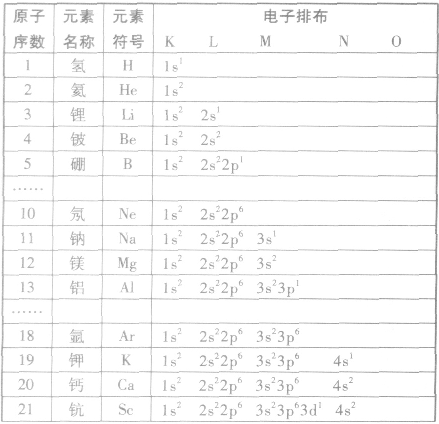
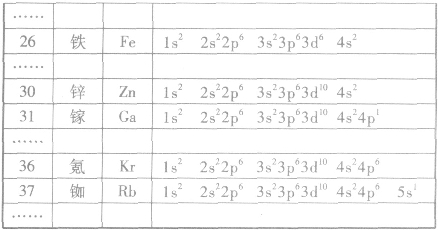
能量最低原理、基态与激发态、光谱:
1.能量最低原理
原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,简称能量最低原理。
2.基态原子与激发态原子
处于最低能量的原子叫做基态原子。当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。
例如:基态碳原子的价电子排布为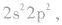 而激发态时电子排布为
而激发态时电子排布为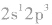 (1个2s能级上的电子跃迁到了2p能级上)。
(1个2s能级上的电子跃迁到了2p能级上)。
3.光谱与光谱分析
(1)原子光谱:不同元素的原子发生跃迁时会吸收或释放不同的光,可以用光谱仪摄取各种元素的电子的吸收光谱或发射光谱,总称原子光谱。
(2)发射光谱与吸收光谱

(3)光谱分析:在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析。
与“下面是一些原子的电子排布式,其中不是激发态原子的是[ ]A.1s...”考查相似的试题有:
- 甲、乙、丙、丁、戊为原子序数依次增大的短周期元素。甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是...
- 含有非极性键且分子中各原子都满足8电子稳定结构的是( )A.CH4B.CO2C.BeCl2D.N2
- 已知A、B、C、D均为周期表中前36号元素,且原子序数依次增大。A、B、C为同一周期的主族元素,A原子最外层有3个未成对电子,B...
- A、B、C、D分别代表四种不同的短周期元素。A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素原子的最...
- (三选一)【化学-物质结构与性质】氯是一种非常重要的非金属元素。(1)氯元素的基态原子的价电子层排布式是____________。...
- [化学-物质结构与性质]短周期六元素A、B、C、D、E、F,原子序数依次增大;A、B的阴离子与C、D的阳离子的电子排布式均为ls22s2...
- 下列关于元素的叙述正确的是( )A.目前使用的元素周期表中,最长的周期含有36种元素B.只有在原子中,质子数才与核外电子数...
- 下列表达方式正确的是( )A.Na+的电子排布图:B.Na原子的简化电子排布式:[Na]3s1C.钾原子的基态原子结构示意图为:D.H2...
- 二茂铁分子[Fe (C5H5)2]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等....
- 为了解释原子的稳定性和_______的实验事实,丹麦科学家玻尔在 __________原子模型的基础上提出了_________的原子结构模型,该...