本试题 “将37.2gNa、Na2O、Na2O2组成的混合物放入盛有206.4mL水(密度为1.0g/cm3)的特定容器中充分反应,将反应后产生的气体全部收集,收集到的气体通过放电恰好完全...” 主要考查您对溶液质量分数的计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶液质量分数的计算
溶液质量分数的计算:
(1)溶质的质量分数=
(2)溶质的质量分数、溶质的物质的量浓度及溶液密度之间的关系:
①溶质的质量分数=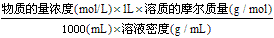
②物质的量浓度=
(1)溶质的质量分数=

(2)溶质的质量分数、溶质的物质的量浓度及溶液密度之间的关系:
①溶质的质量分数=
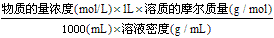
②物质的量浓度=

有关溶液密度的问题:
1.溶液质量分数与密度的关系
(1)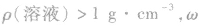 越大,则ρ(溶液)越大,常见溶液如NaCl溶液、硫酸溶液等。
越大,则ρ(溶液)越大,常见溶液如NaCl溶液、硫酸溶液等。
(2)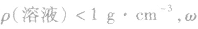 越大,则ρ(溶液)越小,常见溶液如氨水、酒精溶液等。
越大,则ρ(溶液)越小,常见溶液如氨水、酒精溶液等。
2.溶液混合后质量分数的变化规律
质量分数分别为 的两溶液(同种溶质)混合,混合后溶液的质量分数为ω。
的两溶液(同种溶质)混合,混合后溶液的质量分数为ω。
(1)等体积混合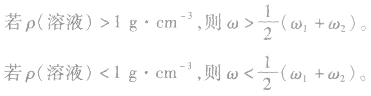
若是加等体积水稀释,可视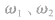 中其一为0 分析。
中其一为0 分析。
(2)等质量混合: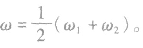
发现相似题
与“将37.2gNa、Na2O、Na2O2组成的混合物放入盛有206.4mL水(密度...”考查相似的试题有:
- 氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.5%。工业上常通过下列反...
- 常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,混合后得到密度为1.17 g/cm3的溶液。请计算:(1)混合后溶液中Na...
- 20℃时,饱和KCl溶液的密度为1.174g•cm-3,物质的量浓度为4.0mol•L-1,则下列说法中正确的是( )A.25℃时,饱和KCl溶液的浓度...
- 在25℃时,硫酸铜的溶解度为S g,在该温度下,把S克无水硫酸铜粉末加入(100+S)克饱和硫酸铜溶液中,得到一定量的蓝色晶体....
- (1)已知硫酸溶液的浓度越大密度也越大.和50%的H2SO4溶液等质量混合后,所得溶液溶质的质量分数______(填“大于”“小于”或“...
- 下列坐标图所表示的量的关系错误的是( )A.烷烃分子中碳原子数x与碳的质量分数y的关系B.NOx溶于水完全转化为硝酸,x与消耗...
- 工业上以CaO和HNO3为原料制备Ca(NO3)2·4H2O晶体。为了确保制备过程中既不补充水,也无多余水分,所用硝酸溶液溶质的质量分数...
- 下列叙述正确的是( )A.①分液,②过滤,③分馏,④重结晶都是混合物分离常用方法,其中根据粒子大小分离的只有②B.欲配制质量...
- 某温度下,100 g饱和氯化钠溶液中含有氯化钠26.5 g。若向此溶液中添加3.5 g氯化钠和6.5 g水,则所得溶液的溶质质量分数是[ ]A...
- 50g物质的量浓度为C1的浓H2SO4,质量分数为W1,与体积为V的水混合后得到物质的量浓度为C2的稀H2SO4,质量分数为W2(以下填“>...