本试题 “下列叙述不正确的是[ ]A.元素的化学性质主要取决于原子的最外层电子数B.16O、17O和18O互为同位素,化学性质基本相同C.相同温度下,在任何物质的水溶液中,...” 主要考查您对同位素
强电解质、弱电解质
水的离子积常数
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 同位素
- 强电解质、弱电解质
- 水的离子积常数
定义:
质子数相同而中子数不同的原子互称为同位素(即同一元素的不同核素互称为同位素)。元素符号表示不同,如 ;电子结构相同,原子核结构不同;物理性质不同,化学性质相同。
;电子结构相同,原子核结构不同;物理性质不同,化学性质相同。
同位素的应用:
(1)同位素在医学领域中的应用最为广泛,主要用于显像、诊断和治疗,还用于医疗用品消毒、药物作用机理研究和生理医学研究等。
(2)同位素辐射育种技术为农业提供了改进农产品质量、增加产量的新技术;利用同位素示踪技术,可检测并确定植物的最佳肥料吸入量和农药吸入量。
(3)14C纪年测定法与其他放射性同位素测定法已成为地质学、考古学、人类学、地球科学等领域广泛采用的一种准确的断代方法。
在水溶液里或熔融状态下,能全部电离的化合物。包括:强酸、强碱、大多数盐、活泼金属氧化物等;完全电离、不可逆、不存在电离平衡;电离方程式用“=”表示。
弱电解质:
在水溶液里或熔融状态下,不能全部电离的化合物。包括:弱酸、弱碱、少数盐等;部分电离、可逆、存在电离平衡,电离方程式用“
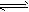 ”表示。
”表示。 强电解质和弱电解质的比较:
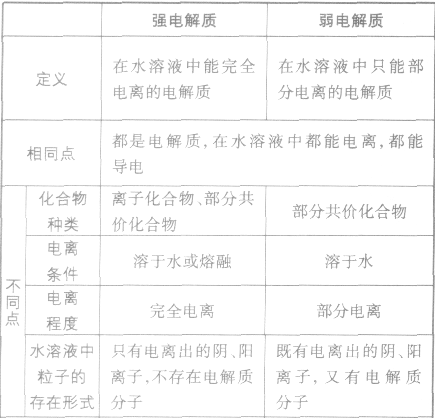
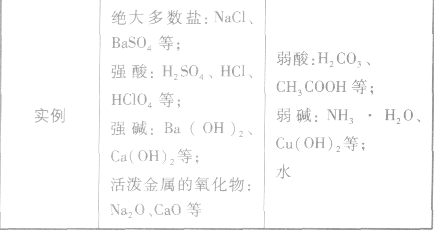
强弱电解质的判断依据:
1.在相同浓度、相同温度下,与强电解质做导电性对比实验.
2.浓度与pH的关系。如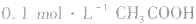 溶液的pH>1,则证明
溶液的pH>1,则证明 是弱电解质。
是弱电解质。
3.测定对应盐溶液的酸碱性。如 溶液呈碱性,则证明醋酸是弱电解质。
溶液呈碱性,则证明醋酸是弱电解质。
4.稀释前后的pH变化与稀释倍数的关系。例如,将pH=2的酸溶液稀释1000倍,若pH<5,则证明该酸为弱电解质;若pH=5,则证明该酸为强电解质。
5.采用实验证明电离平衡。如向醋酸溶液中滴人石蕊试液,溶液变红,再加入醋酸钠晶体,颜色变浅。
水的电离:
水是一种极弱的电解质,它能微弱地电离:
实验测得:25℃时,1L纯水中只有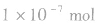 的水分子发生电离,故25℃时纯水中
的水分子发生电离,故25℃时纯水中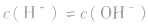

水的离子积:
在一定温度下,水电离出的c(H+)与c(OH-)的乘积是一个常数,称为水的离子积常数,简称水的离子积,用符号 表示,即
表示,即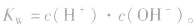
(1)在一定温度下,水的离子积都是一个常数,在25℃时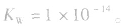
(2)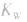 随温度的变化而变化,温度升高,
随温度的变化而变化,温度升高,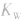 增大。
增大。
(3)水的离子积常数揭示了在任何水溶液中均存在水的电离平衡,都有 存在。在酸性或碱性的稀溶液中,当温度为25℃时,
存在。在酸性或碱性的稀溶液中,当温度为25℃时,
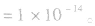
(4)在酸或碱的稀溶液中,由水电离出的c(H+)和c(OH-)总相等.即 如25℃时
如25℃时 或NaOH溶液中,
或NaOH溶液中,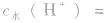
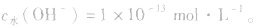
溶液中c(H+)或c(OH-)的计算:
常温下,稀溶液中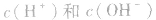 的乘积总是
的乘积总是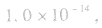 知道
知道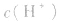 就可以计算出
就可以计算出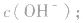 反之亦然
反之亦然
1.酸溶液
当在水中加入酸后,将使水的电离平衡向左移动 (抑制水的电离)。在酸的水溶液中,H+主要由酸电离产生,即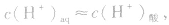 而OH-是由水电离产生的:
而OH-是由水电离产生的: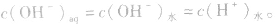
2.碱溶液
同理,在碱的水溶液中,OH-主要由碱电离产生,即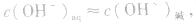 而H+是由水电离产生的:
而H+是由水电离产生的: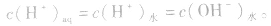
3.盐溶液
在盐的水溶液中,H+和OH-全部来自水的电离,且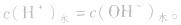
(1)若单一水解的盐的水溶液呈酸性,c(H+)> c(OH-),即弱碱阳离子水解


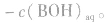
(2)若单一水解的盐的水溶液呈碱性,c(OH一)> c(H+),即弱酸阴离子水解
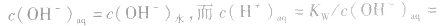
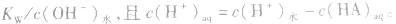
说明:由以上分析可以看出,在常温下(25℃):
酸(或碱)的溶液中,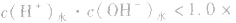
 发生水解的盐溶液中
发生水解的盐溶液中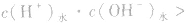
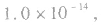 但
但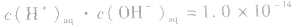 总成立。
总成立。
与“下列叙述不正确的是[ ]A.元素的化学性质主要取决于原子的最...”考查相似的试题有:
- 与铂同族的贵金属钯(Pd)有多种同位素.下列关于46103Pd、46104Pd的说法正确的是( )A.质子数相同,互称为同位素B.中子数...
- 下列叙述正确的是( )A.168O2和188O2互为同位素,性质相似B.常温下,H+、NO3-、Fe2+可以大量共存C.最外层有2个电子的原子...
- 下列说法正确的是( )A.同位素:1H、D+、T2B.0.1 mol的OH-与0.1 mol的-OH中所含质子数相等C.1molC5H12分子中含有17×6.02×...
- 我国的“神州六号”载人飞船已发射成功,“嫦娥”探月工程已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨3...
- 下列说法正确的是[ ]A.在水溶液中导电能力弱的电解质一定是弱电解质B.强电解质的水溶液导电能力一定比弱电解质水溶液的导电能...
- 下列有关叙述中正确的是:A.难溶于水的电解质一定是弱电解质B.强电解质的水溶液导电能力一定比弱电解质水溶液的导电能力强C...
- 当光束通过下列分散系时,能形成一条光亮通路的是 A.食盐水B.碘酒C.淀粉溶液D.Fe(OH)3沉淀
- 常温下,用0.1000 mol/L HCl溶液滴定20.00 mL 0.1000 mol/L NH3•H2O溶液,滴定曲线如下图。下列说法正确的是A.①溶液:c(C1—)...
- 下列叙述正确的是A.可以根据PbI2和AgCl的Ksp的大小比较两者的溶解度B.常温下,同浓度的Na2S与NaHS溶液相比,NaHS溶液的pH大...
- 下列有关溶液中粒子浓度的关系式中,正确的是( )A.pH相同的①CH3COONa、②NaHCO3、③Na2CO3三份溶液中的c(Na+):③>②>①B.0...