本试题 “汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体.(1)汽油在不同空燃比(空气与燃油气的体积比)时尾气的...” 主要考查您对一氧化氮
二氧化氮
盖斯定律
能量的相互转化
影响化学反应速率的因素
勒夏特列原理
有机物的合成
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 一氧化氮
- 二氧化氮
- 盖斯定律
- 能量的相互转化
- 影响化学反应速率的因素
- 勒夏特列原理
- 有机物的合成
氮元素有+1、+2、+3、+4、+5五种正价,五种正价对应六种氧化物N2O(俗称“笑气”,具有麻醉作用)、 NO、N2O4(暗蓝色气体)、NO2、N2O4、N2O5(白色固体)。其中N2O3和N2O5分别是HNO2和HNO3的酸酐,它们都是空气污染物,空气中的NO2是造成光化学污染的主要因素。另外,在思考某些问题时,要注意:2NO2
 N2O4。对气体体积及平均相对分子质量的影响:
N2O4。对气体体积及平均相对分子质量的影响:一氧化氮的物理性质和化学性质:
(1)物理性质:无色、不溶于水、有毒的气体,密度比空气稍重。
(2)化学性质:
①极易被空气中的O2氧化: 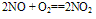
②NO中的氮为+2价,处于中间价态,既有氧化性又有还原性。
二氧化氮的物理性质和化学性质:
(1)物理性质:红棕色、有刺激性气味、有毒的气体,易溶于水、易液化,比空气重。
(2)化学性质:
与H2O反应: 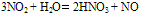
(工业制HNO3原理,在此反应中,NO2同时作氧化剂和还原剂)
NO、NO2的性质、实验室制法的比较:
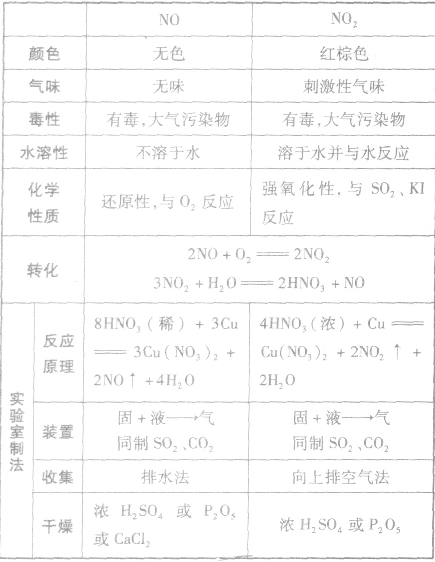
隐含反应: 的应用:
的应用:
通常“纯净”的NO2或N2O4并不纯,因为在常温、常压下能发生反应 ,由于此平衡的存在,导致一些物理量的理论值与实验值有一定的误差。例如:
,由于此平衡的存在,导致一些物理量的理论值与实验值有一定的误差。例如:
1.收集到的1mo1NO2在标准状况下的体积应小于22.4L
2.标准状况下22.4LNO2的质量大于46g。
3.NO与O2混合后,所得物质的相对分子质量应大于按体积比求得的数值。
4.温度影响“ ”平衡体系,其他条件不变,体系颜色随温度改变而改变。升高温度,气体颜色变深;降低温度,气体颜色变浅。
”平衡体系,其他条件不变,体系颜色随温度改变而改变。升高温度,气体颜色变深;降低温度,气体颜色变浅。
5.恒容时,在“ ”平衡体系中增加 N01,相当于增大压强。
”平衡体系中增加 N01,相当于增大压强。
有关混合气体NO、NO2、O2溶于水的计算:
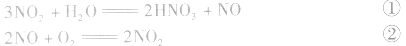
①×2+②得NO2、O2与水反应生成HN3,的化学方程式为: 
①×2+②×3得NO、O2与水反应生成HNO3的化学方程式为: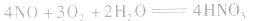
一般NO、NO2、O2与水反应,可归纳成四种情况:
1.NO和NO2混合 剩余气体为NO
剩余气体为NO
2.NO2和O2混合
3.NO和O2混合 
4.NO2、NO、O2的混合
当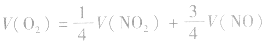 时,反应后无气体剩余
时,反应后无气体剩余
特例:当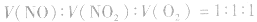 时,无气体剩余。
时,无气体剩余。
不管化学反应是一步完成还是分几步完成,其反应热是相同的。换句话说,化学反应的反应热只与反应的始态和终态有关,而与反应进行的途径无关。如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一一步完成时的反应热是相同的,这就是盖斯定律。
盖斯定律的意义:
利用盖斯定律可以间接计算某些不能直接测得的反应的反应热。例如:
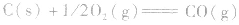 的△H无法直接测得,可以结合下面两个反应的△H,利用盖斯定律进行计算。
的△H无法直接测得,可以结合下面两个反应的△H,利用盖斯定律进行计算。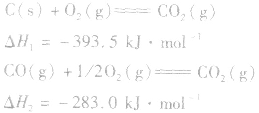
根据盖斯定律,就可以计算出所给反应的△H。分析上述两个反应的关系,即知
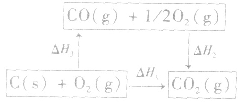
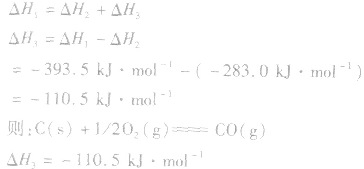
盖斯定律在反应热大小比较中的应用:
1.同一反应生成物状态不同时
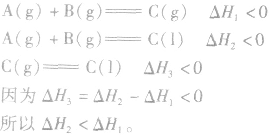
若按以下思路分析:
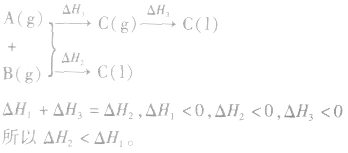
2.同一反应物状态不同时
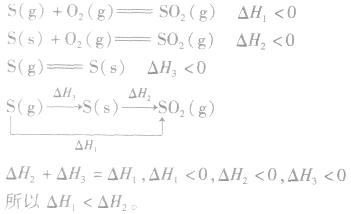
3.两个有联系的不同反应相比
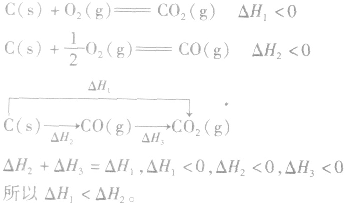
并且据此可写出下面的热化学方程式:

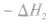
能量的相互转化:
化学反应中的能力变化表现为热量的变化。常见能量转化有:化学能和电能的相互转化、化学能和热能的相互转化、化学能和光能、风能的相互转化等。
如:燃料燃烧产生能量最终带动发电机发电,将化学能转化为电能;铜、锌形成原电池,将化学能转化为电能。
1.内因:参加反应的物质的结构及性质。
2.外因:主要是指浓度、温度、压强和催化剂,另外还有光、超声波、激光、搅拌、固体表面积、形成原电池等。
(1)浓度:其他条件相同时,增大反应物浓度,化学反应速率增大;减小反应物浓度,化学反应速率减小。在一定温度下,同体、纯液体的浓度视为定值,如C与CO2的反应、Na与H2O的反应中,C的量和Na、H2O 的量减少并不意味着其“浓度”减小,即不冈其量的增减而影响反应速率,但会因固体表面积的变化而改变反应速率。
(2)温度:其他条件相同时,升高温度,可以加快反应速率,实验测得,温度每升高10℃,化学反应速率通常增大到原来的2~4倍。
经验公式为
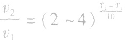
(3)压强:对于气体反应,当温度不变时,增大压强可以加快反应速率。对于气体反应体系,压强改变时有以下几种情况:

(4)催化剂:催化剂是能改变化学反应速率但在反应前后本身的质量和化学性质都不变的物质。对于某些化学反应,使用正催化剂能显著加快化学反应速率。
(5)其他因素:增大同体的表面积(如将块状改为粉末状),可增大反应速率;光照一般也可增大某些反应的速率;形成原电池可以加快反应速率;此外,超声波、放射线、电磁波等因素也能影响反应速率。
3.外因对化学反应速率影响的微观解释
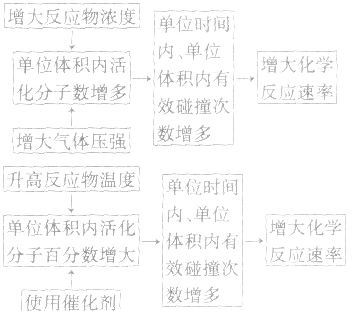
如果改变影响平衡的一个条件(如浓度、压强、温度),平衡将向着能够减弱这种改变的方向移动。勒夏特列原理又叫平衡移动原理。
适用范围:
平衡移动原理适用于化学平衡、溶解平衡、电离平衡、水解平衡等动态平衡。
注意事项:
(1)平衡向“减弱”外界条件变化的方向移动,但不能“抵消”外界条件的变化。
(2)
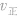 增大并不意味着平衡一定向正反应方向移动,只有
增大并不意味着平衡一定向正反应方向移动,只有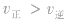 时才可以肯定平衡向正反应方向移动。
时才可以肯定平衡向正反应方向移动。 (3)当平衡向正反应方向移动时,反应物的转化率并不一定提高,生成物的体积分数也并不一定增大(因为反应物或反应混合物的总量增大了),增大一种反应物的浓度会提高另一种反应物的转化率。
(4)存在平衡且平衡发生移动时才能应用平衡移动原理。
分析思路:
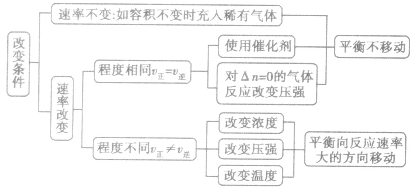
有机合成过程主要包括两个方面,
其一是碳原子骨架的变化,例如碳链的增长和缩短、链状和环状的互相转化;
其二是官能团的引入和消除、官能团的衍变等变化。
解答有机物的合成相关题目的方法:
考查有机合成实质是根据有机物的性质,进行必要的官能团反应,从而达到考查官能团性质的目的。因此,要想熟练解答此类问题,须掌握如下知识:
(1)官能团的引入:
在有机化学中,卤代烃可谓烃及烃的衍生物的桥梁,只要能得到卤代烃,就可能得到诸如含有羟基、醛
基、羧基、酯基等官能团的物质。此外,由于卤代烃可以和醇类相互转化,因此在有机合成中,如果能引入羟
基,也和引入卤原子的效果一样,其他有机物都可以信手拈来。同时引入羟基和引入双键往往是改变碳原子骨
架的终南捷径,因此官能团的引入着重总结羟基、卤原子、双键的引入。
①引入羟基(-OH)
A. 醇羟基的引入:烯烃与水加成、卤代烃水解、醛(酮)与氢气的加成、酯的水解等。
B. 酚羟基的引入:酚钠盐过渡中通入CO2,
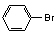 的碱性水解等。
的碱性水解等。 C. 羧羟基的引入:醛氧化为酸(被新制Cu(OH)2悬浊液或银氨溶液氧化)、酯的水解等。
②引入卤原子:烃与卤素取代、不饱和烃与HX或X2加成、醇与HX取代等。
③引入双键:某些醇或卤代烃的消去引入C=C键、醇的氧化引入C=O键等。
(2)官能团的消除:
①通过加成消除不饱和键。
②通过消去、氧化或酯化等消除羟基(-OH)
③通过加成或氧化等消除醛基(-CHO)
(3)官能团间的衍变: 可根据合成需要(或题目中所给衍变途径的信息),进行有机物官能团的衍变,以使中间物向产物递进。常见方式有以下三种:
①利用官能团的衍生关系进行衍变:如以丙烯为例,看官能团之间的转化:

上述转化中,包含了双键、卤代烃、醇、醛、羧酸、酯高分子化合物等形式的关系,领会这些关系,基本可
以把常见的有机合成问题解决。
②通过某种化学途径使一个官能团变为两个,如
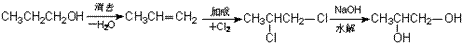
③通过某种手段,改变官能团的位置:如:
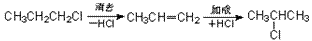
(4)碳骨架的变化:
①碳链增长:若题目中碳链增长,课本中目前的知识有:酯化反应、氨基缩合反应、不饱和结构与HCN的加
成反应、不饱和化合物间的聚合,此外常由信息形式给出,例如羟醛缩合反应、卤代烃与金属钠反应等。
例如:

②碳链变短:碳链变短的形式有烃的裂化裂解,某些烃(如烯烃、苯的同系物)的氧化、羧酸及盐的脱羧反应等。
例如:
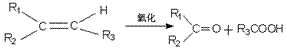
③链状变环状:不饱和有机物之间的加成,同一分子中或不同分子中两个官能团互相反应结合成环状结构。
例如,-OH与-OH间的脱水、羧基和羟基之间的反应、氨基和羧基之间的反应等。
④环状变链状:酯及多肽的水解、环烯的氧化等。当然,掌握上述相关知识后,还要分析要合成的有机物的结构,对比官能团与所给原料的官能团的异同,展开联想,理清衍变关系。同时深入理解并充分运用新信息要注意新信息与所要求合成的物质间的联系,找出
其结合点或共同性质,有时根据需要还应从已知信息中通过对比、分析、联想,开发出新的信息并加以利用。
与“汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,...”考查相似的试题有:
- 汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源,治理的方法之一是在汽车的排气管上装一个“催化 转换器”(铂、...
- 下列物质间转化都能通过一步实现的是[ ]A.Si→SiO2→H2SiO3→Na2SiO3B.Al→Al2O3→NaAlO2→Al(OH)3C.S→SO3→H2SO4→SO2D.N2→NO2→H...
- 为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2.已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ•...
- (2014届江西省景德镇市高三第一次模拟考试卷理综化学试卷)某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直...
- 下表中是各组反应的反应物和温度,反应刚开始时,放出H2速率最快的是[ ] 金属(粉末状)(mol)酸的浓度及体积反应温度(℃)A...
- 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如右的...
- 已知N2(g)+3H2(g)2NH3(g),正反应为放热反应,2SO2(g)+O2(g)2SO3(g),正反应为放热反应。回答下列问题:(1)从影响反应速率...
- 下列各图中能表示A(g)+B(g)2C(g)(正反应放热)这个可逆反应的图像为[ ]A.B.C.D.
- 化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。A的相关反应如下图所示: 已知R—CH=CHOH(烯醇)不稳...
- 汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体.(1)汽油在不同空燃比(...